
 2Fe+Al2O3;
2Fe+Al2O3; 2Fe+Al2O3 ;
2Fe+Al2O3 ;

 新思維寒假作業(yè)系列答案
新思維寒假作業(yè)系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
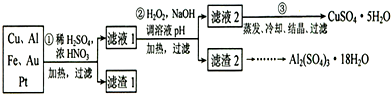
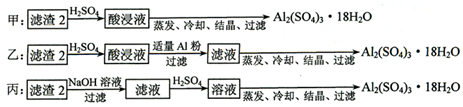
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
 CaO+CO2↑
CaO+CO2↑ 2Fe+3CO2
2Fe+3CO2查看答案和解析>>
科目:高中化學 來源: 題型:單選題
| 選項 | 陳述I | 陳述Ⅱ |
| A | SO3可與水反應(yīng) | 工業(yè)生產(chǎn)硫酸用水吸收SO3 |
| B | Cl2和SO2都有較好的漂白作用 | Cl2和SO2混合后可用于漂白紙漿 |
| C | 鋁的最外層電子較鈉多 | 鈉的金屬性強于鋁 |
| D | 石墨常用作電解池的電極 | 石墨的化學性質(zhì)穩(wěn)定且導電性好 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com