
分析 (1)電解質導電的原因:含有自由移動的離子或自由電子;
電解質是在水溶液里或熔融狀態下能導電的化合物是電解質,包括酸、堿、鹽、活潑金屬氧化物和水;
非電解質是在水溶液里和熔融狀態下都不能導電的化合物,包括一些非金屬氧化物、氨氣、大多數有機物(如蔗糖、酒精等);
(2)鐵與鹽酸反應生成氯化亞鐵和氫氣;
氯氣與氫氧化鈣反應生成氯化鈣、次氯酸鈣和水;
(3)分析反應中元素化合價變化,所含元素化合價升高的反應物為還原劑,對應產物為氧化產物;所含元素化合價降低的反應物為氧化劑,對應產物為還原產物;依據氧化還原反應得失電子守恒書寫方程式,計算轉移電子數.
解答 解:(1)①鐵單質含有自由電子,能夠導電,既不是電解質也不是非電解質;
②石墨屬于單質,含有自由電子,能夠導電,既不是電解質也不是非電解質;
③氯氣 是單質,不含自由移動的離子或自由電子,不導電;既不是電解質也不是非電解質;
④硫酸鋇晶體不含自由移動的離子或自由電子,不導電;熔化狀態下能夠導電的化合物屬于電解質;
⑤純硫酸不含自由移動的離子或自由電子,不導電;水溶液中能夠導電的化合物屬于電解質;
⑥鹽酸含自由移動的離子,能夠導電;屬于混合物,既不是電解質也不是非電解質;
⑦澄清石灰水含自由移動的離子,能夠導電;屬于混合物,既不是電解質也不是非電解質;
⑧乙醇不含自由移動的離子或自由電子,不導電;水溶液和熔融狀態下都不導電的化合物,是非電解質;
⑨熔化的硝酸鉀含自由移動的離子,能夠導電;屬于電解質;
⑩FeCl2溶液含自由移動的離子,能夠導電;是混合物,既不是電解質也不是非電解質;
所以:中能導電的是①②⑥⑦⑨⑩;屬于電解質的是④⑤⑨;
故答案為:①②⑥⑦⑨⑩;④⑤⑨;
(2)鐵與鹽酸反應生成氯化亞鐵和氫氣,離子方程式:Fe+2H+═Fe2++H2↑,
故答案為:Fe+2H+═Fe2++H2↑;
氯氣與氫氧化鈣反應生成氯化鈣、次氯酸鈣和水,離子方程式:Cl2+2OH-=Cl-+ClO-+H2O;
故答案為:Cl2+2OH-=Cl-+ClO-+H2O;
(3)反應中過氧化氫中-1價的氧化合價降低為-2價,過氧化氫為氧化劑,氯化亞鐵中-2價化合價升高為-3價,被氧化對應氯化鐵為氧化產物,依據得失電子守恒、原子個數守恒,方程式為:2HCl+1H2O2+2FeCl2=2FeCl3+2H2O,用單線橋表示為: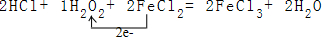 ;
;
依據方程式可知生成2mol水即36g水轉移電子數為2mol,則生成9g水轉移電子數為0.5mol;
故答案為: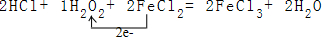 ;負1價氧;FeCl3(Fe3+);0.5;
;負1價氧;FeCl3(Fe3+);0.5;
點評 本題考查了電解質的判斷及離子方程式的書寫、氧化還原反應方程式配平及有關電子轉移的計算,題目難度不大,注意單質、混合物既不是電解質也不是非電解質.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 7種和2種 | B. | 8種和3種 | C. | 42種和3種 | D. | 56種和3種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
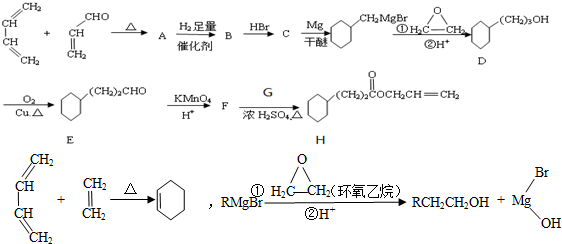
 ,G物質核磁共振氫譜共有4個峰.
,G物質核磁共振氫譜共有4個峰. .寫出D生成E的化學方程式
.寫出D生成E的化學方程式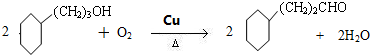 .
.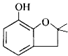 呋喃酚是一種合成農藥的重要中間體,它的同分異構體很多,寫出符合下列條件的所有芳香族同分異構體的結構簡式:
呋喃酚是一種合成農藥的重要中間體,它的同分異構體很多,寫出符合下列條件的所有芳香族同分異構體的結構簡式: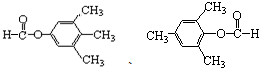 .
.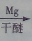 CH3CH2MgBr
CH3CH2MgBr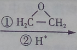 CH3CH2CH2CH2OH.
CH3CH2CH2CH2OH.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | (NH4)2CO3+H2SO4═(NH4)2SO4+H2O+CO2↑ | |
| B. | NaHCO3+HNO3═NaNO3+H2O+CO2↑ | |
| C. | Na2CO3+2CH3COOH═2CH3COONa+H2O+CO2↑ | |
| D. | CaCO3+2HCl═CaCl2+H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 硫化亞鐵溶于足量稀硝酸中:FeS+2H+═Fe2++H2S↑ | |
| B. | 石灰石溶于醋酸:CaCO3+2CH3COOH═2CH3COO-+Ca2++CO2↑+H2O | |
| C. | FeCl2溶液中通入少量氯氣:Fe2++Cl2═Fe3++2Cl- | |
| D. | 硫酸亞鐵溶液中滴加酸化的雙氧水:2Fe2++2H++H2O2═2Fe3++2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
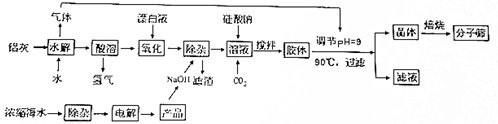
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 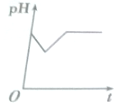 | B. | 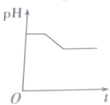 | C. | 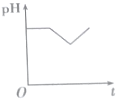 | D. |  |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com