
| 裝置序號 | 實驗現象或作用 | 實驗結論或化學方程式 |
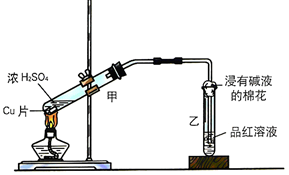
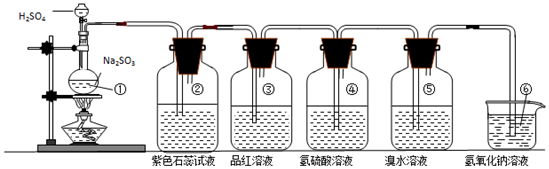
| ① | 有氣泡產生 | 化學方程式為:Na2SO3+H2SO4(濃)=Na2SO4+H2O+SO2↑ |
| ② | 紫色石蕊試液變紅色 | 證明SO2溶于水顯酸性 |
| ③ | 品紅溶液褪色 | 證明SO2具有漂白性 |
| ④ | 溶液變渾濁 | 證明SO2具有氧化性 |
| ⑤ | 溴水褪色 | 證明SO2具有還原性 |
| ⑥ | 吸收尾氣 | 證明SO2屬于酸性氧化物 |
分析 (1)①銅與濃硫酸反應生成硫酸銅和二氧化硫氣體;
②評價實驗方案要從反應的可操作性,生成物的性質,環保節能等方面分析.由于濃硫酸與銅直接反應時會生成有毒的二氧化硫,且需要的硫酸量較大所以一般不采用這種方式進行;
(2)①亞硫酸鈉與濃硫酸反應生成二氧化硫、硫酸鈉和水;
②二氧化硫溶于水和水反應生成亞硫酸,亞硫酸為弱酸;酸可以使紫色石蕊試液變紅;
③二氧化硫與品紅化合生成無色物質,能使品紅溶液褪色;
④SO2中+4價S具有氧化性,硫化氫中-2價S具有還原性,二氧化硫能把硫化氫氧化成單質硫,本身被還原成單質硫;
⑤二氧化硫具有還原性,能夠被溴水氧化;
⑥二氧化硫有毒,不能直接排放到空氣中,為酸性氧化物能夠與氫氧化鈉反應生成亞硫酸鈉和水.
解答 解:(1)①銅與濃硫酸反應生成硫酸銅和二氧化硫氣體,反應的化學方程式為:Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,故答案為:Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
②甲方案生成二氧化硫,二氧化硫是一種有毒氣體,所以甲方案不可取,通過計算可知生成相同質量的硫酸銅,乙方案消耗的硫酸少,既節約了原料,又不污染環境.
故答案為:乙;甲有二氧化硫產生,污染空氣,乙無污染,硫酸利用率高;
(2)①中為亞硫酸鈉和濃硫酸反應生成二氧化硫氣體,反應的化學方程式為:Na2SO3+H2SO4(濃)=Na2SO4+SO2↑+H2O,
故答案為:Na2SO3+H2SO4(濃)=Na2SO4+H2O+SO2↑;
②氧化硫溶于水和水反應生成亞硫酸,亞硫酸為弱酸,可以使紫色石蕊試液變紅,
故答案為:紅色;
③二氧化硫與品紅化合生成無色物質,能使品紅溶液褪色,故二氧化硫具有漂白性,
故答案為:漂白性;
④SO2中+4價S具有氧化性,硫化氫中-2價S具有還原性,二氧化硫能把硫化氫氧化成單質硫,本身被還原成單質硫,反應方程式為SO2+2H2S=3S↓+2H20,
故答案為:氧化;
⑤二氧化硫具有還原性,能夠與溴水發生氧化還原反應生成氫溴酸和硫酸,溴水褪色,
故答案為:還原;
⑥二氧化硫有毒,不能直接排放到空氣中,二氧化硫酸性氧化物能夠與氫氧化鈉反應生成亞硫酸鈉和水,故答案為:酸.
點評 本題考查了SO2的性質的實驗設計和性質分析判斷,掌握二氧化硫酸性氧化物性質、漂白性、氧化性和還原性等是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:實驗題
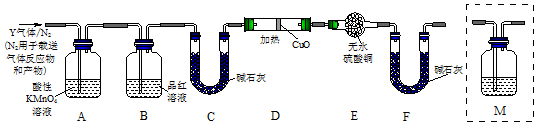
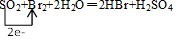 ,
,
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 膠體是一種分散系,屬于混合物 | |
| B. | 膠體的本質特征是能發生丁達爾現象 | |
| C. | 膠體粒子直徑介于1nm-100nm | |
| D. | 利用丁達爾現象是區分膠體和溶液的一種常用方法 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 稱取3.55g硫酸鈉,加入250mL水 | |
| B. | 稱取2.84g硫酸鈉,加水配成250mL溶液 | |
| C. | 稱取6.44g硫酸鈉晶體(Na2SO4•10H2O)配成250mL溶液 | |
| D. | 稱取8.05g硫酸鈉晶體(Na2SO4•10H2O)配成250mL溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若Ⅰ達平衡時,A、B、C各增加1mol,則C轉化率將一定增大 | |
| B. | 若向Ⅰ平衡體系中在加入1molA和3molB,C的體積分數若大于x,可斷定n>3 | |
| C. | 若Ⅱ體系起始物質的量滿足9a+c=3b,則可判斷n=3 | |
| D. | 若n=2,則Ⅱ體系起始物質的量應滿足2a+1<b<3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 11:2 | B. | 9:1 | C. | 9:4 | D. | 5:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 100ml0.1mol•L-1Na2SO4溶液中,微粒總數是0.03NA | |
| B. | 標準狀況下,分子數為NA的N2、C2H4混合氣體的質量無法確定 | |
| C. | 常溫常壓下,32g O2-中所含電子的數目為17NA | |
| D. | 標準狀況下,11.2L酒精含有的分子數為0.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com