
| A. | 都正確 | B. | ②③④⑤ | C. | ②③⑤ | D. | ②④⑤ |
分析 ①能和水反應只生成堿的氧化物是堿性氧化物,發生的反應為復分解反應;
②Na2CO3溶液和NaHCO3溶液與Ca(OH)2溶液反應生成碳酸鈣沉淀;
③鈉在常溫下易被氧化,加熱杯氧化生成過氧化鈉;
④Na2O2能與二氧化碳反應生成碳酸鈉和氧氣,而Na2O與二氧化碳反應生成碳酸鈉;
⑤碳酸鈉和碳酸氫鈉都是強堿弱酸鹽,碳酸根離子、碳酸氫根離子水解溶液顯堿性;
解答 解:①Na2O和水反應只生成堿,是堿性氧化物,Na2O2和水反應生成氫氧化鈉和氧氣,發生氧化還原反應,不是堿性氧化物,故①錯誤;
②Na2CO3溶液和NaHCO3溶液都能跟Ca(OH)2溶液反應得到白色沉淀,Ca2++CO32-=CaCO3↓,Ca2++OH-+HCO3-=CaCO3↓+H2O,②正確;
③鈉在常溫下易被氧化生成白色固體氧化鈉,加熱反應生成淡黃色固體過氧化鈉,故③錯誤;
④Na2O2能與二氧化碳反應生成碳酸鈉和氧氣,而Na2O與二氧化碳反應生成碳酸鈉,所以Na2O2可作供氧劑,而Na2O不行,故④正確;
⑤碳酸為弱酸,Na2CO3溶液和NaHCO3溶液都是強堿弱酸鹽溶液,碳酸氫鈉溶液中碳酸氫根離子水解程度大于電離程度,碳酸根離子和碳酸氫根離子水解溶液都呈堿性,故⑤正確;
故選D.
點評 本題主要考查了物質的性質與用途,主要是那及其化合物性質的應用,難度不大,根據所學知識即可完成.


 百年學典課時學練測系列答案
百年學典課時學練測系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 ;元素Z的離子結構示意圖為
;元素Z的離子結構示意圖為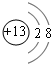 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 相同物質的量的氣體,其氣體摩爾體積也相同 | |
| B. | 氣體摩爾體積是指1mol任何氣體所占的體積為22.4L | |
| C. | 標準狀況下的氣體摩爾體積約為22.4L/mol | |
| D. | 一定物質的量的氣體所占的體積就是氣體摩爾體積 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe( N03)3溶液中加入過量HI溶液:2Fe3++2I-═2Fe2++I2 | |
| B. | 濃燒堿溶液中加入鋁片:2A1+20H-═2AlO2-+H2 | |
| C. | H2SO4與Ba(OH)2溶液反應:Ba2+OH-+H++SO42-═BaSO4+H2O | |
| D. | 將新制氫氧化銅懸濁液加入氨水中:Cu(OH)2+4NH3═[Cu(NH3)4]2++2OH - |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
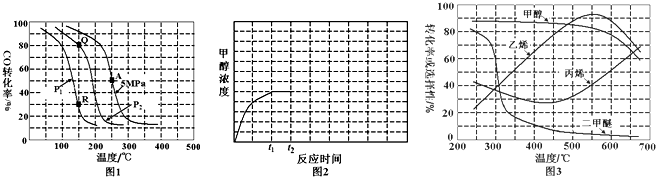
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 綠色更淺 | B. | 綠色更深 | C. | 變黃 | D. | 無變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 文獻名稱 | 有關Fe(OH)2的描述 |
| 《大學普通化學(下冊)》 | 白色沉淀,易被氧化成微綠色Fe3(OH)8 |
| 《化學教育》 | 白色沉淀,在冷水中易形成綠色的水合物Fe(OH)2•nH2O,熱水中不易形成水合物 |
| 實驗序號 | 實驗步驟 | 實驗現象 |
| 一 | ①在試管中加入20mL蒸餾水,加熱煮沸,滴苯液封 ②保持較高溫度,使用長滴管伸入液面下依次擠入一滴飽和FeSO4溶液、一滴NaOH溶液 | 出現白色絮狀沉淀,并能保持一段時間 |
| 二 | ①在試管中加入20mL蒸餾水 ②加入一滴飽和FeSO4溶液、一滴NaOH溶液 | 出現白色沉淀,迅速轉變為灰綠色,最后變為紅褐色 |
| 三 | ①在試管中加入20mL蒸餾水,加熱煮沸,滴苯液封 ②恢復室溫后,使用長滴管伸入液面下依次擠入一滴飽和FeSO4溶液、一滴NaOH溶液 | 出現白色沉淀,迅速轉變為綠色沉淀 |
| 實驗步驟 | 實驗現象與結論 |
| ①在試管中加入20mL蒸餾水,加熱煮沸,滴苯液封 ②迅速用長滴管伸入液面下依次擠入一滴飽和FeSO4 溶液、一滴NaOH溶液 ③將O2緩緩通入白色沉淀中. | 若沉淀中出現綠色的跡象,則假設二成立; 若沉淀中沒有出現任何綠色的跡象,則假設二不成立. |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com