
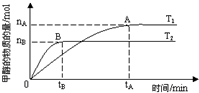
 科學家利用太陽能分解水生成的氫氣在催化劑作用下與二氧化碳反應生成甲醇,并開發出直接以甲醇為燃料的燃料電池.已知H2(g)、CO(g)和CH3OH(l)的燃燒熱△H分別為-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.請回答下列問題:
科學家利用太陽能分解水生成的氫氣在催化劑作用下與二氧化碳反應生成甲醇,并開發出直接以甲醇為燃料的燃料電池.已知H2(g)、CO(g)和CH3OH(l)的燃燒熱△H分別為-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.請回答下列問題:| 1 |
| 2 |
| 1 |
| 2 |
| 4-2a |
| 4 |
| 4-2a |
| 4 |


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
| A、NaClO、NaClO2、KClO3、NaClO4中Cl的化合價依次升高 |
| B、C與CuO高溫共熱,C的氧化產物只能是CO2 |
| C、H2SO4由分子構成,溶于水離解成H+和SO42- |
| D、Al與Fe2O3高溫反應生成Al2O3與Fe,屬于置換反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
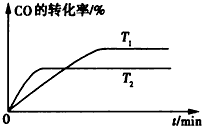
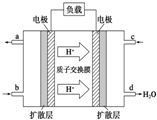
查看答案和解析>>
科目:高中化學 來源: 題型:

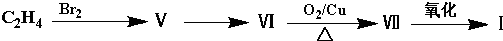
查看答案和解析>>
科目:高中化學 來源: 題型:
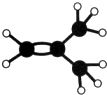 如圖是某烴A分子的球棍模型.回答下列問題:
如圖是某烴A分子的球棍模型.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com