
| 化學反應 | 催化劑 | Ea/KJ•mol-1 | k(催)/k(無) | |
| 無催化劑 | 有催化劑 | |||
| C12H22O11(蔗糖)+H2O═ C6H12O6 (葡萄糖)+C6H12O6(果糖) | 蔗糖酶 | 107 | 36 | 9.2×1011(310K) |
| 2HI═H2+I2 | 金 | 184 | 105 | 1.6×108(503K) |
| CH3CHO═CH4+CO | 碘 | 210 | 136 | 7.5×104(793K) |
| 2H2O2═2H2O+O2 | 過氧化氫酶 | 75 | 25 | 5.8×108(298K) |
科目:高中化學 來源: 題型:解答題

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 開始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | -74.8kJ.mol-1 | B. | +74.8kJ.mol-1 | C. | -149.6kJ.mol-1 | D. | +149.6kJ.mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
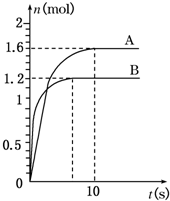
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應③中Br2 是氧化劑,溴元素被氧化 | |
| B. | 氧化性強弱順序為:MnO4->Cl2>Fe3+>Br2 | |
| C. | 反應①中,被氧化的HCl占參加反應的HCl的5/8 | |
| D. | 溶液中可發生反應:2Fe3++2Cl-=2Fe2++Cl2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯化銅溶液與鐵粉反應:Cu2++Fe═Fe2++Cu | |
| B. | 碳酸鈣與鹽酸反應:CaCO3+2H+═H2O+CO2↑ | |
| C. | 氫氧化鋇溶液與稀硫酸反應:Ba2++SO${\;}_{4}^{2-}$═BaSO4↓ | |
| D. | 稀硫酸與鐵粉反應:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  比較非金屬性強弱:S>C>Si 比較非金屬性強弱:S>C>Si | B. |  分離CH3COOC2H5和飽和碳酸鈉溶液 分離CH3COOC2H5和飽和碳酸鈉溶液 | ||
| C. |  觀察純堿的焰色反應 觀察純堿的焰色反應 | D. |  比較Na2CO3和NaHCO3的熱穩定性 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com