
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
分析 ①根據v=$\frac{△c}{△t}$計算v(C),再根據速率之比等于化學計量數之比計算v(A);
②計算C的物質的量變化量,根據方程式計算轉化的A的物質的量,根據轉化率定義計算A的轉化率;
③利用速率之比等于化學計量數之比計算v(B);
④濃度變化量之比等于化學計量數之比,據此計算B的濃度變化量,進而計算2S時B的濃度.
解答 解:①2s后測得C的濃度為0.6mol•L-1,則v(C)=$\frac{0.6mol/L}{2s}$=0.3mol/(L.min),速率之比等于化學計量數之比,故v(A)=v(C)=0.3mol/(L.min),故①正確;
②C的物質的量變化為2L×0.6mol•L-1=1.2mol,根據方程式可知轉化的A的物質的量=1.2mol,故A的轉化率=$\frac{1.2mol}{4mol}$×100%=30%,故②錯誤;
③速率之比等于化學計量數之比,故v(B)=$\frac{1}{2}$v(C)=$\frac{1}{2}$×0.3mol/(L.min)=0.15mol/(L.min),故③錯誤;
④濃度變化量之比等于化學計量數之比,故B的濃度變化量=$\frac{1}{2}$×0.6mol•L-1=0.3mol/L,故2S時B的濃度為$\frac{2mol}{2L}$-0.3mol/L=0.7mol/L,故④正確,
故選B.
點評 本題考查化學平衡與化學反應速率的有關計算,難度不大,側重對基礎知識的鞏固,注意反應速率通常利用定義法與速率規律計算.


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,鈉露置在空氣中易被氧氣氧化為過氧化鈉,因此應保存在煤油里 | |
| B. | 鈉是強還原劑,它能從鹽溶液中置換出金屬活動順序表中排在鈉后面的金屬 | |
| C. | 鈉蒸氣充入燈泡中制成鈉燈,常用于公路照明 | |
| D. | 金屬鈉著火時,能用水來滅火 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ③ | B. | ①③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
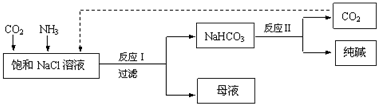
| A. | 反應Ⅰ原理為CO2+NH3+NaCl+H2O→NaHCO3↓+NH4Cl | |
| B. | 向飽和NaCl溶液中先通入足量的CO2,再通入足量的NH3 | |
| C. | 反應Ⅰ生成的沉淀,經過過濾、洗滌、煅燒可得到純堿 | |
| D. | 往母液中通入氨氣,加入細小的食鹽顆粒并降溫,可使氯化銨析出 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:Y>Z>W | |
| B. | ZW2電子式為 | |
| C. | 片狀Y在空氣中點燃時現象不劇烈 | |
| D. | 已知XW2熔點為-107℃、沸點為12.5℃,熔融時不導電,可說明固態XW2為共價化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③⑥⑧ | B. | ②③⑤⑥⑦ | C. | ②③④⑥⑧ | D. | ①③④⑥⑦ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com