
分析 (1)容量瓶瓶頸較細,轉移液體應用玻璃棒引流;定容時,接近刻度線1-2cm應改為膠頭滴管逐滴滴加蒸餾水到凹液面最低處與刻度線相切;
(2)依據配制一定物質的量濃度溶液的一般步驟排序;
(3)根據溶液稀釋前后物質的量不變計算所需濃硫酸的體積;
(4)①依據配制溶液的體積選擇合適的容量瓶;
②依據容量瓶的使用注意事項解答:容量瓶不能稀釋濃溶液、不能用于溶解固體、儲存溶液,不能用于加熱、只能用來配制一定體積準確濃度的溶液;
(5)分析不當操作對溶質的物質的量和溶液的體積的影響,依據C=$\frac{n}{V}$進行誤差分析;
(6)根據各物理量的多少與體積是否有關判斷;
(7)A.碳酸氫鈉與鹽酸反應生成氯化鈉、二氧化碳和水;
B.向氨水中滴加AlCl3溶液反應生成氫氧化鋁和氯化銨.
解答 解:(1)容量瓶瓶頸較細,轉移液體應用玻璃棒引流;定容時,接近刻度線1-2cm應改為膠頭滴管逐滴滴加蒸餾水到凹液面最低處與刻度線相切;
故答案為:引流;膠頭滴管;
(2)配制一定物質的量濃度溶液的操作步驟有檢查容量瓶是否漏水、量取、稀釋、移液、洗滌、定容、搖勻等操作,所以正確的操作步驟為:d a c b e g f;
故答案為:d a c b e g f;
(3)溶液稀釋前后物質的量不變,設需要濃硫酸的體積V,則18mol•L-1×V=1.8mol•L-1×100mL,V=10.0mL,故答案為:10;
(4)①要配制100mL濃度為1.8mol•L-1的H2SO4,應選擇100mL容量瓶,故答案為:B;
②容量瓶不能稀釋濃溶液、不能用于溶解固體、儲存溶液,不能用于加熱、只能用來配制一定體積準確濃度的溶液,故選BCD;
(5)①定容時,俯視刻度線,導致溶液的體積偏小,溶液的濃度偏大;
故答案為:偏大;
②搖勻后液面低于刻度線后又加水,導致溶液的體積偏大,溶液的濃度偏小;
故答案為:偏小;
③配制前,容量瓶壁上有少量水,對溶質的物質的量和溶液的體積都不會產生影響,溶液的濃度不變;
故答案為:無影響;
④未洗滌燒杯和玻璃棒,導致溶質的物質的量偏小,溶液的濃度偏小;
故答案為:偏小;
(6)A.溶液中H2SO4的物質的量n=CV,所以與溶液的體積有關,故A錯誤;
B.溶液具有均一性,濃度與體積無關,故B正確;
C.溶液中H+的數目N=CVNA,所以與溶液的體積有關,故C錯誤;
D.溶液的密度與所量取溶液的體積無關,故D正確;
故選:BD;
(7)A.碳酸氫鈉與鹽酸反應生成氯化鈉、二氧化碳和水,離子方程式:HCO3-+H+=H2O+CO2↑,故答案為:HCO3-+H+=H2O+CO2↑;
B.向氨水中滴加AlCl3溶液反應生成氫氧化鋁和氯化銨,離子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故答案為:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
點評 本題考查了配制一定物質的量濃度溶液、溶液的性質、離子方程式的書寫,熟悉配制原理和操作步驟是解題關鍵,題目難度不大.


科目:高中化學 來源: 題型:解答題
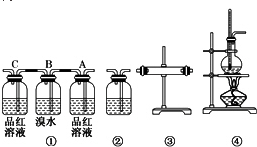
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
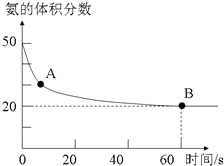 氨氣是一種重要的化工原料,在工農業中都有廣泛的應用.
氨氣是一種重要的化工原料,在工農業中都有廣泛的應用.| 溫度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡氣體總濃度 (10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
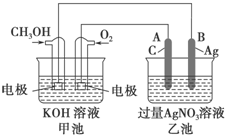 如圖是一個化學過程的示意圖.已知甲池的總反應式為2CH3OH+3O2+4KOH═2K2CO3+6H2O
如圖是一個化學過程的示意圖.已知甲池的總反應式為2CH3OH+3O2+4KOH═2K2CO3+6H2O查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | MnO4-、Fe2+、K+、Cl- | B. | Ca2+、Na+、Cl-、SO42- | ||
| C. | Ca2+、Cl-、NO3-、K+ | D. | Ca2+、H+、OH-、CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
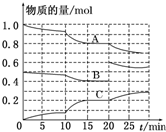 在恒定溫度T℃,2L恒容密閉容器中發生反應aA(g)+bB(g)?cC(g),容器中A、B、C物質的量變化如圖所示,回答下列問題:
在恒定溫度T℃,2L恒容密閉容器中發生反應aA(g)+bB(g)?cC(g),容器中A、B、C物質的量變化如圖所示,回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com