
分析 (1)檢驗二氧化硫用品紅溶液,檢驗二氧化碳用澄清的石灰水,檢驗水蒸氣用無水硫酸銅,因溶液中有水,所以首先檢驗水蒸氣;因為CO2是用澄清石灰水來檢驗的,而SO2也可以使澄清石灰水變渾,二氧化硫能使品紅褪色,二氧化碳不能,所以,檢驗二氧化硫在檢驗二氧化碳之前,再通過澄清石灰水確認CO2存在;
(2)二氧化硫能使品紅褪色;SO2能和溴水發生氧化還原反應;
(3)無水硫酸銅和水作用,白色變藍色;二氧化碳能使石灰水變渾濁.
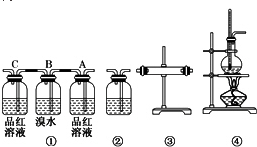
解答 解:(1)乙醇跟濃H2SO4溫度過高反應,CH3CH2OH+4H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$4SO2↑+CO2↑+7H2O+C,選用裝置④;因溶液中有水,所以必須先檢驗水蒸氣,選用裝置③,放入無水硫酸銅,變藍則說明有水生成;因二氧化碳和二氧化硫都能使澄清的石灰水變渾濁,二氧化硫能使品紅褪色,二氧化碳不能,所以用裝置①,A裝置品紅褪色,則說明有SO2氣體產生,B裝置吸收SO2,C裝置品紅不褪色,說明吸收完全;最后用裝置②,通過澄清石灰水變渾濁,確認CO2存在,故答案為:④③①②;
(2)實驗時裝置①的作用是檢驗二氧化硫的存在并除去二氧化硫,A瓶中裝有品紅溶液,二氧化硫能使品紅褪色,所以現象是品紅褪色,說明混合氣中有SO2;B裝置吸收SO2,SO2+Br2+2H2O=H2SO4+2HBr,現象是橙色褪去;C裝置品紅不褪色,說明SO2吸收完全,故答案為:品紅褪色;混合氣中有SO2;橙色褪去;除SO2氣體;SO2被除盡;
(3)裝置③的作用是檢驗水蒸氣,用白色的無水硫酸銅粉末,CuSO4+5H2O═CuSO4•5H2O變藍說明混合氣體中有水蒸氣;裝置②的作用是檢驗二氧化碳,用澄清石灰水,Ca(OH)2+CO2=CaCO3↓+H2O,澄清石灰水變渾濁,確認CO2存在,故答案為:無水CuSO4;水蒸氣;澄清石灰水;CO2.
點評 本題考查了乙醇跟濃硫酸反應生成二氧化硫、二氧化碳、水蒸氣和炭黑產物的檢驗,注意當有多種產物需檢驗時,應考慮先后順序,二氧化碳和二氧化硫都能使澄清的石灰水變渾濁,二氧化硫能使品紅褪色,二氧化碳不能是解答本題的關鍵,題目難度中等.


 新非凡教輔沖刺100分系列答案
新非凡教輔沖刺100分系列答案科目:高中化學 來源: 題型:選擇題
 |  |  |  |
| ① | ② | ③ | ④ |
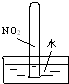
| A. | 實驗①試管最終會充滿水 | |
| B. | 實驗②試管中溶液變為血紅色 | |
| C. | 實驗③試管中出現磚紅色沉淀 | |
| D. | 實驗④CuSO4溶液中會形成一條光亮的通路 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 氨水加水稀釋后,溶液中c (NH3•H2O)/c (NH4+)的值減小,c (H+)增大 | |
| B. | 因為合金在潮濕的空氣中易形成原電池,所以合金耐腐蝕性都較差 | |
| C. | 相同條件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次增強 | |
| D. | 加熱蒸干氯化鋁溶液并灼燒殘留物至質量不變,所得固體為氧化鋁 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=4的NaHSO3溶液中:c(Na+ )>c(HSO3-)>c(H2SO3)>c(SO32-) | |
| B. | 0.01mol•L-1 的NaHCO3 溶液中存在如下平衡:HCO3-?H++CO3 2-,加水稀釋溶液中的HCO3-、H+、CO3 2-濃度減少 | |
| C. | 濃度均為0.1mol•L-1 的CH3COOH、CH3COOK混合溶液中,2c(H+)+c(CH3COOH)=2c(OH-)+c(CH3COO-) | |
| D. | 若Ka(HA)=3.6×10-4,Ka(HB)=1.75×10-5,則等物質的量濃度的NaA、KB溶液相比:c(Na+ )-c(A-)=c(K+ )-c(B-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
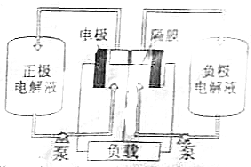 偏釩酸銨(NH4VO3)為白色或微黃色的晶體粉末,微溶于水和氨水,而難溶于冷水,在釩的濕法冶金中占重要地位.
偏釩酸銨(NH4VO3)為白色或微黃色的晶體粉末,微溶于水和氨水,而難溶于冷水,在釩的濕法冶金中占重要地位.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 7種 | B. | 8種 | C. | 9種 | D. | 10種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗操作設計 | 現象記錄 | 結論解釋 | |
| A | 將少量濃硝酸逐滴加入Cu 和稀硫酸的混合物中 | 產生紅棕色氣體 | 硝酸被還原為NO2 |
| B | 用坩堝鉗夾住鋁箔在酒精燈 上加熱 | 鋁箔熔化但并不滴落 | 熔點:Al2 O3>Al |
| C | 向某氯化亞鐵溶液中加入 Na2O2粉末 | 出現紅褐色沉淀 | 加入Na2O2粉末前,原氯化 亞鐵溶液已經變質 |
| D | 向紫色石蕊試液中持續長時 間通人氯氣 | 溶液先變紅,最后變 為無色 | 氯氣有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com