
Ⅰ、實驗室采用MgCl2、 AlCl3的混合溶液與過量氨水反應
AlCl3的混合溶液與過量氨水反應 制備MgAl2O4,主要流程如下:
制備MgAl2O4,主要流程如下:
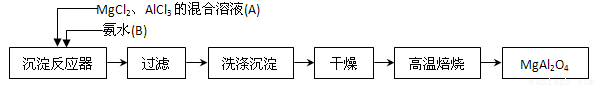
(1)寫出AlCl3與氨水反應的化學反應方程式_________________________。
(2)判斷流程中沉淀是否洗凈所用的試劑是 ,高溫焙燒時,用于盛放固體的儀器名稱是 。
Ⅱ、無水AlCl3(183 ℃升華)遇潮濕空氣即產生大量白霧,實驗室可用下列裝置制備。
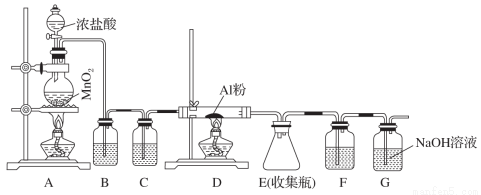
(3)其中裝置A用來制備氯氣,寫出其離子反應方程式:______________________。
(4)裝置B中盛放飽和NaCl溶液,該裝置的主要作用是__________________________。
(5)F中試劑是________。G為尾氣處 理裝置,其中反應的化學方程式:__________________。
理裝置,其中反應的化學方程式:__________________。
(6)制備氯氣的反應會因鹽酸濃度下降而停止。為測定反應殘余液中鹽酸的濃度,探究小組同學提出下列實驗方案:與足量AgNO3溶液反應,稱量生成的AgCl質量。此方案 (填“可行”,“不可行”),理由是_________________________。
 期末金牌卷系列答案
期末金牌卷系列答案 輕松課堂標準練系列答案
輕松課堂標準練系列答案科目:高中化學 來源:2016-2017學年江西省高二12月月考化學卷(解析版) 題型:推斷題
根據下列試題給予的信息,回答問題。
(1)某烴是一種常用的化工原料,可用于制造炸藥、農藥、苯甲酸、染料、合成樹脂及滌綸等。下圖是該烴分子的球棍模型,則該烴的分子式是________,其一氯代物有________種。
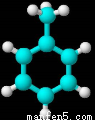
(2)分子中有6個甲基,而一溴代 物只有1種的烷烴,結構簡式是____________。
物只有1種的烷烴,結構簡式是____________。
(3)烯烴與溴化氫、水加成時,產物有主次之分,例如:
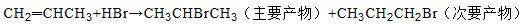
A是一種不對稱烯烴,與HBr加成時,生成的主要產物為B,與水加成時,生成的主要產物為C,且B 中僅含有4個碳原子、1個溴原子、1種氫原子,則B的結構簡式為__________, A與水在催化劑存在下發生加成反應的化學方程式為_________________(只寫主要產物)。
(4) 某氣態烷烴和一氣態烯烴組成的混合氣體在同溫、同壓下對氫氣的相對密度為13,取標準狀況下此混合氣體4.48L,通入足量的溴水,溴水質量增加2.8g,此兩種烴的組成為__________和___________(填分子式)。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省高一12月月考化學試卷(解析版) 題型:選擇題
當光束通過下列分散系時,能觀察到丁達爾效應的是
A.蔗糖溶液 B.鹽酸 C.氯化鈉溶液 D.Fe (OH)3 膠體
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南瀏陽一中等兩校高二12月聯考化學卷(解析版) 題型:選擇題
下列說 法正確的是( )
法正確的是( )
A. 用潤濕的pH試紙測定稀堿溶液的pH,測定值偏小
B. 用堿式滴定管量取22.00mL的KMnO4溶液
C. 在未知液中滴加 BaCl2溶液產生白色沉淀,加稀硝酸,沉淀不溶解,說明該未知液中一定含有SO42-或SO32-
BaCl2溶液產生白色沉淀,加稀硝酸,沉淀不溶解,說明該未知液中一定含有SO42-或SO32-
D. 實驗室制備氫氧化鐵膠體的方法是將氫氧化鈉稀溶液滴入飽和氯化鐵溶液中
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南瀏陽一中等兩校高二12月聯考化學卷(解析版) 題型:選擇題
下列過程或現象與鹽類水解無關的是 ( )
A.純堿溶液去油污  B.鐵在潮濕的環境下生銹
B.鐵在潮濕的環境下生銹
C.加熱氯化鐵溶液顏色變深 D.濃硫化鈉溶液有臭味
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江哈爾濱六中高一上期末化學卷(解析版) 題型:選擇題
下列說法錯誤的是( )
A. Na2SO3與BaCl2溶液作用,有白色沉淀生成,加稀HNO3后沉淀消失
B. 將SO2氣體分別通入Ba(OH)2溶液、FeCl3與BaCl2的混合溶液、HNO3酸化的BaCl2溶液中,均可有白色沉淀生成
C.將SO2氣體通入BaCl2溶液中沒有白色沉淀生成,將SO2氣體通入Ba(NO3)2溶液中有白色沉淀生成
D.將SO2氣體、Cl2一起通入BaCl2溶液中,或將SO2氣體、NO2氣體一起通入BaCl2 溶液中,均有白色沉淀生成
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江哈爾濱六中高一上期末化學卷(解析版) 題型:選擇題
銅粉放入稀硫酸溶液中,加熱后無明顯變化,但加入下列某種鹽后銅粉逐漸溶解,這種鹽是( )
A.NaCl B.KNO3 C.K2SO4 D.Na2CO3
查看答案和解析>>
科目:高中化學 來源:2017屆江西省高三上月考五化學試卷(解析版) 題型:實驗題
氯化亞鐵具有獨有的脫色能力,適用于染料、染料中間體、印染、造紙行業的污水處理。某課題小組設計如下方案制備氯化亞鐵并探究氯化亞鐵(Fe2+)的還原性。
某同學選擇下列裝置用氯化鐵制備少量氯化亞鐵(裝置不可以重復使用)。
查閱資料知:氯化鐵遇水劇烈水解,在加熱條件下氫氣還原氯化鐵生成FeCl2和HCl。
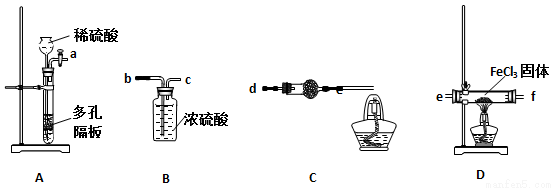
(1)實驗開始前應先檢查裝置的氣密性,請敘述裝置A氣密性檢驗的方法: 。
(2)氣流從左至右,裝置接口連接順序是:
a→ ( )→( )→( )→( )→( )
(3)裝置C中干燥管中所盛試劑為堿石灰,其作用是: 、
用上述方法制得的氯化亞鐵中可能含有氯化鐵,某同學設計了如下實驗,測定樣品中鐵元素的質量分數x.請按要求回答下列問題:
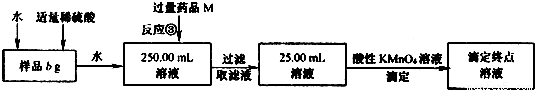
(4)反應③的離子方程式為__ ___.
(5)若3次平行滴定實驗,平均消耗c mol/L KMnO4溶液的體積為d mL,則樣品中鐵元素的質量分數(化簡代數式)x=_____________;若樣品溶解仍使用鹽酸而不改用稀硫酸,則所得樣品中鐵元素的質量分數將(填“偏大”、“偏小”或“無影響”)____ _________.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com