
已知: ①2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol;
②Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=-226 kJ/mol
O2(g) ΔH=-226 kJ/mol
根據以上熱化學方程式判斷,下列說法正確的是( )
A.CO的燃燒熱為 283 kJ
B.反應①正反應活化能與逆反應活化能之差為+566 kJ/mol
C.反應 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D. CO(g)與 Na2O2(s)反應放出 509 kJ 熱量時,電子轉移數為 6.02×1023
科目:高中化學 來源:2017屆河北省高三上期中化學試卷(解析版) 題型:選擇題
下列表示化學反應的離子方程式,其中正確的是:
A.NH4HSO3溶液與足量NaOH溶液共熱:NH4++HSO3-+2OH-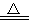 NH3↑+SO32-+2H2O
NH3↑+SO32-+2H2O
B.向氯化鋁溶液中加入過量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
C.大理石溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O
D.硫酸亞鐵溶液中加入用硫酸酸化的過氧化氫溶液Fe2++2H++H2O2═Fe3++2H2O
查看答案和解析>>
科目:高中化學 來源:2016-2017學年云南省高二上期中化學試卷(解析版) 題型:選擇題
下列關于“中和反應反應熱的測定”實驗描述,正確的是
A.實驗過程中,用環形銅棒攪拌,使溶液充分混合
B.為了操作方便,可將0.11gNaOH固體迅速投入50mL0.50mol/L的鹽酸中進行反應
C.用量筒量取50.0mL鹽酸時,俯視刻度導導致所取鹽酸體積偏大
D.為了反應充分進行,使用50mL0.50mol/L的鹽酸和50mL0.55mol/L的NaOH溶液反應
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高二上半期考試化學卷(解析版) 題型:選擇題
下列關于晶體的敘述中,不正確的是
A、金剛石網狀結構中,由共價鍵形成的碳原子環其中最小環有6個碳原子
B、在氯化鈉的晶體中,每個Na+或Cl-的周圍都緊鄰6個Cl-或Na+
C、在氯化銫晶體中,每個Cs+周圍都緊鄰8個Cl—,每個Cl—周圍也緊鄰8個Cs+
D、在干冰的晶體中,每個CO2分子周圍都緊鄰4個CO2分子
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高二上11月考試化學卷(解析版) 題型:選擇題
已知NaHSO3溶液顯酸性,溶液中存在以下平衡:
HSO3-+H2O H2SO3+OH- ①
H2SO3+OH- ①
HSO3- H++SO32- ②
H++SO32- ②
向 0.1 mol·L-1的NaHSO3溶液中分別加入以下物質,下列有關說法正確的是( )
A.加入少量金屬 Na,平衡①左移,平衡②右移,溶液中 c(HSO3-)增大
B.加入少量NaOH溶液,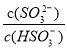 、
、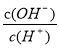 的值均增大
的值均增大
C.加入少量Na2SO3 固體,則 c(H+)+c(Na+)=c(HSO3-)+c(OH-)+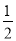 c(SO32-)
c(SO32-)
D.加入氨水至中性,則 2c(Na+)=c(SO32-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化學 來源:2017屆重慶八中高三上學期定時訓練14化學試卷(解析版) 題型:選擇題
金屬(M)-空氣電池(如圖)具有原料易得、能量密度高等優點,有望成為新能源汽車和移動設備的電源。該類電池放電的總反應方程式為:4M+nO2+2nH2O=4M(OH)n。己知:電池的“理論比能量”指單位質量的電極材料理論上能釋放出的最大電能。下列說法不正確的是( )

A.采用多孔電極的目的是提高電極與電解質溶液的接觸面積,并有利于氧氣擴散至電極表面
B.比較Mg、Al、Zn三種金屬-空氣電池,Al-空氣電池理論比能量最高
C. M-空氣電池放電過程的正極反應式:4Mn++nO2+2nH2O+4ne-=4M(OH)n
D.在M-空氣電池中,為防止負極區沉積Mg(OH)2,宜采用中性電解質及陽離子交換膜
查看答案和解析>>
科目:高中化學 來源:2017屆云南省高三上第四次月考化學卷(解析版) 題型:填空題
氮是地球上含量豐富的一種元素。氮及其化合物在在工農業生產、生活中有著重要作用。
(1)在固定體積的密閉容器中,進行如下化學反應:N2(g)+3H2(g)  2NH3(g),△H<0,其平衡常數K與溫度t的關系如下表
2NH3(g),△H<0,其平衡常數K與溫度t的關系如下表
T/K | 298 | 398 | 498 |
平衡常數K | 4.1 x 106 | K1 | K2 |
如果合成氨反應的方程式寫為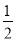 N2(g)+
N2(g)+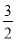 H2(g)
H2(g) NH3(g),其平衡常數為K’,則K’與K之間關系的數學表達式為_________________;根據已知條件可判定K1____________K2(填“>”“<”或“=”)
NH3(g),其平衡常數為K’,則K’與K之間關系的數學表達式為_________________;根據已知條件可判定K1____________K2(填“>”“<”或“=”)
(2)下列能說明合成氨反應已達到平衡狀態的是___________(填序號)。(反應是在固定體積的密閉容器中進行的)
A.容器內溫度保持不變
B.v正(N2)=3v逆(H2)
C.容器內壓強保持不變
D.混合氣體的密度保持不變
E.混合氣體的平均相對分子質量保持不變
(3)合成氨工業中,按照勒夏特列原理,工業生產中應采用的條件為高壓、低溫,但事實上反應中并未采用較低的溫度,原因是_____________________。
(4)硝酸工業在國民經濟、國防工業和航天事業中占有重要地位。隨著化學纖維、近代有機合成、火箭、導彈等工業迅速發展,需要使用大量的硝酸。
①工業生產中用鉑系金屬作為催化劑,用氨氧化法制取硝酸。第一步反應為氨在催化劑作用下與氧氣發生反應生成NO,寫出反應的化學方程:________________________。
②銅既能與稀硝酸反應,也能與濃硝酸反應,當銅與一定濃度硝酸反應時,可將方程式表示為:Cu+HNO3 → Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)。反應中的還原產物是_________________, 0.8mol Cu被硝酸完全溶解后,如果得到NO和NO2物質的量相同,那么標準狀況下的氣體體積為_________________L。(標況下NO和NO2視為氣體)
查看答案和解析>>
科目:高中化學 來源:2017屆山東省東營市高三上期中化學卷(解析版) 題型:選擇題
按下圖所示裝置進行實驗,若x軸表示流入陰極的電子的物質的量,則y軸應表示( )
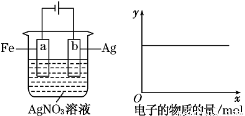
①c(Ag+) ②c(NO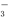 ) ③a棒的質量
) ③a棒的質量
④b棒的質量 ⑤c(H+)
A.①③ B.③④ C.①②④ D.①②⑤
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上學期統練三化學試卷(解析版) 題型:選擇題
下列說法正確的是( )
A.常溫下.NH4Cl溶液加水稀釋,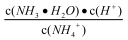 增大
增大
B.0.1mol/LNa2CO3溶液加熱后,溶液的pH減小
C室溫下稀釋0.1mol/LCH3COOH溶液,溶液的導電能力減弱,因此溶液中所有離子濃度均減小
D.向沸水中滴加FeCl3飽和溶液制備Fe(OH)3膠體的原理是加熱促進Fe3+水解
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com