
| 溫度/℃ | 25 | 80 | 230 |
| 平衡常數 /mol-3•L3 | 5×104 | 2 | 1.9×10-5 |
| A. | 上述生成Ni(CO)4(g)的反應為放熱反應 | |
| B. | 在25℃時,反應Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常數為2×10-5 mol3•L-3 | |
| C. | 在80℃時,測得某時刻,Ni(CO)4、CO濃度均為0.5 mol•L-1,則此時v正>v逆 | |
| D. | 在80℃達到平衡時,測得n(CO)=0.3 mol,則Ni(CO)4的平衡濃度為2 mol•L-1 |
分析 A.由表中數據可知,溫度越高,K越小;
B.互為逆反應時,K為倒數關系;
C.在80℃時,測得某時刻,Ni(CO)4、CO濃度均為0.5 mol•L-1,Qc=$\frac{0.5}{0.{5}^{4}}$=8>K=2,平衡逆向移動;
D.80℃達到平衡時,測得n(CO)=0.3 mol,c(CO)=$\frac{0.3mol}{0.3L}$=1mol/L,設Ni(CO)4的平衡濃度為x,則$\frac{x}{{1}^{4}}$=2.
解答 解:A.由表中數據可知,溫度越高,K越小,則生成Ni(CO)4(g)的反應為放熱反應,故A正確;
B.互為逆反應時,K為倒數關系,則25℃時,反應Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常數為$\frac{1}{5×1{0}^{4}}$=2×10-5 mol3•L-3,故B正確;
C.在80℃時,測得某時刻,Ni(CO)4、CO濃度均為0.5 mol•L-1,Qc=$\frac{0.5}{0.{5}^{4}}$=8>K=2,平衡逆向移動,則此時v正<v逆,故C錯誤;
D.80℃達到平衡時,測得n(CO)=0.3 mol,c(CO)=$\frac{0.3mol}{0.3L}$=1mol/L,設Ni(CO)4的平衡濃度為x,則$\frac{x}{{1}^{4}}$=2,解得x=2mol/L,故D正確;
故選C.
點評 本題考查化學平衡的計算,為高頻考點,把握K與溫度的關系、K的計算、平衡移動為解答的關鍵,側重分析與應用能力的考查,注意表格數據的分析與應用,題目難度不大.


 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源: 題型:選擇題
| 編號 | 元素性質或原子結構 |
| X | X的某一種原子沒有中子 |
| Y | 最高正價與最低負價的代數和為0 |
| Z | 最外層電子數是周期數的3倍 |
| M | 含M元素的物質,其焰色反應為黃色 |
| G | G的簡單離子半徑在同周期中最小 |
| A. | X是組成有機物的必需元素 | |
| B. | Y、Z所形成的氫化物分子均含有10個電子 | |
| C. | Z的簡單離子半徑大于G的簡單離子半徑 | |
| D. | G的氧化物不溶于M的最高價氧化物所對應的水化物的水溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO2的電子式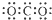 | B. | 質量數為37的氯原子${\;}_{37}^{17}$Cl | ||
| C. | 乙烯的結構簡式C2H4 | D. | Cl-的結構示意圖: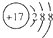 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 兩種物質中所含的氧原子數 | B. | 兩種物質中所含的氧分子數 | ||
| C. | 兩種物質的體積 | D. | 兩種物質的質量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 燃料電池工作時,正極反應為O2+2H2O+4e-═4OH- | |
| B. | 此裝置用于鐵表面鍍銅時,a為鐵b為Cu,工作一段時間要使右池溶液復原可加入適量的CuO | |
| C. | a極是粗銅,b極是純銅時,a極逐漸溶解,b極上有銅析出 | |
| D. | 若a、b兩極均為石墨時,在相同條件下,a極產生的氣體與電池中消耗的H2體積相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
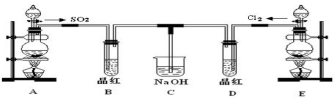
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com