
【題目】某學習小組按如下實驗過程(固定、加熱及盛接儀器略)證明了海帶中存在碘元素:

下列說法不正確的是
A.步驟①需要將干海帶放入坩堝中灼燒
B.步驟②反應的離子方程式為:2I-+2H++H2O2=I2+2H2O
C.步驟③操作后,觀察到試管中溶液變為藍色,可以說明海帶中含有碘元素
D.若步驟③加入的試劑是CCl4,振蕩、靜置后,液體分層,上層紫色,下層無色
 陽光考場單元測試卷系列答案
陽光考場單元測試卷系列答案 名校聯盟沖刺卷系列答案
名校聯盟沖刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化學 來源: 題型:
【題目】丙烯酸酯類物質廣泛用于建筑、包裝材料等,丙烯酸是合成丙烯酸酯的原料之一。丙烯醇可用于生產甘油、塑料等。以丙烯醛為原料生產丙烯醇、丙烯酸的流程如圖所示:

已知:
①2CH2=CH-CHO+NaOH![]() CH2=CHCH2OH+CH2=CHCOONa
CH2=CHCH2OH+CH2=CHCOONa
②2CH2=CHOONa+H2SO4→2CH2=CHCOOH+Na2SO4
③有關物質的相關性質如表:
物質 | 丙烯醛 | 丙烯醇 | 丙烯酸 | 四氯化碳 |
沸點/℃ | 53 | 97 | 141 | 77 |
熔點/℃ | - 87 | - 129 | 13 | -22.8 |
密度/g·mL-3 | 0.84 | 0.85 | 1.02 | 1.58 |
溶解性(常溫) | 易溶于水和有機溶劑 | 溶于水和有機溶劑 | 溶于水和有機溶劑 | 難溶于水 |
(1)操作①需要連續加熱30min,所用裝置如圖所示。儀器L名稱是________。

(2)操作②使用的主要儀器是分液漏斗,在使用之前需進行的操作是 ___。
(3)操作④包括____、過濾、冰水洗滌、低溫吸干。
(4)操作⑤中,加熱蒸餾“下層液體”,分離出四氯化碳;再分離出丙烯醇(如圖),要得到丙烯醇應收集 ____(填溫度)的餾分。圖中有一處明顯錯誤,應改為____。

(5)測定丙烯醇的摩爾質量:準確量取amL丙烯醇于分液漏斗中,燒瓶內盛裝足量鈉粒。實驗前量氣管B中讀數為b mL,當丙烯醇完全反應后,冷卻至室溫、調平B、C液面,量氣管B的讀數為c mL。已知室溫下氣體摩爾體積為VL·mol-1。

調平B、C液面的操作是____;實驗測得丙烯醇的摩爾質量為____g·mol-1(用代數式表示)。如果讀數時C管液面高于B管,測得結果將____(填“偏大”“偏小”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是恒溫條件下某化學反應的反應速率隨反應時間變化的示意圖。下列敘述與示意圖不相符合的是( )

A.反應達到平衡時,正反應速率和逆反應速率相等
B.該反應達到平衡狀態Ⅰ后,增大反應物濃度,平衡發生移動,達到平衡狀態Ⅱ
C.該反應達到平衡狀態Ⅰ后,減小反應物濃度,平衡發生移動,達到平衡狀態Ⅱ
D.同一種反應物在平衡狀態Ⅰ和平衡狀態Ⅱ時濃度不相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氧化還原滴定原理同中和滴定原理相似,為了測定某未知濃度的NaHSO3溶液的濃度,現用0.2000mol/L的酸性KMnO4溶液進行滴定,回答下列問題:
(1) 配平離子方程式:______MnO4-+HSO3-+H+=Mn2++SO42-+H2O。
(2)用KMnO4進行滴定時,KMnO4溶液應裝在_______________中,判斷滴定終點的現象是_______。
(3)下列操作會導致測定結果偏高的是_________。
A. 盛裝未知濃液的錐形瓶用蒸餾水洗過,未用待測液潤洗
B. 未用標準濃度的酸性KMnO4溶液潤洗滴定管
C. 觀察讀數時,滴定前仰視,滴定后俯視
D. 滴定前滴定管尖嘴部分有氣泡,滴定后氣泡消失
(4) 根據下表測定的實驗數據,計算KMnO4溶液體積的平均值為___mL;NaHSO3溶液的物質的量濃度為___mol/L(數據精確到0.1)。
試驗編號 | 待測NaHSO3溶液的體積/ mL | KMnO4溶液體積/ mL |
1 | 20.00 | 15.98 |
2 | 20.00 | 17.00 |
3 | 20.00 | 16.02 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】改革開放四十年來,我國在很多領域取得了舉世矚目的成就,下列工程使用的部分材料如下所示,其中屬于有機高分子的是
A.  港珠澳大橋橋墩——混凝土
港珠澳大橋橋墩——混凝土
B.  “人造太陽”核聚變實驗裝置——鎢合金
“人造太陽”核聚變實驗裝置——鎢合金
C.  高鐵軌道與地基之間填隙減震——聚氨酯
高鐵軌道與地基之間填隙減震——聚氨酯
D.  “玉兔”月球車太陽能電池帆板——硅
“玉兔”月球車太陽能電池帆板——硅
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某科研人員提出HCHO與O2在羥基磷灰石(HAP)表面催化氧化生成CO2、H2O的歷程,該歷程示意圖如下(圖中只畫出了HAP的部分結構)。下列說法不正確的是
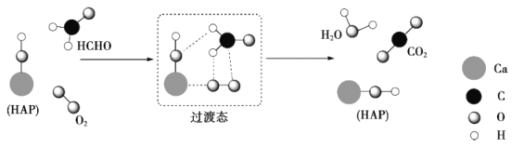
A.HAP能提高HCHO與O2的反應速率
B.根據圖示信息,CO2分子中的氧原子全部來自O2
C.HCHO在反應過程中,有C-H鍵發生斷裂
D.該反應可表示為: HCHO+O2![]() CO2+H2O
CO2+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用0.10 mol/L的NaOH溶液分別滴定體積均為20.00mL、濃度均為0.050 mol/L的鹽酸、磷酸及谷氨酸(H2G),滴定曲線如圖所示:
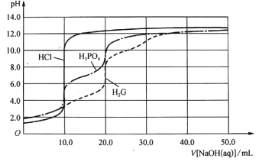
下列說法正確的是
A.滴定鹽酸時,用甲基橙作指示劑比用酚酞更好
B.H3PO4與H2G的第一電離平衡常數K1的數量級不同
C.用酚酞作指示劑滴定磷酸到終點時,溶液中的溶質為Na2HPO4
D.NaH2PO4溶液中:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗設計不合理的是
A. 自制“84”消毒液
自制“84”消毒液
B.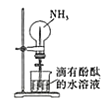 利用噴泉實驗探究NH3的部分性質
利用噴泉實驗探究NH3的部分性質
C. 制備Fe(OH)2白色沉淀
制備Fe(OH)2白色沉淀
D.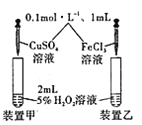 探究不同催化劑對雙氧水分解速率的影響
探究不同催化劑對雙氧水分解速率的影響
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】錳及其化合物在現代工業、農業生產中有著廣泛的應用,同時也是實驗室中常用的重要試劑。
(1)KMnO4是強氧化劑,其溶液中c(H+)=c(OH-),則常溫下0.01molL-1的HMnO4溶液的pH=_____________。
(2)MnS常用于除去污水中的Pb2+等重金屬離子:Pb2+(aq)+ MnS(s)PbS(s)+Mn2+(aq),若經過處理后的水中c(Mn2+)=1 ×10-6 molL-1,則c(Pb2+)=______________[已知Ksp(PbS)=8×10-28、Ksp(MnS)=2×10-13]。
(3)錳是農作物生長的重要微量元素,用硫酸錳溶液拌種可使農作物產量提高10%~15%。某工廠利用回收的廢舊鋅錳干電池生成硫酸錳晶體(MnSO4H2O)的流程如圖所示:
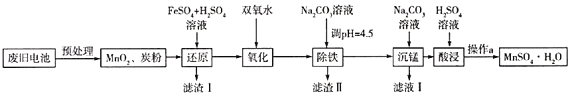
①MnSO4中含有的化學鍵類型有_______________。
②濾渣Ⅱ的主要成分是____________,濾渣Ⅰ是一種黑色單質,“還原”過程中氧化產物是Fe3+,寫出相應反應的離子方程式_________,此反應中MnO2的轉化率與溫度之間的關系如圖所示,則適宜的溫度是______________(填字母)。
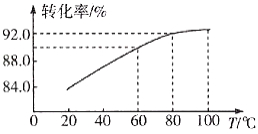
a.40 ℃ b.60 ℃ c.80 ℃ d.100 ℃
③“沉錳”中有無色無味的氣體生成,還有MnCO36Mn(OH)25H2O生成,寫出相應反應的化學方程式_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com