
| A. | CaCO3 | B. | BaCO3 | C. | MgCO3 | D. | SrCO3 |
分析 堿土金屬離子與碳酸根的極化作用,堿土金屬都帶兩個正電荷,如果離子半徑越小對陰離子(碳酸根離子)的極化作用越強,極化作用越強金屬鍵越容易往共價鍵發展,即越不穩定.所以從第2主族由上到下,極化作用越弱,分解溫度越高.
解答 解:堿土金屬離子與碳酸根的極化作用,堿土金屬都帶兩個正電荷,如果離子半徑越小對陰離子(碳酸根離子)的極化作用越強,極化作用越強金屬鍵越容易往共價鍵發展,即越不穩定.所以從第2主族由上到下,極化作用越弱,分解溫度越高;堿土金屬的碳酸鹽熱分解溫度,MgCO3>CaCO3>SrCO3>BaCO3,碳酸鹽中最易分解為氧化物的是MgCO3,
故選C.
點評 本題考查酸鹽的熱分解溫度與晶格能的大小關系,學生只要清楚影響晶格能大小的因素,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,44g CO2中含有2NA個π鍵 | |
| B. | 1mol•L-1NaCl溶液含有NA個Na+ | |
| C. | 0.5mol Cu和足量濃硝酸反應可以生成22.4LNO2 | |
| D. | 過量的液溴與鐵反應,若反應中消耗1mol鐵,則轉移的電子數目為2NA個 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 亞硫酸鈉溶液顯堿性:SO32-+2H2O=H2SO3+2OH- | |
| B. | (NH4)2FeSO4溶液與過量NaOH溶液混合制取氫氧化亞鐵:Fe2++2OH-=Fe(OH)2 | |
| C. | NaAlO2溶液中通入過量CO2制取氫氧化鋁:2AlO2-+CO2+3H2O=2Al(OH)3+CO32- | |
| D. | 鐵紅溶于HI酸溶液:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 體系的壓強不再改變 | |
| B. | 體系的溫度不再改變 | |
| C. | 消耗1molN2的同時,新生成3molH2 | |
| D. | 反應消耗的N2、H2與產生的NH3的速率υ(N2):υ(H2):υ(NH3)═1:3:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氮氣的化學性質不活潑,是因為氮元素不活潑 | |
| B. | 雷雨可以增加土壤中硝酸鹽類氮肥的含量,此過程中的反應都屬于氮的固定 | |
| C. | 氮氣可替代稀有氣體作焊接金屬的保護氣 | |
| D. | NO2溶于水生成硝酸,因此NO2是硝酸的酸酐 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molNa2O2與足量H2O充分反應轉移的電子數為2NA | |
| B. | 200mL,1mol/LFe2(SO4)3溶液中,Fe3+和SO42-離子總數為6.02×1023 | |
| C. | 已知2A(g)+B(g)═2C(g)△H=-akJ/mol,若將2NA個A與NA個B混合充分反應放出akJ的熱量 | |
| D. | 28gSi3N4晶體中含有的硅氮鍵的數目為2.4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
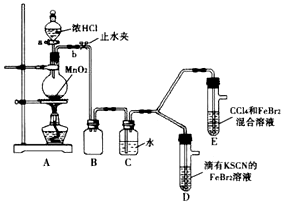
| 實驗操作 | 實驗現象 | 結論 |
| 打開活塞a,向圓底燒瓶中滴入適置濃鹽酸,然后關閉活塞a,點燃酒精燈 | D裝罝中:溶液變紅,E裝置中:水層溶液變黃,振蕩后CCl4層無明顯變化 | Cl2、Br2、Fe2+的氧化性由強到弱的順序為Cl2>Br2>Fe3+ |
| i.(SCN)2性質與鹵素單質類似.氧化性:Cl2>(SCN)2 ii.Cl2和Br2反應生成BrCl,它呈紅色(略帶黃色)沸點約為5℃,與水發生水解反應 iii.AgClO、AgBrO均可溶于水 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
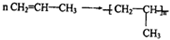
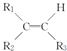 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$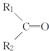 +R3-COOH,
+R3-COOH,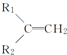 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$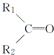 +CO2
+CO2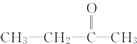 ),則此烯烴的結構簡式是CH2=C(CH3)C2H5.
),則此烯烴的結構簡式是CH2=C(CH3)C2H5.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol H2約含有6.02×1023個氫分子 | |
| B. | 1 mol H2O的質量為18 g | |
| C. | 1 mol O2的體積為22.4 L | |
| D. | 1L 1 mol/L NaCl溶液中含1 molNa+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com