
| 離子半徑 | 電負性 | 第一電離能 | 沸點 |
| O2->Al3+ | C<N | N>O | CH4< NH3 |
分析 (1)根據Fe元素位于周期表第四周期第 VIII族,其基態原子價電子的排布式為3d64S2判斷未成對電子數;根據金剛石是原子晶體,C60是分子晶體,判斷熔點高低;
(2)根據核外電子排布相同的離子,核電荷數越大,離子半徑越小判斷;
根據同一周期元素,電負性隨著原子序數的增大而增大判斷;
根據N基態原子的價電子排布式為2s22p3處于半充滿的穩定結構第一電離能大判斷;
根據NH3和CH4都屬于分子晶體,NH3分子間存在氫鍵,沸點高判斷.
(3)Al能將污水中NO3-轉化為N2,同時鋁的反應產物還能凈化污水,該反應的離子方程式10Al+6NO3-+18H2O=3N2↑+10Al(OH)3+6OH-,其中產生的鋁的化合物能凈水的原理是生成的Al(OH)3膠體具有吸附作用.
(4)根據蓋斯定律①2H2(g)+O2(g)=2H2O(l)△H=-571.66kJ•mol-1
②CH2=CH2(g)+3O2(g)=2CO2(g)+2H2O(l)△H=-1306.42kJ•mol-1
則CO2和H2合成(CH2=CH2)的熱化學方程式為①×3-②得該熱化學方程式,據此計算焓變;
解答 解:(1)Fe元素位于周期表第四周期第VIII族,價電子的排布式為3d64S2,所以其基態原子未成對電子數為4,因為金剛石是原子晶體,C60是分子晶體,故金剛石熔點比C60高,故答案為:四;VIII;4;高;
(2)核外電子排布相同的離子,核電荷數越大,離子半徑越小,所以離子半徑:O2->Al3+;同一周期元素,電負性隨著原子序數的增大而增大,故電負性C<N;因為N基態原子的價電子排布式為2s22p3處于半充滿的穩定結構,O基態原子的價電子排布式為2s22p4,O原子比N原子更容易失去第一個電子,故第一電離能N>O;NH3和CH4都屬于分子晶體,NH3分子間存在氫鍵,故沸點CH4<NH3,故答案為:>;<;>;<;
(3)Al能將污水中NO3-轉化為N2,同時鋁的反應產物還能凈化污水,該反應的離子方程式10Al+6NO3-+18H2O=3N2↑+10Al(OH)3+6OH-,其中產生的鋁的化合物能凈水的原理是生成的Al(OH)3膠體具有吸附作用,
故答案為:10Al+6NO3-+18H2O=3N2↑+10Al(OH)3+6OH-;生成的Al(OH)3膠體具有吸附作用;
(4)①2H2(g)+O2(g)=2H2O(l)△H=-571.66kJ•mol-1
②CH2=CH2(g)+3O2(g)=2CO2(g)+2H2O(l)△H=-1306.42kJ•mol-1
則CO2和H2合成(CH2=CH2)的熱化學方程式為①×3-②得:2CO2(g)+6 H2(g)═CH2=CH2(g)+4H2O(l)△H=(-571.66×3+1306.42)kJ•mol-1=-408.56kJ•mol-1,故答案為:2CO2(g)+6 H2(g)═CH2=CH2(g)+4H2O(l)△H=-408.56kJ•mol-1.
點評 本題考查了元素周期表以及元素周期律的應用,以此為載體,考查了蓋斯定律、熔沸點的比較、電負性、第一電離能以及鋁的凈水等,難度中等.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化學 來源: 題型:選擇題
| A. | NH4Cl→NH3↑+HCl↑ | B. | NH3+CO2+H2O→NH4HCO3 | ||
| C. | 2NaOH+Cl2→NaCl+NaClO+H2O | D. | 2Na2O2+2CO2→2Na2CO3+O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題

| A. | 分子中含有2個手性碳原子 | |
| B. | 能發生氧化、取代、加成反應 | |
| C. | 1 mol該化合物與足量濃溴水反應,最多消耗3 mol Br2 | |
| D. | 1 mol該化合物與足量NaOH溶液反應,最多消耗4 mol NaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 24種 | B. | 16種 | C. | 12種 | D. | 8種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
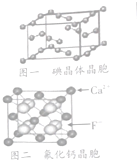 鹵族元素的單質和化合物很多,我們可以利用所學物質結構與性質的相關知識去認識和理解
鹵族元素的單質和化合物很多,我們可以利用所學物質結構與性質的相關知識去認識和理解| 氯 | 氧 | 溴 | 碘 | 鍍 | |
| 第一電離能(kj/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
 )和HIO4,前者為五元酸,后者為一元酸,請比較二者酸性強弱:H5IO6<HIO4(填“>”、“<”或“=”)
)和HIO4,前者為五元酸,后者為一元酸,請比較二者酸性強弱:H5IO6<HIO4(填“>”、“<”或“=”)查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| A | A的一種單質在自然界中硬度最大 |
| B | B元素的第一電離能比同周期相鄰兩個元素都大 |
| C | 同周期中,C元素的最高價氧化物對應的水化物的堿性最強 |
| D | D的基態原子M層電子數是K層的2 倍 |
| E | E與C位于不同周期,E原子核外最外層電子數與C相同,其余各層電子均充滿 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 按系統命名法,化合物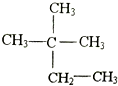 的名稱為2-甲基-2-乙基丙烷 的名稱為2-甲基-2-乙基丙烷 | |
| B. | 分別向皂化反應完成后的溶液、豆漿、牛奶中加入濃食鹽水都有固體析出 | |
| C. | 碳原子數小于5的烷烴共有4種,他們之間互為同系物 | |
| D. | 石油裂解可以得到乙烯,煤干餾得到的煤焦油中可以提取苯,乙烯和苯使溴水褪色的原理相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 元素符號 | X | Y | Z | R | T |
| 原子半徑(nm) | 0.160 | 0.186 | 0.102 | 0.143 | 0.074 |
| 主要化合價 | +2 | +1 | -2,+4,+6 | +3 | -2 |
| A. | 離子的還原性:T2->Z2- | |
| B. | 離子半徑:T2->X2+ | |
| C. | 元素最高價氧化物對應水化物的堿性:Y>R>X | |
| D. | 形成氫化物的沸點:Z>T |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com