

 分子式:C12H10
分子式:C12H10 其苯環上的一氯代物有_5種
其苯環上的一氯代物有_5種 的系統命名是2,6-二甲基辛烷
的系統命名是2,6-二甲基辛烷 1mol該物質消耗5molH2,5molBr21molNa
1mol該物質消耗5molH2,5molBr21molNa分析 (1)熟悉常見原子團的書寫方法以及常見官能團的結構簡式和名稱即可輕松解答;
(2)乙烯是空間平面結構的分子;
(3)根據化學鍵類型及原子間形成共用電子對數目解答;
(4)苯的同系物的通式CnH2n-6(n≥6的整數);
(5)根據結構簡式結合碳原子的成鍵特點書寫分子式;
(6)有機物中的等效氫原子有幾種,其一氯代物就有幾種;
(7)(9)烷烴命名原則:
①長:選最長碳鏈為主鏈;
②多:遇等長碳鏈時,支鏈最多為主鏈;
③近:離支鏈最近一端編號;
④小:支鏈編號之和最小.看下面結構簡式,從右端或左端看,均符合“近-----離支鏈最近一端編號”的原則;
⑤簡:兩取代基距離主鏈兩端等距離時,從簡單取代基開始編號.如取代基不同,就把簡單的寫在前面,復雜的寫在后面;據此回答;
(8)根據炔烴的命名原則寫出4,4,5-三甲基-2-己炔的結構簡式;
(10)有機物中的雙鍵可以被氫氣以及溴單質加成,其中的羥基可以和金屬鈉之間反應;
(11)苯不溶于水,密度比水小,可以萃取溴水中的溴,溶液分層,有機層在上方;碘化鉀與溴水發生氧化還原反應生成單質碘;硝酸銀與溴水反應生成淺黃色沉淀;己烯與溴發生加成反應,溴水顏色褪去;四氯化碳不溶于水,但密度比水大,可以萃取溴水中的溴,溶液分層,有機層在下層,可用濃溴水鑒別有機物;
(12)分子式為C5H8的炔烴有官能團位置異構、碳鏈異構.
解答 解:(1)-CH2CH3為乙基,-Br為鹵素中的溴原子;三鍵-C≡C-,故答案為:乙基;溴原子;-C≡C-;
(2)乙烯是空間平面結構的分子,故答案為:平面結構;
(3)乙炔中碳原子最外層有4個電子,要達到穩定結構要形成四對共用電子對,而1個氫原子只能與1個碳原子形成形成1對公用電子對,所以碳原子和碳原子間只能形成3對公用電子對,所以乙炔的電子式為 ,故答案為:
,故答案為: ;
;
(4)苯的同系物的通式CnH2n-6(n≥6的整數),故答案為:CnH2n-6(n≥6的整數);
(5) 分子式是C12H10,故答案為:C12H10;
分子式是C12H10,故答案為:C12H10;
(6) 中存在5中等效氫原子,所以 其苯環上的一氯代物有5種,故答案為:5;
中存在5中等效氫原子,所以 其苯環上的一氯代物有5種,故答案為:5;
(7)2,5-二甲基-4-乙基庚烷,最長的主鏈含有7個C原子,甲基處于2、5號碳原子上,乙基處于4號碳原子上,其結構簡式為:CH3)2CHCH2CH(C2H5)CH(CH3)CH2CH3,故答案為:(CH3)2CHCH2CH(C2H5)CH(CH3)CH2CH3.
(8)4,4,5-三甲基-2-己炔,該有機物主鏈為己炔,碳碳三鍵在2號C,在4、4、5號C原則各含有1個甲基,該有機物的結構簡式為:CH3C≡C-C(CH3)2CH(CH3)2,故答案為:CH3C≡C-C(CH3)2CH(CH3)2;
(9) 的主鏈碳原子數數目是8個,為辛烷,在2、6號碳原子上有甲基,名稱為:2,6-二甲基辛烷,故答案為:2,6-二甲基辛烷;
的主鏈碳原子數數目是8個,為辛烷,在2、6號碳原子上有甲基,名稱為:2,6-二甲基辛烷,故答案為:2,6-二甲基辛烷;
(10)有機物中的雙鍵5mol可以被氫氣以及溴單質加成,分別消耗氫氣和溴單質是5mol,其中的羥基1mol可以和1mol金屬鈉之間反應,故答案為:5;5;1;
(11)苯不溶于水,密度比水小,可以萃取溴水中的溴,溶液分層,層由無色變為橙紅色,下層由橙色變為無色,碘化鉀與溴水發生氧化還原反應生成單質碘,溶液顏色由無色變為黃色,硝酸銀與溴水反應生成淺黃色沉淀,己烯與溴發生加成反應,溶液分層,上,下兩層均變為無色,四氯化碳不溶于水,但密度比水大,可以萃取溴水中的溴,溶液分層,上層由橙色變為無色,下層由無色變為橙紅色,所以可以用溴水來進行鑒別,故答案為:濃溴水;
(12)分子式為C5H8的炔烴,可能的結構簡式有:CH≡CCH2CH2CH3、CH3C≡CCH2CH3、CH≡CCH(CH3)2,
故答案為:CH≡CCH2CH2CH3、CH3C≡CCH2CH3、CH≡CCH(CH3)2.
點評 本題涉及有機物的同分異構體的書寫、有機物的命名、有機物的空間結構、有機物的鑒別等方面的知識,屬于綜合知識的考查,注意知識的歸納和梳理是關鍵,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 1.0 L 1.0 mo1•L-1的NaAlO2水溶液中含有的氧原子數為2NA | |
| B. | 56 g鐵片投入足量濃H2SO4中生成NA個SO2分子 | |
| C. | 標準狀況下,22.4 L氨水含有NA個NH3分子 | |
| D. | 常溫常壓下,14 g由N2與CO組成的混合氣體含有的原子數目為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaOH固體置于大小相同的濾紙上稱量 | |
| B. | 蒸餾操作時,冷凝水的方向須與氣體的流向相同 | |
| C. | 配制稀硫酸時,將濃硫酸溶解后直接轉移入容量瓶 | |
| D. | 分液時,先要打開分液漏斗上口活塞,再打開旋塞 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 該混合液中一定含有:K+、NH4+、CO32-、SO42-,可能含Cl- | |
| B. | 該混合液中-定含有:NH4+、CO32-、SO42-,可能含K+、Cl- | |
| C. | 該混合液中一定含有:NH4+、CO32-、SO42-、Cl-,可能含K+ | |
| D. | 該混合液中:c(K+)≥0.1mol/L c(CO32-)=0.1mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
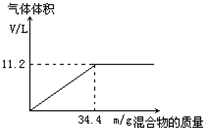 在100mL NaOH溶液中加入NH4NO3和(NH4)2SO4的固體混合物,加熱充分反應.如圖表示加入的混合物的質量與產生的氣體體積(標準狀況)的關系.
在100mL NaOH溶液中加入NH4NO3和(NH4)2SO4的固體混合物,加熱充分反應.如圖表示加入的混合物的質量與產生的氣體體積(標準狀況)的關系.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 相關信息 | |
| X | 單質為雙原子分子.若低溫蒸發液態空氣,因其沸點較低可先獲得X的單質 |
| Y | 含Y元素的物質焰色反應為黃色 |
| Z | 同周期元素中原子半徑最小 |
| R | R元素原子的最外層電子數是K層電子數的3倍 |
 ;
; ,寫出乙溶液在空氣中變質生成Y2R2的化學方程式4Na2S+O2+2H2O═4NaOH+2Na2S2.
,寫出乙溶液在空氣中變質生成Y2R2的化學方程式4Na2S+O2+2H2O═4NaOH+2Na2S2.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 容器編號 | 起始時各物質物質的量/mol | 達平衡時體系 能量的變化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出熱量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出熱量:Q |
| A. | 容器②中達平衡時放出的熱量Q=23.15 kJ | |
| B. | 平衡時,兩個容器中NH3的體積分數均為$\frac{1}{7}$ | |
| C. | 容器①、②中反應的平衡常數相等 | |
| D. | 若容器①體積為0.5L,則平衡時放出的熱量<23.15kJ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com