
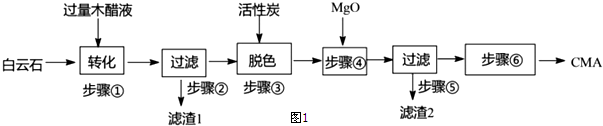

分析 根據流程圖可知,白云石(主要成分MgCO3•CaCO3,含SiO2等雜質)與木醋液(主要成分乙酸)反應生成醋酸鈣和醋酸鎂,過濾得濾渣1為二氧化硅,濾液中主要溶質是醋酸鈣和醋酸鎂,加入活性碳脫色,再加入氧化鎂,調節溶液中n(Ca):n(Mg)的值,過濾,除去混合液中固體雜質,得醋酸鈣和醋酸鎂溶液,將濾液蒸發結晶、過濾、洗滌及干燥得CMA,
(1)步驟①MgCO3•CaCO3與CH3COOH的反應生成醋酸鈣和醋酸鎂;
(2)己知lmol NaOH與二氧化硅發生反應時放出熱量為QkJ,則反應的熱化學方程式為Si02(s)+2NaOH(aq)=Na2SiO3(aq)+H2O(l),△H=-2QkJ/mol,
步驟②所得濾液常呈褐色,顏色除與木醋液中含有少量的有色的焦油有關外,產生顏色的另一主要原因是實驗過程中苯酚被空氣中氧氣氧化最終產生褐色物質;
(3)根據如圖2所示鈣、鎂的物質的量之比與出水率(與融雪效果成正比)關系,可知,當n(Ca):n(Mg)約為3:7時,出水率最高;
(4)根據上面的分析可知,步驟⑥包含的操作有 蒸發結晶、過濾、洗滌及干燥;
(5)取akg含MgC03•CaC03質量分數為b%的白云石,經過上述流程制備CMA.已知MgC03'•CaC03的損失率為c%,則可得n(Ca(CH3COO)2)=$\frac{a×b%(1-c%)}{184}×1{0}^{3}$mol,
n(Mg(CH3COO)2)=$\frac{a×b%(1-c%)}{184}×1{0}^{3}$×$\frac{7}{3}$mol,
步驟④之后到產品CMA的損失率為d%,以此計算產量.
解答 解:根據流程圖可知,白云石(主要成分MgCO3•CaCO3,含SiO2等雜質)與木醋液(主要成分乙酸)反應生成醋酸鈣和醋酸鎂,過濾得濾渣1為二氧化硅,濾液中主要溶質是醋酸鈣和醋酸鎂,加入活性碳脫色,再加入氧化鎂,調節溶液中n(Ca):n(Mg)的值,過濾,除去混合液中固體雜質,得醋酸鈣和醋酸鎂溶液,將濾液蒸發結晶、過濾、洗滌及干燥得CMA,
(1)步驟①發生的反應離子方程式為 MgCO3•CaCO3+4CH3COOH=Ca2++Mg2++4CH3COO-+2CO2↑+2H2O,
故答案為:MgCO3•CaCO3+4CH3COOH=Ca2++Mg2++4CH3COO-+2CO2↑+2H2O;
(2)己知lmol NaOH與二氧化硅發生反應時放出熱量為QkJ,則反應的熱化學方程式為Si02(s)+2NaOH(aq)=Na2SiO3(aq)+H2O(l),△H=-2QkJ/mol,
步驟②所得濾液常呈褐色,顏色除與木醋液中含有少量的有色的焦油有關外,產生顏色的另一主要原因是實驗過程中苯酚被空氣中氧氣氧化最終產生褐色物質,
故答案為:Si02(s)+2NaOH(aq)=Na2SiO3(aq)+H2O(l),△H=-2QkJ/mol;實驗過程中苯酚被空氣中氧氣氧化最終產生褐色物質;
(3)根據如圖2所示鈣、鎂的物質的量之比與出水率(與融雪效果成正比)關系,可知,當n(Ca):n(Mg)約為3:7時,出水率最高,所以步驟④的目的除調節n(Ca):n(Mg)約為3:7,步驟④中加入氧化鎂的目的是調節鈣、鎂離子的物質的量之比,除去過量的乙酸,
故答案為:3:7;除去過量的乙酸;
(4)根據上面的分析可知,步驟⑥包含的操作有 蒸發結晶、過濾、洗滌及干燥,
故答案為:蒸發結晶;
(5)取akg含MgC03•CaC03質量分數為b%的白云石,經過上述流程制備CMA.已知MgC03'•CaC03的損失率為c%,則可得n(Ca(CH3COO)2)=$\frac{a×b%(1-c%)}{184}×1{0}^{3}$mol,
n(Mg(CH3COO)2)=$\frac{a×b%(1-c%)}{184}×1{0}^{3}$×$\frac{7}{3}$mol,
步驟④之后到產品CMA的損失率為d%,
則可知所得產品質量約為 ($\frac{a×b%(1-c%)×158}{184}+\frac{a×b%×(1-c%)×\frac{7}{3}×142}{184}$)×(1-d%),
故答案為:($\frac{a×b%(1-c%)×158}{184}+\frac{a×b%×(1-c%)×\frac{7}{3}×142}{184}$)×(1-d%).
點評 本題考查CMA的工藝流程,側重考查學生閱讀題目獲取信息能力、對工藝流程的理解、物質分離提純與條件控制等,綜合性較強,題目難度中等,需要學生具備扎實的基礎知識與綜合運用知識、信息進行解決問題的能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
 的系統名稱是3,4-二甲基-3-乙基己烷.
的系統名稱是3,4-二甲基-3-乙基己烷. .
.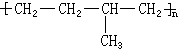 形成該高聚物的單體的結構簡式分別為
形成該高聚物的單體的結構簡式分別為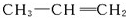 、
、 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
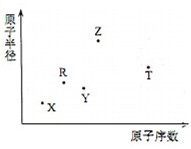 短周期主族元素X、Y、Z、R、T的原子半徑與原子序數關系如圖所示.R原子最外層電子數是電子層數的2倍.Y與Z能形成Z2Y、Z2Y2型離子化合物.Z與T形成的化合物Z2T能破壞水的電離平衡.下列推斷正確的是( )
短周期主族元素X、Y、Z、R、T的原子半徑與原子序數關系如圖所示.R原子最外層電子數是電子層數的2倍.Y與Z能形成Z2Y、Z2Y2型離子化合物.Z與T形成的化合物Z2T能破壞水的電離平衡.下列推斷正確的是( )| A. | 原子半徑和離子半徑均滿足:Y<Z | |
| B. | 氫化物的沸點不一定是:Y>R | |
| C. | 最高價氧化物對應水化物的酸性:T<R | |
| D. | 由X、R、Y、Z四種元素組成的化合物水溶液一定顯堿性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
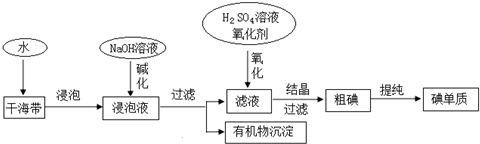
| A. | 因海水中蘊藏著極其豐富的碘元素,所以工業上也可以直接用海水來提取碘元素 | |
| B. | 堿化操作時,加入NaOH溶液的原因是在堿性溶液中,可溶性有機質可形成沉淀 | |
| C. | 在實驗室進行氧化操作時,加入的氧化劑可以是新制氯水、雙氧水等 | |
| D. | 在實驗室進行過濾操作時,需要用到玻璃儀器有玻璃棒、燒杯、漏斗 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 預期現象及結論 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
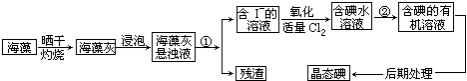
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 用50mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液在如圖所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量.回答下列問題:
用50mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液在如圖所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Si、P、S、Cl元素的單質與氫氣化合越來越容易 | |
| B. | 非金屬元素的非金屬性越強,其氧化物對應水化物的酸性也一定越強 | |
| C. | 元素原子最外層電子數越多,元素金屬性越強 | |
| D. | F-、O2-、Mg2+、Na+離子半徑逐漸減小 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com