
(13分)
(1)某科研小組研究在其他條件不變的情況下,改變起始氫氣物質的量[用n(H2)表示]對N2(g)+3H2(g) 2NH3(g)反應的影響,實驗結果可表示成如下圖所示的規律(圖中T表示溫度,n表示物質的量):
2NH3(g)反應的影響,實驗結果可表示成如下圖所示的規律(圖中T表示溫度,n表示物質的量):
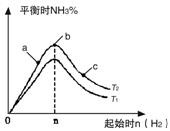
①比較在a、b、c三點所處的平衡狀態中,反應物N2的轉化率最高的是__________。
②若容器容積為1L,n=3mol,反應達到平衡時H2的轉化率為60%,則在起始時體系中加入N2的物質的量為__________mol,此條件下(T2),反應的平衡常數K=__________。
③圖像中T2和T1的關系是__________。(填“高于”、“低于”、“等于”、“無法確定”)。
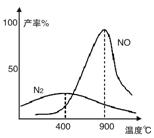
(2)氨氣和氧氣從145℃就開始反應,在不同溫度和催化劑條件下生成不同產物(如圖):
4NH3+5O2 4NO+6H2O
4NO+6H2O
4NH3+3O2 2N2+6H2O
2N2+6H2O
溫度較低時以生成__________為主,溫度高于900℃時,NO產率下降的原因是__________。
(3)現以H2與O2、熔融鹽Na2CO3組成的燃料電池(如圖所示,其中Y為CO2)裝置進行電解。
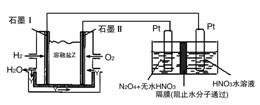
寫出石墨Ⅰ電極上發生反應的電極反應式:__________。
在電解池中生成N2O5的電極反應式為:__________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
(1)某科研小組研究在其他條件不變的情況下,改變起始氫氣物質的量[用n(H2)表示]對N2(g)+3H2(g)![]() 2NH3(g)反應的影響,實驗結果可表示成如下圖所示的規律(圖中T表示溫度,n表示物質的量):
2NH3(g)反應的影響,實驗結果可表示成如下圖所示的規律(圖中T表示溫度,n表示物質的量):
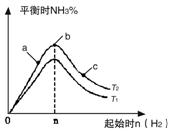
①比較在a、b、c三點所處的平衡狀態中,反應物N2的轉化率最高的是__________。
②若容器容積為1L,n=3mol,反應達到平衡時H2的轉化率為60%,則在起始時體系中加入N2的物質的量為__________mol,此條件下(T2),反應的平衡常數K=__________。
③圖像中T2和T1的關系是__________。(填“高于”、“低于”、“等于”、“無法確定”)。
(2)氨氣和氧氣從145℃就開始反應,在不同溫度和催化劑條件下生成不同產物(如圖):
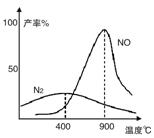
4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
4NH3+3O2![]() 2N2+6H2O
2N2+6H2O
溫度較低時以生成__________為主,溫度高于900℃時,NO產率下降的原因是__________。
(3)現以H2與O2、熔融鹽Na2CO3組成的燃料電池(如圖所示,其中Y為CO2)裝置進行電解。
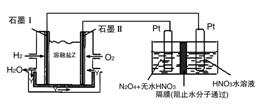
寫出石墨Ⅰ電極上發生反應的電極反應式:__________。
在電解池中生成N2O5的電極反應式為:__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
(13分)
(1)某科研小組研究在其他條件不變的情況下,改變起始氫氣物質的量[用n(H2)表示]對N2(g)+3H2(g) 2NH3(g)反應的影響,實驗結果可表示成如下圖所示的規律(圖中T表示溫度,n表示物質的量):
①比較在a、b、c三點所處的平衡狀態中,反應物N2的轉化率最高的是__________。
②若容器容積為1L,n=3mol,反應達到平衡時H2的轉化率為60%,則在起始時體系中加入N2的物質的量為__________mol,此條件下(T2),反應的平衡常數K=__________。
③圖像中T2和T1的關系是__________。(填“高于”、“低于”、“等于”、“無法確定”)。
(2)氨氣和氧氣從145℃就開始反應,在不同溫度和催化劑條件下生成不同產物(如圖):
4NH3+5O24NO+6H2O
4NH3+3O22N2+6H2O
溫度較低時以生成__________為主,溫度高于900℃時,NO產率下降的原因是__________。
(3)現以H2與O2、熔融鹽Na2CO3組成的燃料電池(如圖所示,其中Y為CO2)裝置進行電解。
寫出石墨Ⅰ電極上發生反應的電極反應式:__________。
在電解池中生成N2O5的電極反應式為:__________。
查看答案和解析>>
科目:高中化學 來源:2013屆黑龍江省大慶市三十五中高三期中考試化學試卷(帶解析) 題型:填空題
(14分)(1)某科研小組研究在其他條件不變的情況下,改變起始氫氣物質的量[用n(H2)表示]對N2(g)+3H2(g) 2NH3(g)反應的影響,實驗結果可表示成如下圖所示的規律(圖中T表示溫度,n表示物質的量):
2NH3(g)反應的影響,實驗結果可表示成如下圖所示的規律(圖中T表示溫度,n表示物質的量):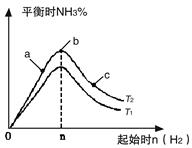
①比較在a、b、c三點所處的平衡狀態中,反應物N2的轉化率最高的是__________。
②若容器容積為1L,n=3mol,反應達到平衡時N2、H2的轉化率均為60%,則在起始時體系中加入N2的物質的量為__________mol,此條件下(T2),反應的平衡常數K=_________,當溫度升高時該平衡常數將__________。
③圖像中T2和T1的關系是__________。(填“高于”、“低于”、“等于”、“無法確定”)。
(2)氨氣和氧氣從145℃就開始反應,在不同溫度和催化劑條件下生成不同產物(如圖):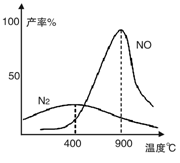
4NH3+5O2 4NO+6H2O 4NH3+3O2
4NO+6H2O 4NH3+3O2 2N2+6H2O
2N2+6H2O
溫度較低時以生成__________為主,溫度高于900℃時,NO產率下降的原因是___________________
查看答案和解析>>
科目:高中化學 來源:2012-2013學年黑龍江省大慶市高三期中考試化學試卷(解析版) 題型:填空題
(14分)(1)某科研小組研究在其他條件不變的情況下,改變起始氫氣物質的量[用n(H2)表示]對N2(g)+3H2(g) 2NH3(g)反應的影響,實驗結果可表示成如下圖所示的規律(圖中T表示溫度,n表示物質的量):
2NH3(g)反應的影響,實驗結果可表示成如下圖所示的規律(圖中T表示溫度,n表示物質的量):
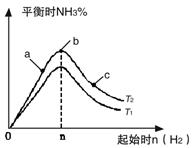
①比較在a、b、c三點所處的平衡狀態中,反應物N2的轉化率最高的是__________。
②若容器容積為1L,n=3mol,反應達到平衡時N2、H2的轉化率均為60%,則在起始時體系中加入N2的物質的量為__________mol,此條件下(T2),反應的平衡常數K=_________,當溫度升高時該平衡常數將__________。
③圖像中T2和T1的關系是__________。(填“高于”、“低于”、“等于”、“無法確定”)。
(2)氨氣和氧氣從145℃就開始反應,在不同溫度和催化劑條件下生成不同產物(如圖):
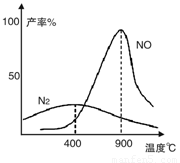
4NH3+5O2 4NO+6H2O 4NH3+3O2
4NO+6H2O 4NH3+3O2 2N2+6H2O
2N2+6H2O
溫度較低時以生成__________為主,溫度高于900℃時,NO產率下降的原因是___________________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com