
| A. | ③④⑤⑦⑧⑨ | B. | ③⑤⑥⑦⑧⑨ | C. | ②③④⑤⑦⑧ | D. | ①②④⑥⑧⑨ |
分析 元素的非金屬性越強,其原子得電子能力越強,所以可以根據元素的非金屬性判斷,非金屬性強弱的比較方法:①單質與氫氣易(難)反應;②生成的氫化物穩定(不穩定);③最高價氧化物的水化物(含氧酸)酸性強(弱);④相互置換反應(強制弱);⑤單質得電子的能力比較非金屬性強弱等,以此來解答.
解答 解:①物質的溶解性屬于物理性質,與元素的非金屬性及得電子能力無關,所以HCl的溶解度比H2S大,不能說明氯元素原子得電子能力比硫強,故①錯誤;
②不能根據氫化物的水溶液的酸性強弱比較非金屬性,例如HI的酸性比HCl強,但非金屬性Cl>I;雖硫化氫的酸性比鹽酸弱,但非金屬性Cl>S,不能說明氯元素原子得電子能力比硫強,故②錯誤;
③元素的非金屬性越強,對應氫化物的穩定性越強,氯化氫比硫化氫穩定,可說明氯元素的非金屬性比硫元素強,能說明氯元素原子得電子能力比硫強,故③正確;
④陰離子的還原性越強,對應元素的非金屬性越弱,還原性:Cl-<S2-,能說明氯元素原子得電子能力比硫強,故④正確;
⑤元素的非金屬性越強,對應最高價氧化物的水化物的酸性越強,HClO4的酸性比H2SO4強,能說明氯元素原子得電子能力比硫強,故⑤正確;
⑥單質的熔沸點屬于物理性質,與得電子能力無關,單質熔點:S>Cl2,不能說明氯元素原子得電子能力比硫強,故⑥錯誤;
⑦元素的非金屬性越強,對應單質的氧化性越強,氯氣與H2S能發生置換反應,說明氯氣的氧化性大于S,元素的非金屬性Cl大于S,能說明氯元素原子得電子能力比硫強,故⑦正確;
⑧同周期從左到右元素的非金屬性增強,得電子能力增強,所以在周期表中Cl處于S同周期的右側,能說明氯元素原子得電子能力比硫強,故⑧正確;
⑨元素的非金屬性越強,對應單質的氧化性越強,得電子能力越強,Cl2與鐵反應生成FeCl3,而S與鐵反應生成FeS,能說明氯元素原子得電子能力比硫強,故⑨正確.
故選A.
點評 本題考查元素原子得電子能力的比較,可以從非金屬性的角度判斷,題目難度中等,注意非金屬性的遞變規律以及比較非金屬性的角度.


 學練快車道快樂假期暑假作業新疆人民出版社系列答案
學練快車道快樂假期暑假作業新疆人民出版社系列答案 浙大優學小學年級銜接導與練浙江大學出版社系列答案
浙大優學小學年級銜接導與練浙江大學出版社系列答案 小學暑假作業東南大學出版社系列答案
小學暑假作業東南大學出版社系列答案 津橋教育暑假拔高銜接廣東人民出版社系列答案
津橋教育暑假拔高銜接廣東人民出版社系列答案科目:高中化學 來源: 題型:解答題
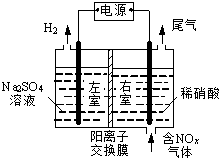 電解法處理含氮氧化物廢氣,可回收硝酸,具有較高的環境效益和經濟效益.實驗室模擬電解法吸收NOx的裝置如右圖所示(圖中電極均為石墨電極).
電解法處理含氮氧化物廢氣,可回收硝酸,具有較高的環境效益和經濟效益.實驗室模擬電解法吸收NOx的裝置如右圖所示(圖中電極均為石墨電極).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③④⑤⑥ | B. | 只有②③⑤ | C. | 只有①③④⑥ | D. | 只有①②③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 等濃度的碳酸鈉、碳酸氫鈉溶液混合后:c(CO32-)<c(HCO3-) | |
| B. | 沸水中滴加適量飽和FeCl3溶液,形成帶電的膠體,導電能力增強 | |
| C. | 在恒溫、恒容條件下,SO2與O2按照物質的量之比為2:1通入達到平衡,若向上述平衡體系中通入氧氣,則SO3的百分含量將減小 | |
| D. | pH=3的鹽酸和醋酸,等體積混合因為醋酸被稀釋pH>3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH2CH2CH2Cl | B. | CH3CH2-CHCl-CH2CH3 | ||
| C. | CH3-CHCl-CH2CH2CH3 | D. | (CH3)3CCH2Cl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
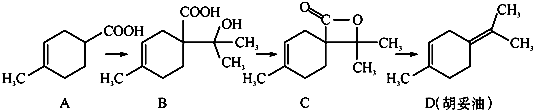
| A. | 從B到C的反應是消去反應 | |
| B. | D分子中所有碳原子一定共面 | |
| C. | 等物質的量的B分別與足量的Na、NaHCO3反應,產生的氣體的物質的量前者大于后者 | |
| D. | 若A是由2-甲基-1,3-丁二烯和丙烯酸(CH2=CHCOOH)加熱得到的,則該反應的類型屬于加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 共價化合物中只有共價鍵,一定沒有離子鍵 | |
| B. | 金屬和非金屬一定形成離子化合物 | |
| C. | 含有離子鍵的化合物一定是離子化合物 | |
| D. | 離子化合物中可能含有極性共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com