
【題目】(1)根據反應回答下列問題:K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
①用雙線橋法分析該氧化還原反應(標明得失電子及數目):__
K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
②以上反應中還原產物是__,氧化劑與還原劑的物質的量之比為___。
(2)寫出下列化學反應的離子方程式:
①過氧化鈉與水反應___。
②鈉單質與水反應___。
③醋酸與氫氧化鉀溶液反應___。
【答案】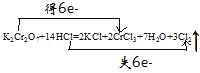 CrCl3 1:6 2Na2O2+2H2O=4Na++4OH-+O2↑ 2Na+2H2O=2Na++2OH-+H2↑ CH3COOH+OH-=CH3COO-+H2O
CrCl3 1:6 2Na2O2+2H2O=4Na++4OH-+O2↑ 2Na+2H2O=2Na++2OH-+H2↑ CH3COOH+OH-=CH3COO-+H2O
【解析】
(1)根據氧化還原反應中元素化合價的變化分析雙線橋和氧化劑和還原劑;
(2)根據離子方程式的書寫原則書寫離子方程式。
(1)①反應中鉻元素化合價降低,得電子,氯元素化合價升高,失去電子,根據電子數分析,雙線橋為: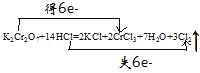 ;
;
②反應中鉻元素化合價降低,所以CrCl3為還原產物,K2Cr2O7為氧化劑,HCl為還原劑,二者比例為1:6;
(2)過氧化鈉和水反應生成氫氧化鈉和水,離子方程式為:2Na2O2+2H2O=4Na++4OH-+O2;
鈉和水反應生成氫氧化鈉和氫氣,離子方程式為:2Na+2H2O=2Na++2OH-+H2↑;
醋酸和氫氧化鉀反應生成醋酸鉀和水,離子方程式為:CH3COOH+OH-=CH3COO-+H2O。


科目:高中化學 來源: 題型:
【題目】免兒草醛是一種常見的香料添加劑。由免兒草醇制備免兒草醛的反應如下:
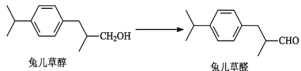
下列說法正確的是( )
A. 兔兒草醛的分子結構中苯環上的二溴代物有4種
B. 兔兒草醇和兔兒草醛都能發生氧化反應、加成反應,不能發生取代反應
C. 將兔兒草醇轉化為兔兒草醛所采用的試劑可以是“酸性K2Cr2O7溶液
D. 兔兒草醇分子結構中的所有碳原子可能共平面
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物J 是我國自主成功研發的一類新藥,它屬于酯類,分子中除苯環外還含有一個五元環。合成J的一種路線如下:

已知:RBr![]() RMgBr
RMgBr 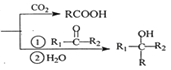
回答下列問題:
(1)B的結構簡式是________________。C的結構簡式是______________。
(2)D生成E的化學方程式為_________________。
(3)J的結構簡式是________________。
(4)根據C ![]() X,X的分子式為______。X有多種同分異構體,其中滿足下列條件的同分異構體共有______種(已知:碳碳叁鍵或碳碳雙鍵不能與羥基直接相連)。
X,X的分子式為______。X有多種同分異構體,其中滿足下列條件的同分異構體共有______種(已知:碳碳叁鍵或碳碳雙鍵不能與羥基直接相連)。
A 除苯環外無其他環,且無-O-O-鍵
B 能與FeCl3溶液發生顯色反應
C 苯環上一氯代物只有兩種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列敘述正確的是( )
A. 標況下,224 L H2O含有的分子數為10NA
B. 1 mol任何氣體所含的原子數均為NA
C. 28 g CO所含的分子數為NA
D. 標況下,NA個分子的體積為22.4 L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Li4Ti5O12和LiFePO4都是鋰離子電池的電極材料,可利用鈦鐵礦(主要成分為FeTiO3,還含有少量MgO、SiO2等雜質)來制備,工藝流程如下:
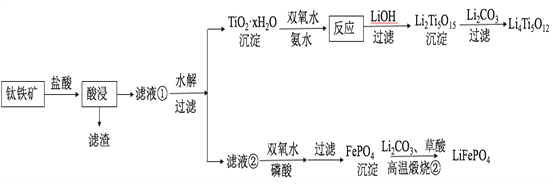
回答下列問題:
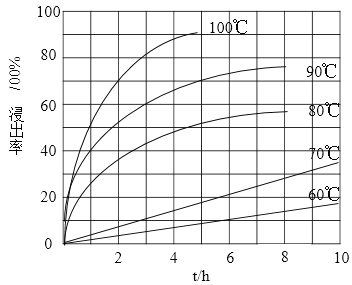
(1)“酸浸”實驗中,鐵的浸出率結果如下圖所示。由圖可知,當鐵的凈出率為70%時,所采用的實驗條件為___________________。
(2)“酸浸”后,鈦主要以TiOCl42-形式存在,寫出相應反應的離子方程式__________________。
(3)TiO2·xH2O沉淀與雙氧水、氨水反應40 min所得實驗結果如下表所示:
溫度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O轉化率% | 92 | 95 | 97 | 93 | 88 |
分析40℃時TiO2·xH2O轉化率最高的原因__________________。
(4)Li2Ti5O15中Ti的化合價為+4,其中過氧鍵的數目為__________________。
(5)若“濾液②”中c(Mg2+)=0.02 mol/L,加入雙氧水和磷酸(設溶液體積增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L,此時是否有Mg3(PO4)2沉淀生成?___________(列式計算)。
FePO4、Mg3(PO4)2的Ksp分別為1.3×10-22、1.0×10-24。
(6)寫出“高溫煅燒②”中由FePO4制備LiFePO4的化學方程式______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是硫酸試劑瓶標簽上的內容:

(1)該硫酸的物質的量濃度為___mol/L。
(2)某小組進行硫酸酸性實驗探究時,需要250mL 4.6mol/L的稀硫酸,則需要取上述的濃硫酸___mL。
(3)在配制4.6mol/L稀硫酸的過程中,下列情況對所配制硫酸溶液物質的量濃度有何影響(填“偏高”“偏低”或“無影響”)?
①定容時仰視讀數:__;
②移液時不慎將少量溶液滴在容量瓶外面:___。
(4)實驗過程中出現下列情況應如何處理?
①向容量瓶中加入蒸餾水至距刻度線1~2cm時,應___;
②加蒸餾水時不慎超過了刻度,應__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將飽和氯化鐵溶液滴入沸水時,液體變為________色,得到的是________,反應的化學方程式為________________________。用此分散系進行實驗:
(1)將其裝入U形管內,用石墨作電極,接通直流電源,通電一段時間后發現陰極附近顏色________,這表明____________________,這種現象稱為________。
(2)向其中加入飽和的氯化鈉溶液,發生的現象是____________。
(3)向其中逐滴加入過量稀硫酸,現象是______________,原因是___________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)下列關于充電電池、干電池的敘述合理的是___________。
①干電池可以實現化學能向電能的轉化和電能向化學能的轉化
②鋅錳干電池長時間連續使用時內裝糊狀物可能流出腐蝕電器
③充電電池可以無限制地反復放電、充電
④充電是使放電時的氧化還原反應逆向進行
(2)鉛蓄電池中,正極材料為PbO2,負極材料為Pb,放電時其負極反應式為_____________。
(3)原電池在NaOH溶液介質中,鋁為負極,其負極反應式為_______________。
(4)如圖為綠色電源“二甲醚(CH3OCH3)燃料電池”的工作原理示意圖。b電極是_____極,請寫出負極的電極反應方程式:___________________________。
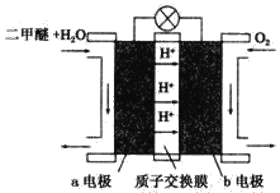
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA表示阿伏加德羅常數的值,下列說法中正確的有
①0.1mol丙烯酸中含有雙鍵的數目為0.1NA
②12g金剛石中,碳碳共價鍵數為4NA
③常溫下,21g C3H6和C4H8的混合物中含有的碳原子數為1.5NA
④2g ![]() 中含有的質子數、中子數、電子數均為NA
中含有的質子數、中子數、電子數均為NA
⑤常溫常壓下,S2和S6的混合物共6.4g,其中所含硫原子數一定為0.2NA
⑥10mL 18mol/L的濃硫酸與足量的鎂反應時轉移的電子數為0.18NA
A. ①⑥B. ④⑤⑥C. ③④⑤D. ①②⑥
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com