
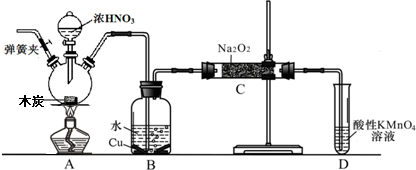
分析 (1)以木炭、濃硝酸、水和銅為原料生成的一氧化氮與過氧化鈉反應制備亞硝酸鈉,由于該實驗中有氣體參加,所以在組裝好儀器后首先要檢查裝置的氣密性,再裝藥品,由于實驗過程中有一氧化氮產生,所以要將裝置中的空氣全部排盡,再進行實驗,據此確定實驗操作順序;
(2)裝置B中是A裝置生成的二氧化氮和水反應生成硝酸和一氧化氮,硝酸和銅反應生成硝酸銅,一氧化氮和水;通過裝置C中的過氧化鈉吸收一氧化氮、二氧化碳,最后通過酸性高錳酸鉀溶液除去剩余一氧化氮防止污染空氣;
(3)依據亞硝酸鈉具有氧化性或還原性,選擇還原劑或氧化劑發生的反應現象證明產物中是否是亞硝酸鈉;
(4)因為一氧化氮中混有二氧化碳和水蒸汽,二氧化碳和過氧化鈉發生的反應生成碳酸鈉和氧氣,水與過氧化鈉反應生成氫氧化鈉;為避免產生這些副產物,應在B、C裝置間增加裝置E,E中盛放的試劑應堿石灰,用來吸收二氧化碳;
(5)依據碳酸鈉與強酸反應生成能使澄清石灰水變渾濁的氣體證明產物中是否是碳酸鈉;
(6)n(Na2O2)=$\frac{15.6g}{78g/mol}$=0.2mol,根據2NO+Na2O2=2NaNO2、3NO2+H2O=2HNO3+NO、C+4HNO3(濃) $\frac{\underline{\;△\;}}{\;}$CO2↑+4NO2↑+2H2O計算需要C的質量.
解答 解:(1)(1)以木炭、濃硝酸、水和銅為原料生成的一氧化氮與過氧化鈉反應制備亞硝酸鈉,由于該實驗中有氣體參加,所以在組裝好儀器后首先要檢查裝置的氣密性,再裝藥品,由于實驗過程中有一氧化氮產生,所以要將裝置中的空氣全部排盡,再進行實驗,所以實驗操作順序為⑤④③②①,
故答案為:⑤④③②①;
(2)裝置B中是A裝置生成的二氧化氮和水反應生成硝酸和一氧化氮,3NO2+H2O=2HNO3+NO,硝酸和銅反應生成硝酸銅,一氧化氮和水,所以反應現象為溶液變藍,銅片溶解,導管口有無色氣體冒出;通過裝置C中的過氧化鈉吸收一氧化氮、二氧化碳,最后通過酸性高錳酸鉀溶液除去剩余一氧化氮防止污染空氣,
故答案為:銅片溶解,溶液變藍,導管口有無色氣體冒出;除去未反應的NO,防止污染空氣;
(3)檢驗亞硝酸鈉的實驗設計為:取少量生成物置于試管中,加入稀鹽酸,若產生無色氣體并在液面上方變為紅棕色,則產物是亞硝酸鈉.
故答案為:取樣,加入稀鹽酸,若產生無色氣體并在液面上方變為紅棕色,則產物是亞硝酸鈉;
(4)因為一氧化氮中混有二氧化碳和水蒸汽,二氧化碳和過氧化鈉發生的反應生成碳酸鈉和氧氣,水與過氧化鈉反應生成氫氧化鈉,故C產物中除亞硝酸鈉外還含有副產物碳酸鈉和氫氧化鈉,為避免產生這些副產物,應在B、C裝置間增加裝置E,E中盛放的試劑應堿石灰,用來吸收二氧化碳;
故答案為:氫氧化鈉; 堿石灰;
(5)檢驗碳酸鈉的實驗設計為:取少量生成物置于試管中,加入稀鹽酸,若產生能使澄清石灰水變渾濁的氣體,則產物有碳酸鈉.
故答案為:取樣,加入稀鹽酸,若產生能使澄清石灰水變渾濁的氣體,則產物有碳酸鈉;
(6)n(Na2O2)=$\frac{15.6g}{78g/mol}$=0.2mol,根據2NO+Na2O2=2NaNO2知,0.2mol過氧化鈉反應需要0.4molNO,根據3NO2+H2O=2HNO3+NO知生成0.4molNO需要1.2mol二氧化氮、根據C+4HNO3(濃) $\frac{\underline{\;△\;}}{\;}$CO2↑+4NO2↑+2H2O知生成1.2mol二氧化氮需要0.3molC,則C的質量=12g/mol×0.3mol=3.6g,
故答案為:3.6.
點評 本題考查了物質制備實驗方案的設計和信息判斷,物質性質的理解應用,注意實驗過程中的反應現象分析,掌握基礎是關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | ①③⑤ | B. | ④⑤⑥ | C. | ②③④ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
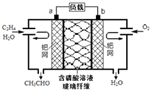 乙烯催化氧化成乙醛可設計成如圖所示的燃料電池,能在制備乙醛的同時獲得電能,其總反應為:2CH2=CH2+O2→2CH3CHO.下列有關說法正確的是( )
乙烯催化氧化成乙醛可設計成如圖所示的燃料電池,能在制備乙醛的同時獲得電能,其總反應為:2CH2=CH2+O2→2CH3CHO.下列有關說法正確的是( )| A. | a電極發生還原反應 | |
| B. | 放電時,每轉移2mol電子,理論上需要消耗28g乙烯 | |
| C. | b極反應式為:O2+4e-+2H2O═4OH- | |
| D. | 電子移動方向:電極a→磷酸溶液→電極b |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 海水蒸發→云→降水,這是地球水循環的過程,該過程主要是物理變化 | |
| B. | 海水中所含的常量元素大部分以鹽的形式存在,其中含量最高的鹽是氯化鈉 | |
| C. | 海洋是化學元素的集散地,元素周期表所有的元素在海水中都能找到 | |
| D. | 由海水制備鎂、氯、溴、碘等單質均需要涉及氧化還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | a mol Na2O2中含有的離子數為4aNA | |
| B. | 100mL 1mol/L NaHCO3溶液中含有0.1NA個HCO3- | |
| C. | 標準狀況下,2.24L氟化氫,其分子數為0.1NA | |
| D. | 28g N2和N4的混合氣體中含有原子個數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 單質沸點:X>Y | B. | 陽離子的氧化性:W>Y | ||
| C. | 氧化物對應水化物的酸性:Z>X | D. | Y、Z離子均能抑制水的電離 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 過氧化鈉與水反應時,生成22.4L氧氣轉移的電子數為2 NA | |
| B. | 18g D2O中含有的電子數和中子數均為10 NA | |
| C. | 密閉容器中2mol NO與1mol O2充分反應,產物的分子數為2 NA | |
| D. | 1mol Na與足量的O2反應,生成Na2O和Na2O2的混合物,鈉失去 NA個電子 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com