
(9分)高鐵酸鈉是一種高效多功能水處理劑。工業上常采用NaClO氧化法生產,反應原理為:在堿性條件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4,過濾得到粗產品,再用NaOH溶液溶解,重結晶,用有機溶劑脫堿,低溫烘干得到固體樣品。反應方程式為:
3NaClO + 2Fe(NO3)3 + 10NaOH=2Na2FeO4↓+ 3NaCl + 6NaNO3 + 5H2O
(1)上述制備過程中,用NaOH溶液溶解粗產品而不用水的原因是 。
(2)高鐵酸鈉電池是一種新型可充電電池,電解質為NaOH溶液,放電時負極材料為Zn,正極產生紅褐色沉淀,寫出該電池反應方程式 。
(3)生產高鐵酸鈉的原料之一Fe(NO3)3用黑色粉末Fe(含有Fe3O4)與稀硝酸反應制備。準確稱取該黑色粉末13.12g,加入200mL 4 mol·L-1 HNO3攪拌,固體完全溶解,共收集到標準狀況下2688mL的氣體,經分析其中只含有NO,并測得此時溶液中c(H+)=0.4mol·L-1(設反應前后溶液體積不變)。通過以上數據,計算該黑色粉末中Fe的質量分數。(寫出計算過程,結果保留兩位小數)
 中考解讀考點精練系列答案
中考解讀考點精練系列答案科目:高中化學 來源:2016屆黑龍江省高三上學期第一次月考化學試卷(解析版) 題型:選擇題
下列敘述中正確的是
A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3飽和溶液,又有CaCO3沉淀生成
B.向Na2CO3溶液中逐滴加入等物質的量的稀鹽酸,生成的CO2與原Na2CO3的物質的量之比為1:2
C.等質量的NaHCO3和Na2CO3分別與足量鹽酸反應,在同溫同壓下,生成的CO2體積相同
D.向Na2CO3飽和溶液中通入CO2,有NaHCO3結晶析出
查看答案和解析>>
科目:高中化學 來源:2016屆河南省高三第二次月考化學試卷(解析版) 題型:選擇題
下列混合物的分離或提純操作中不正確的是
A.除去N2中的少量O2,可通過灼熱的Cu網后,收集氣體
B.除去Fe(OH)3膠體中混有的Cl- 離子,可用滲析的方法
C.除去乙醇中的少量NaCl,可用蒸餾的方法
D.重結晶、滴定操作都可用于提純物質
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖北省高二第一學期第一次月考化學試卷(解析版) 題型:選擇題
下列描述中,不符合生產實際的是( )
A.電解熔融的氧化鋁制取金屬鋁,用鐵作陽極
B.電解法精煉銅,用純銅作陰極
C.電解飽和食鹽水制燒堿,用涂鎳碳鋼網作陰極
D.在鍍件上電鍍鋅,用鋅作陽極
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省邯鄲市高一上第一次月考化學試卷(解析版) 題型:選擇題
下列說法正確的是(NA表示阿伏加德羅常數的值)
A.在常溫常壓下,11.2 L N2含有的原子數為NA
B.32 g O2在標準狀況下所占體積約為22.4 L
C.標準狀況下,18 g H2O所占的體積約為22.4 L
D.在同溫同壓下,相同體積的任何氣體單質所含的原子數相同
查看答案和解析>>
科目:高中化學 來源:2016屆江蘇省高三上學期第一次月考化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.金屬在反應中只能作還原劑,非金屬在反應中只能作氧化劑
B.氧化劑在反應中失去電子,還原劑在反應中得到電子
C.氧化劑具有氧化性,還原劑具有還原性
D.陽離子只有氧化性,陰離子只有還原性
查看答案和解析>>
科目:高中化學 來源:2016屆黑龍江省高三第一階段考試理綜化學試卷(解析版) 題型:選擇題
鐵、銅混合粉末18.0g加入到100ml 5.0mol/LFeCl3溶液中,剩余固體質量為3.2g。下列說法正確的是
A.剩余固體是鐵、銅混合物
B.反應后溶液中n(Fe2+)+ n(Cu2+)=0.75 mol
C.反應后溶液中n(Fe3+)=0.10 mol
D.原固體混合物中銅的質量是8.0g
查看答案和解析>>
科目:高中化學 來源:2016屆河北省冀州市高三復習班上第一次月考化學試卷A(解析版) 題型:選擇題
科學家宣布發現了鋁的“超級原子”結構———Al13和Al14。 已知這類“超級原子”最外層電子數之和為40個時處于相對穩定狀態。下列說法中,正確的是
A.Al13、Al14互為同位素
B.Al13超原子中Al原子間通過離子鍵結合
C.Al14最外層電子數之和為42,與第ⅡA族元素原子的性質相似
D.Al13和Al14都具有較強的還原性,容易失去電子生成陽離子
查看答案和解析>>
科目:高中化學 來源:2016屆河南省高三第四次大考化學試卷(解析版) 題型:實驗題
(14分)我國制堿工業的先驅 侯德榜先生,1939年發明了著名的侯氏制堿法,其核心反應原理可用如下化學方程式表示:NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓(晶體)依據此原理,欲制得碳酸氫鈉晶體,某校學生設計了如下實驗裝置,其中B裝置中的試管內是溶有氨和氯化鈉的溶液,且二者均已達到飽和。
侯德榜先生,1939年發明了著名的侯氏制堿法,其核心反應原理可用如下化學方程式表示:NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓(晶體)依據此原理,欲制得碳酸氫鈉晶體,某校學生設計了如下實驗裝置,其中B裝置中的試管內是溶有氨和氯化鈉的溶液,且二者均已達到飽和。
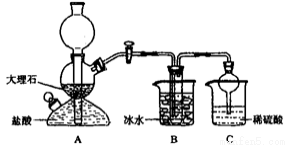
(1)A裝置中所發生反應的離子方程式為________。C裝置中稀硫酸的作用為_________。
(2)該校學生在檢查完此套裝置氣密性后進行實驗,結果沒有得到碳酸氫鈉晶體,指導教師指出應在裝置 之間(填寫字母)連接一個盛有 的洗氣裝置,其作用是 。
(3)過濾NaHCO3 時除燒杯、漏斗外,還用到另一玻璃儀器,該儀器在此操作中的主要作用是 。
(4)若該校學生進行實驗時,所用飽和食鹽水中含NaCl的質量為5.85g,實驗后得到干燥的晶體的質量為5 .04g,則NaHCO3的產率為 。
.04g,則NaHCO3的產率為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com