
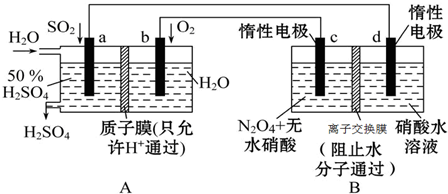
分析 (1)A裝置能自發的進行氧化還原反應且沒有外接電源;
(2)與電源的正極相連的電極為陽極,N2O4在陽極失電子生成N2O5;
(3)通入O2一極是原電池的正極,氧氣得電子生成水;
(4)電池的負極反應式為:SO2-2e-+2H2O=4H++SO42-,根據方程式計算,注意硫酸的濃度不變.
解答 解:(1)A裝置能自發的進行氧化還原反應且沒有外接電源,所以是原電池,
故答案為:原電池;
(2)與電源的正極相連的電極為陽極,c極與正極相連為陽極,N2O4在陽極失電子生成N2O5,電極反應式為:N2O4+2HNO3-2e-═2N2O5+2H+;
故答案為:c極;N2O4+2HNO3-2e-═2N2O5+2H+;
(3)通入O2一極是原電池的正極,電極反應式為:O2-4e-+4H+=2H2O,故答案為:O2-4e-+4H+=2H2O;
(4)電池的負極反應式為:SO2-2e-+2H2O=4H++SO42-,1min內n(SO2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,消耗水0.2mol,生成硫酸的質量為:0.1mol×98g/mol=9.8g,消耗水的質量為:0.2mol×18g/mol=3.6g,向右側正極區定向移動0.2mol,即0.2g H+,
設1min內通入xmLH2O,
則有:$\frac{9.8g}{9.8g+x×1g/mol-3.6g-0.2g}$×100%=50%
x=13.6mL/min,
故答案為:13.6.
點評 本題考查了原電池和電解池原理,根據是否自發進行判斷原電池和電解池,再結合各個電極上發生的電極反應分析解答,難點是電極反應式的書寫,題目難度中等,側重于考查學的分析能力和計算能力.


科目:高中化學 來源: 題型:選擇題
| A. | Fe在少量Cl2中燃燒生成FeCl2 | |
| B. | 石油的裂解、煤的干餾都是化學變化 | |
| C. | 化學反應的焓變與反應的途徑有關 | |
| D. | 等質量的銅按a、b兩種途徑完全轉化為硝酸銅,途徑a、b消耗的硝酸一樣多 途徑a:Cu$→_{△}^{O_{2}}$CuO$\stackrel{稀硝酸}{→}$Cu(NO3)2;途徑b:Cu$\stackrel{稀硝酸}{→}$Cu(NO3)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原電池是將電能轉變為化學能的裝置 | |
| B. | 原電池陽極發生氧化反應 | |
| C. | 電解池陰極發生還原反應 | |
| D. | 電解池的陰極連接電源正極 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al3+與SO42-的物質的量濃度之比為2:3 | |
| B. | 1L溶液中SO42-的物質的量為1.5mol | |
| C. | 準確稱取17.1g的Al2(SO4)3用100 mL蒸餾水溶解可配制得到該濃度的溶液 | |
| D. | 從1L 0.5 mol•L-1Al2(SO4)3溶液中取出100mL,Al3+濃度仍為1 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 氫氧化鈉質量(g) | 氯化鈉質量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
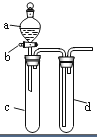 某興趣小組設計出如圖所示裝置來改進教材中“銅與硝酸反應”實驗,以探究化學實驗的綠色化.
某興趣小組設計出如圖所示裝置來改進教材中“銅與硝酸反應”實驗,以探究化學實驗的綠色化.| 方案 | 反應物 |
| 甲 | Cu、濃HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向某溶液中滴加足量稀HCl,產生氣體能使澄清石灰水變渾濁,則說明原溶液中一定含CO32- | |
| B. | 向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,則說明原溶液中一定含Ag+ | |
| C. | 向某溶液中滴加KSCN溶液,若溶液出現血紅色則說明原溶液中含Fe3+ | |
| D. | 用鉑絲蘸取某溶液在酒精燈火焰上灼燒直接觀察火焰顏色,未見紫色,說明原溶液中不含K+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:C>A | |
| B. | 氣態氫化物的穩定性:A>B | |
| C. | 最髙價氧化物對應水化物的堿性:C<D | |
| D. | 元素C、D的最高價氧化物對應的水化物之間不能發生反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com