
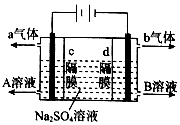
 利用三室式電解池(裝置結構如圖所示,電極均為惰性電極)可以實現用硫酸鈉溶液制取硫酸和氫氧化鈉.下列敘述正確的是( )
利用三室式電解池(裝置結構如圖所示,電極均為惰性電極)可以實現用硫酸鈉溶液制取硫酸和氫氧化鈉.下列敘述正確的是( )| A. | a氣體為氫氣,b氣體為氧氣 | |
| B. | A為氫氧化鈉溶液,B為硫酸溶液 | |
| C. | 通電后中間隔室的SO42-向陰極移動,陽極區溶液的pH增大 | |
| D. | 該電解反應的方程式為2Na2SO4+6H2O$\frac{\underline{\;電解\;}}{\;}$2H2SO4+4NaOH+O2↑+2H2↑ |
分析 根據外加電源的正負極可知有氣體a生成的一極為陽極,發生氧化反應,生成a為氧氣,同時生成氫離子,有氣體b生成的一極為陰極,發生還原反應,生成b為氫氣,同時陰極生成氫氧根離子;陽離子透過d隔膜向陰極移動,陰離子透過c隔膜向陽極移動,A應為硫酸,B為氫氧化鈉,以此解答該題.
解答 解:A.在陽極氫氧根離子放電生成氧氣,在陰極氫離子放電生成氫氣,所以a氣體為氧氣,b氣體為氫氣,故A錯誤;
B.在陽極氫氧根離子放電生成氧氣,同時生成氫離子,所以陽極生成硫酸,即A溶液為硫酸;在陰極氫離子放電生成氫氣,同時生成氫氧根離子,所以陰極生成NaOH,即B溶液為氫氧化鈉,故B錯誤;
C.通電后中間隔室的SO42-向陽極移動,陽極生成硫酸,pH減小,故C錯誤;
D.在陽極氫氧根離子放電生成氧氣,在陰極氫離子放電生成氫氣,所以該電解反應的總方程式為2Na2SO4+6H2O$\frac{\underline{\;電解\;}}{\;}$2H2SO4+4NaOH+O2↑+2H2↑,故D正確.
故選D.
點評 本題考查了電解池原理的應用,為高考常見題型和高頻考點,側重考查學生的分析能力,注意根據外加電源的正負極判斷電解池的陰陽極,根據離子移動方向判斷離子交換膜,注意把握題目中給出的信息,題目難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3COOH+H2O?CH3COO-+H3O+ | B. | HS-+H2O?S2-+H3O+ | ||
| C. | CO2+H2O?HCO3-+H+ | D. | CO32-+H2O?HCO3-+OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 35Cl原子所含質子數為18 | |
| B. | $\frac{1}{18}$mol的1H35Cl的分子所含中子數約為6.02×1023 | |
| C. | 3.5Cl2氣體的體積約為22.4L | |
| D. | 35Cl2氣體的摩爾質量為70 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 編號 | 實驗操作 | 實驗現象 | 解釋與結論 |
| A | 將SO2氣體通入KMnO4(H+)溶液中 | 溶液褪色 | SO2有漂白性 |
| B | 將SO2氣體通入H2S溶液中 | 溶液變渾濁 | SO2有氧化性 |
| C | 將SO2氣體通入紫色石蕊溶液中 | 溶液先變紅色后褪色 | SO2是酸性氧化物 |
| D | 將SO2氣體通入Ca(ClO)2溶液中 | 溶液變渾濁 | 亞硫酸的酸性比次氯酸的酸性強 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 圖中膜為陰膜(只允許陰離子通過),OH-從右往左通過該膜 | |
| B. | 電解時,陰極電極反應式為:2H++2e-═H2↑ | |
| C. | 電解時,如有3mol電子通過導線,則一定生成0.6mol KIO3 | |
| D. | 電池總反應為:KI+3H2O $\frac{\underline{\;電解\;}}{\;}$KIO3+3H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
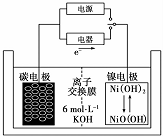 一種二次電池如圖所示,該電池的電解質為強堿溶液,下列說法中正確的是( )
一種二次電池如圖所示,該電池的電解質為強堿溶液,下列說法中正確的是( )| A. | 充電時陰極發生氧化反應 | |
| B. | 充電時將碳電極與電源的正極相連 | |
| C. | 放電時碳電極反應為原電池的負極 | |
| D. | 放電時鎳電極反應為Ni(OH)2-e-+OH-=NiO(OH)+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 油脂屬于天然高分子化合物,在堿性條件下水解可制得肥皂 | |
| B. | 在一定條件下,氨基酸之間能發生反應合成多肽 | |
| C. | 在淀粉水解液中加入氫氧化鈉,再加入碘水,溶液未變藍,說明淀粉己完全水解 | |
| D. | 蛋白質溶液中加入Na2SO4濃溶液有固體析出,加入足量水后固體不溶解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | -48.5kJ/mol | B. | +48.5kJ/mol | C. | -45.5kJ/mol | D. | +45.5kJ/mol |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com