
| 序號 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 儀 器 及 裝 置 圖 |  |  |  |  |  |  |
分析 利用實驗室制得的氯氣與銅反應制取純凈氯化銅,因實驗室制得的氯氣中混有氯化氯和水汽,需要除去后得到干燥的氯氣再與銅在加熱的情況下反應,為了得到純凈的氯化銅,在加熱反應前需要將裝置內的空氣排出,形成無氧環境,同時要考慮氯氣的尾氣對環境有污染,需要用氫氧化鈉溶液除去;
(1)儀器的連接方法:先制備反應物,然后除雜質,再使氯氣與銅反應,最后尾氣處理;進行氣體除雜或者干燥時,連接順序一般是:“長進短出”的原則,根據題中實驗原理,用濃鹽酸與二氧化錳反生成氯氣,除雜后與銅反應生成氯化銅,尾氣用氫氧化鈉吸收,據此答題;
(2)因需要干燥的氯氣與銅反應,故利用濃硫酸對氯氣進行干燥處理;
(3)氯氣中混有氯化氫氣體,可利用飽和食鹽水除去;
(4)裝置⑥是尾氣處理,吸收多余的氯氣,氯氣與氫氧化鈉反應生成氯化鈉和次氯酸鈉,根據電荷守恒書寫離子方程式;
(5)實驗中涉及氣體的,實驗開始時一般都要檢驗裝置氣密性,為了防止空氣中的成分的干擾,實驗結束時,有銅粉的裝置中還應再能一會兒氯氣;
(6)裝置⑤是實驗室制取氯氣,在燒瓶中發生反應的是濃鹽酸和二氧化錳,可寫出此反應的化學方程式.
解答 解:(1)儀器的連接方法:先制備反應物,然后除雜質,再使氯氣與銅反應,最后尾氣處理;進行氣體除雜或者干燥時,連接順序一般是:“長進短出”的原則,根據題中實驗原理,用濃鹽酸與二氧化錳反生成氯氣,除雜后與銅反應生成氯化銅,尾氣用氫氧化鈉吸收,所以儀器連接順序為:③⑤④②①⑥,故答案為:③⑤④②①⑥;
(2)裝置②中盛裝的是濃硫酸,可利用此裝置干燥氯氣,故答案為:干燥氯氣;
(3)飽和食鹽水可以除去氯氣中的氯化氫,故答案為:除去氯氣中混有的氯化氫;
(4)裝置⑥中氯氣與氫氧化鈉反應生成氯化鈉和次氯酸鈉,反應的離子方程式為Cl2+2OH-=Cl-+ClO-+H2O,故答案為:Cl2+2OH-=Cl-+ClO-+H2O;
(5)實驗中涉及氣體的,實驗開始時一般都要檢驗裝置氣密性,為了防止空氣中的成分的干擾,實驗結束時,有銅粉的裝置中還應再通一會兒氯氣至硬質玻璃管冷卻,所以實驗結束時,應先熄滅①處的酒精燈,故答案為:檢驗裝置氣密性;①;
(6)裝置⑤是利用二氧化錳和濃鹽酸混合加熱制氯氣,發生反應的化學方程式為MnO2+4HCl$\frac{\underline{\;加熱\;}}{\;}$MnCl2+Cl2↑+2H2O,故答案為:MnO2+4HCl$\frac{\underline{\;加熱\;}}{\;}$MnCl2+Cl2↑+2H2O.
點評 本題考查了常見氣體的制取和收集及實驗的注意事項,氯化鐵的性質和制取;關鍵是掌握其選擇的依據及原理,在裝置的分析中明確裝置的特點及其作用,難度較大.


 小學課時特訓系列答案
小學課時特訓系列答案科目:高中化學 來源: 題型:選擇題
| A. | 漂白粉可長期放置在燒杯中 | |
| B. | 金屬鈉燃燒時不能用水滅火,應該用沙子滅火 | |
| C. | 氯水可以用無色透明的試劑瓶裝保存 | |
| D. | 實驗后剩余的鈉不可放回原試劑瓶中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 (1)根據最新“人工固氮”的研究報道,在常溫常壓和光照條件下N2在催化劑表面與水發生反應:
(1)根據最新“人工固氮”的研究報道,在常溫常壓和光照條件下N2在催化劑表面與水發生反應:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
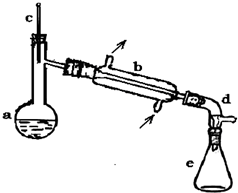 醇脫水是合成烯烴的常用方法,實驗室合成環己烯的反應
醇脫水是合成烯烴的常用方法,實驗室合成環己烯的反應 和實驗裝置如圖:
和實驗裝置如圖:| 相對分子質量 | 密度/(g?cm-3 ) | 沸點/℃ | 溶解性 | |
| 環己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 環己烯 | 82 | 0.8102 | 83 | 難溶于水 |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 活性炭、氯氣都能使品紅溶液褪色 | |
| B. | 苯、乙醇、纖維素都能與濃硝酸反應 | |
| C. | 乙烯、氯乙烯都能使溴水褪色 | |
| D. | 淀粉、蛋白質都能發生顯色(或顏色)反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com