



科目:高中化學(xué) 來源: 題型:
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
 如圖是某學(xué)校實驗室從化學(xué)試劑商店買回的濃硫酸試劑標(biāo)簽上的部分內(nèi)容.
如圖是某學(xué)校實驗室從化學(xué)試劑商店買回的濃硫酸試劑標(biāo)簽上的部分內(nèi)容. 你認(rèn)為該同學(xué)的錯誤步驟有
你認(rèn)為該同學(xué)的錯誤步驟有查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
 某同學(xué)用如圖所示裝置探究SO2的性質(zhì)及其有關(guān)實驗.
某同學(xué)用如圖所示裝置探究SO2的性質(zhì)及其有關(guān)實驗.查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
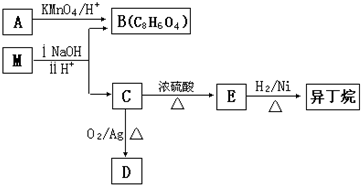 苯的同系物是人類最早認(rèn)識的芳香族化合物,其中對二甲苯(英文名稱p-xylene,縮寫為PX)是化學(xué)工業(yè)的重要原料.
苯的同系物是人類最早認(rèn)識的芳香族化合物,其中對二甲苯(英文名稱p-xylene,縮寫為PX)是化學(xué)工業(yè)的重要原料.查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com