
對于制氫氣原理CH4(g)+H2O(g) CO(g)+3H2(g)ΔH=+206.4 kJ·mol-1,一定可以提高平衡體系中H2百分含量,又能加快反應速率的措施是
CO(g)+3H2(g)ΔH=+206.4 kJ·mol-1,一定可以提高平衡體系中H2百分含量,又能加快反應速率的措施是
A.降低壓強 B.增大水蒸氣濃度 C.加入催化劑 D.升高溫度
 天天練口算系列答案
天天練口算系列答案科目:高中化學 來源:2015-2016學年西藏拉薩中學高二上第一次月考化學試卷(解析版) 題型:選擇題
未來新能源的特點是資源豐富,在使用時對環(huán)境無污染或污染很小,且可以再生。下列符合未來新能源標準的是
①天然氣 ②煤 ③核能 ④石油 ⑤太陽能 ⑥生物質(zhì)能 ⑦風能 ⑧氫能
A.①②③④ B.⑤⑥⑦⑧ C.③⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化學 來源:2016屆福建省高三上學期10月月考化學試卷(解析版) 題型:選擇題
某無色溶液含有下列離子中的若干種:H+、NH4+、Fe3+、Ba2+、Al3+、CO32-、Cl-、OH-、NO3-。向該溶液中加入鋁粉,只放出H2,則溶液中能大量存在的離子最多有
A.3種 B.4種 C.5種 D.6種
查看答案和解析>>
科目:高中化學 來源:2016屆山東省南校區(qū)高三上學期10月階段測化學試卷(解析版) 題型:選擇題
在某溫度下,反應ClF(g)+F2(g)?ClF3(g);ΔH=268 kJ/mol,在密閉容器中達到平衡。下列說法中,正確的是
A.溫度不變,縮小體積,ClF的轉(zhuǎn)化率增大
B.溫度不變,增大體積,ClF3的產(chǎn)率提高
C.升高溫度,增大體積,有利于平衡向正反應方向移動
D.降低溫度,體積不變,F(xiàn)2的轉(zhuǎn)化率增大
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河南洛陽高級中學高二上9月月考化學試卷(解析版) 題型:實驗題
(共18分)某探究小組用KMnO4酸性溶液與H2C2O4溶液反應過程中溶液紫色消失快慢的方法,研究影響反應速率的因素。實驗條件作如下限定:
所用酸性KMnO4溶液的濃度可選擇0.010 mol·L-1、 0.0010 mol·L-1, 催化劑的用量可選擇0.5 g、0 g,實驗溫度可選擇298 K、323 K。每次實驗KMnO4酸性溶液的用量均為4 mL、H2C2O4溶液(0.10 mol·L-1)的用量均為2 mL。
(1)已知草酸溶液中各種微粒存在形式的分布曲線圖如下,請寫出KMnO4酸性溶液與H2C2O4溶液反應的離子方程式 。
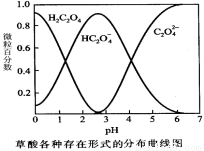
(2)請完成以下實驗設計表,并在實驗目的一欄中填出對應的實驗編號:
實驗編號 | T/K | 催化劑的用量 / g | 酸性KMnO4溶液的濃度/mol·L-1 | 實驗目的 |
① | 298 | 0.5 | 0.010 | a.實驗①和②探究酸性KMnO4溶液的濃度對該反應速率的影響; b.實驗①和 探究溫度對反應速率的影響; c.實驗①和 探究催化劑對反應速率的影響。 |
② | ||||
③ | 0.010 | |||
④ |
(3)某同學對實驗①和②分別進行了三次實驗,測得以下實驗數(shù)據(jù)(從混合振蕩均勻開始計時):
實驗編號 | 溶液褪色所需時間 t / min | ||
第1次 | 第2次 | 第3次 | |
Ⅰ | 14.0 | 13.0 | 11.0 |
Ⅱ | 6.5 | 6.7 | 6.8 |
① 實驗Ⅱ中用KMnO4的濃度變化來表示的平均反應速率為 (忽略混合前后溶液的體積變化)。
②該同學分析上述數(shù)據(jù)后得出“當其他條件相同的情況下,酸性KMnO4溶液的濃度越小,所需要的時間就越短,亦即其反應速率越快”的結論,你認為是否正確 (填“是”或“否”)。他認為不用經(jīng)過計算,直接根據(jù)表中褪色時間的長短就可以判斷濃度大小與反應速率的關系,你認為是否可行 (填“是”或“否”),若不可行(若認為可行則不填),請設計可以直接通過觀察褪色時間的長短來判斷的改進方案:
(4)該反應的催化劑選擇MnCl2還是MnSO4并簡述選擇的理由:
(5)化學催化劑有很多,在生產(chǎn)和科技領域起到重大作用。探究小組又利用乙裝置探究MnO2對H2O2分解的催化效果。將50 mL H2O2一次性加入盛有0.10 mol MnO2粉末的燒瓶中,測得標準狀況下由量氣管讀出氣體的體積[V(量氣管)/mL]和時間(t/min)的關系如下圖所示。
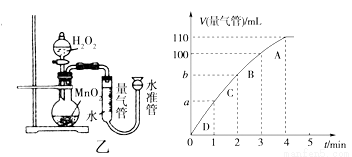
①實驗時放出氣體的總體積是____ ____mL。
②b______ __(填“大于”“小于”或“等于”)90 mL。
查看答案和解析>>
科目:高中化學 來源:2016屆湖南省常德市高三上學期第三次月考化學試卷(解析版) 題型:選擇題
下列兩種方案制備氫氧化鋁:
已知所用的稀鹽酸與NaOH溶液均為3mol/L.圖是向X溶液與Y溶液中分別加入NaOH溶液或稀鹽酸時產(chǎn)生沉淀的質(zhì)量與加入溶液體積之間的關系.相關說法正確的是
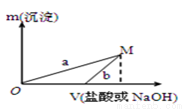
A.a(chǎn)曲線表示的是向Y溶液中加入NaOH溶液
B.方案二比方案一生成更多的氣體
C.在M點時,兩種方案中所得溶液的溶質(zhì)質(zhì)量分數(shù)相同
D.M點以后,a、b兩條曲線將重合為一條
查看答案和解析>>
科目:高中化學 來源:2016屆浙江省高三上學期10月月考化學試卷(解析版) 題型:推斷題
Ⅰ.A、B、C、D、E、F是短周期元素組成的中學常見的物質(zhì),它們的轉(zhuǎn)化關系如圖所示(部分反應條件略去):
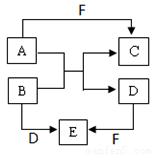
(1)若所有轉(zhuǎn)化都是非氧化還原反應,B、D、E含有同種金屬元素,F(xiàn)為強堿(部分產(chǎn)物略去)則B+D→E的離子方程式為________________,C為同周期元素構成的1:1型化合物,則C的電子式為___________________。
(2)若A、D、F為單質(zhì),B、C、E為化合物,B為兩種非金屬元素所組成的化合物,則E的化學式為___________,A+B→C+D的化學方程式為______________________。
Ⅱ.亞氯酸鈉(NaClO2)是一種重要的消毒劑,主要用于水、砂糖、油脂的漂白與殺菌。以下是制取來氯酸鈉的工藝流程:
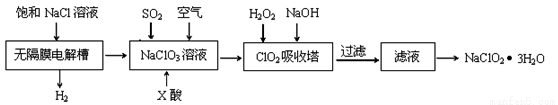
已知:①ClO2氣體只能保持在濃度較低狀態(tài)下以防止爆炸性分解,且需現(xiàn)合成現(xiàn)用 ②ClO2氣體在中性和堿性溶液中不能穩(wěn)定存在。
(1)反應生成ClO2氣體需要X酸酸化,X酸可以為_______________。
A.鹽酸 B.稀硫酸 C.硝酸 D.H2C2O4溶液
(2)吸收塔內(nèi)的溫度不能過高的原因為__________________________。
(3)ClO2被S ClO2被S2-還原為ClO2-、Cl-轉(zhuǎn)化率與pH關系如圖。
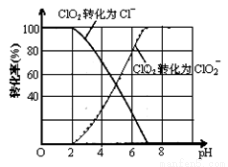
寫出pH≤2時ClO2與S2- 反應的離子方程式:_______________。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年內(nèi)蒙古巴彥淖爾高一上10月月考化學試卷(解析版) 題型:選擇題
將50ml 0.5 mol/LNaOH溶液加水稀釋到500ml,稀釋后溶液中NaOH的物質(zhì)的量濃度為
A.0.5mol/L B.0.05mol/L C.0.04 mol/L D.0.03 mol/L
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧實驗中學高一上10月階段測化學試卷(解析版) 題型:選擇題
0.1L某溶液含有0.1mol KCl和0.1mol CaCl2,此溶液中Cl﹣的物質(zhì)的量濃度是
A.3mol•L﹣1 B.0.2mol•L﹣1 C.0.3mol•L﹣1 D.0.1mol•L﹣1
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com