
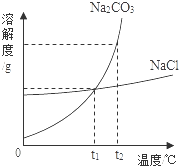
 我國化學家侯德榜創立的侯氏制堿法,就是以海水曬鹽得到的氯化鈉為原料,制得純堿碳酸鈉,碳酸鈉和氯化鈉的溶解度曲線如圖所示,試回答下列問題:
我國化學家侯德榜創立的侯氏制堿法,就是以海水曬鹽得到的氯化鈉為原料,制得純堿碳酸鈉,碳酸鈉和氯化鈉的溶解度曲線如圖所示,試回答下列問題:分析 (1)根據曲線t2℃時,碳酸鈉對應點大于氯化鈉的溶解度對應的點;
(2)降溫結晶適用于溶解度隨溫度變化大而且是隨溫度降低而降低的溶質,而碳酸鈉的溶解度隨溫度的變化比較大;
(3)根據酸堿度的測定用PH試紙,來測定;
(4)蒸發結晶,適用溶解度隨溫度的變化不大的物質分離;
(5)根據碳酸氫鈉用于焙制糕點的發酵粉;治療胃酸過或生產汽水飲料等.
解答 解:(1)由碳酸鈉和氯化鈉的溶解度曲線可知,在t2℃時,氯化鈉的溶解度小于碳酸鈉的溶解度,故答案為:小于;
(2)由碳酸鈉和氯化鈉的溶解度曲線可知,碳酸鈉的溶解度受溫度的影響較大,氯化鈉的溶解度受溫度的影響不大,從天然堿中分離出較純凈的純堿晶體應采用降溫結晶的方法,故答案為:降溫結晶;
(3)在實驗室中,若要測定鹽湖水的酸堿性強弱,可以使用PH試紙測定,故答案為:PH試紙;
(4)由于氯化鈉的溶解度受溫度變化影響不大,氯化鈉通常采取海水曬鹽的方法獲得,故答案為:氯化鈉的溶解度隨溫度的變化不大;
(5)碳酸氫鈉在生活中有廣泛的用途,例如:焙制糕點的發酵粉;治療胃酸過或生產汽水飲料等,故答案為:焙制糕點的發酵粉;治療胃酸過或生產汽水飲料等.
點評 本題考查了學生根據所給的問題情景、圖表信息,結合所學溶解度、方程式計算等相關知識和技能,細心地探究、推理,按照題目要求進行認真分析解決問題的能力.


 走進文言文系列答案
走進文言文系列答案科目:高中化學 來源: 題型:選擇題
| A. | 三氯化硼液態時能導電而固態時不導電 | |
| B. | 三氯化硼加到水中使溶液的pH升高 | |
| C. | 三氯化硼分子呈正三角形,屬非極性分子 | |
| D. | 分子中所有原子都滿足最外層8電子穩定結構 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溶液呈堿性的原因是:C6H5O-+H2O=C6H5OH+OH- | |
| B. | 與少量CO2反應的離子方程式為:2C6H5O-+CO2+H2O=2C6H5OH+CO32- | |
| C. | 25℃時,該溶液中由水電離出的氫離子濃度大于1×10-7mol•L-1 | |
| D. | 該溶液中可能大量存在:K+、SO42-、Cl2、H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=1的硝酸溶液中,H+的數目為NA | |
| B. | 78g苯含有C═C雙鍵的數目為3NA | |
| C. | 常溫常壓下,14g由N2與CO組成的混合氣體含有的原子數目為NA | |
| D. | 標準狀況下,6.72LNO2與水充分反應轉移的電子數目為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子結構示意圖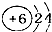 ,可以表示12C,也表示14C ,可以表示12C,也表示14C | |
| B. | 比例模型 可以表示水分子,也可以表示二氧化碳分子 可以表示水分子,也可以表示二氧化碳分子 | |
| C. | 結構示意圖為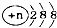 的陰離子都不能破壞水的電離平衡 的陰離子都不能破壞水的電離平衡 | |
| D. | 電子式 可以表示羥基,也可以表示氫氧根離子 可以表示羥基,也可以表示氫氧根離子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4 | B. | 8 | C. | 12 | D. | 16 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| X | Y | ||
| W | Z | ||
| T |
| A. | X、Y、Z三種元素最低價氫化物的沸點依次升高 | |
| B. | 由X、Y和氫三種元素形成的化合物中只有共價鍵 | |
| C. | 原子得電子能力強弱:W<X<Y<Z | |
| D. | T元素的單質可能具有半導體的特性,T與Z元素可形成化合物TZ4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若向①中加適量水,溶液中$\frac{c(C{l}^{-})}{c(N{H}_{4}^{+})}$的值減小 | |
| B. | 若向②中加適量水,水的電離平衡正向移動 | |
| C. | 若將①和②均稀釋100倍,①的pH變化更大 | |
| D. | 若將①和②混合,所得溶液的pH=7,則溶液中的c(NH3.H2O)>c(Na+) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com