
【題目】硫單質及其化合物在工農業生產中有著重要的應用。請回答下列問題:
(1)一種煤炭脫硫技術可以把硫元素以CaSO4的形成固定下來,但產生的CO又會與CaSO4發生化學反應,相關的熱化學方程式如下:
①CaSO4(s)+CO(g)![]() CaO(s)+SO2(g)+CO2(g)△H = +210.5kJmol-1
CaO(s)+SO2(g)+CO2(g)△H = +210.5kJmol-1
②1/4CaSO4(s)+CO(g)![]() 1/4CaS(s)+CO2(g) △H = - 47.3kJmol-1
1/4CaS(s)+CO2(g) △H = - 47.3kJmol-1
反應CaO(s)+3CO(g)+SO2(g) ![]() CaS(s)+3CO2(g) △H= kJmol-1;
CaS(s)+3CO2(g) △H= kJmol-1;
平衡常數K的表達式為 。
(2)圖1為在密閉容器中H2S氣體分解生成H2和S2(g)的平衡轉化率與溫度、壓強的關系。
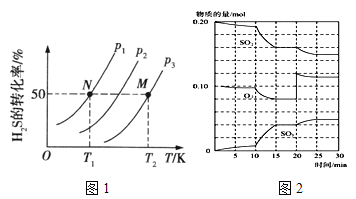
圖1中壓強p1、p2、p3的大小順序為 ,理由是 ;該反應平衡常數的大小關系為K(T1) K(T2) (填“>”、“<”或“=”),理由是 。
(3)在一定條件下,二氧化硫和氧氣發生如下反應:2SO2(g)+O2(g) ![]() 2SO3(g) △H<0
2SO3(g) △H<0
①600℃時,在一密閉容器中,將二氧化硫和氧氣混合,反應過程中SO2、O2、SO3物質的量變化如圖2,反應處于平衡狀態的時間段是 。
②據圖2判斷,反應進行至20min時,曲線發生變化的原因是 (用文字表達);10min到15min的曲線變化的原因可能是 (填寫編號)。
A.加了催化劑 B.縮小容器體積
C.降低溫度 D.增加SO3的物質的量
(4)煙氣中的SO2可用某濃度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,該溶液中c(Na+)= (用含硫微粒濃度的代數式表示)。
【答案】(1)-399.7 ![]()
(2)P1<P2<P3 增大壓強,化學平衡逆向移動,H2S的轉化率減小;<,升高溫度,H2S的轉化率增大,化學平衡正向移動,K增大
①15~20min和25~30 min;②增加了O2的量, A B
2c(SO32-)+c(HSO3-)或c(Na+)=2c(SO32-)+c(HSO3-) (2分)
【解析】
試題分析:(1)利用蓋斯定律將②×4-①可得CaO(s)+3CO(g)+SO2(g)CaS(s)+3CO2(g)△H=4×(-47.3kJmol-1)-(210.5kJmol-1)=-399.7kJmol-1;平衡常數K的表達式為:![]()
(2)H2S氣體分解生產H2和S2(g)的反應為2H2S![]() 2H2+S2,反應前后氣體體積增大,同溫度下,壓強越大,平衡逆向進行,H2S轉化率減小,則P1<P2<P3,溫度升高,H2S的轉化率增大,說明正反應為吸熱反應,升溫平衡正向進行,平衡常數增大,K(T1)<K(T2);(3)①反應混合物各物質的物質的量不變化,說明反應處于平衡狀態,由圖可知在15-20min和25-30min出現平臺,各組分的物質的量不變,反應處于平衡狀態;②由圖可知,反應進行至20min時,平衡向正反應移動,瞬間只有氧氣的濃度增大,應是增大了氧氣的濃度.由圖可知,反應向正反應進行,10min到15min反應混合物單位時間內的變化量增大,說明反應速率增大,10min改變瞬間,各物質的物質的量不變.a.加了催化劑,增大反應速率,a正確;b.縮小容器體積,增大壓強,增大反應速率,b正確;c.降低溫度反應速率降低,c錯誤;d.10min改變瞬間,各物質的物質的量不變,不是增加SO2的物質的量,d錯誤;故答案為:增大氧氣的濃度;ab;
2H2+S2,反應前后氣體體積增大,同溫度下,壓強越大,平衡逆向進行,H2S轉化率減小,則P1<P2<P3,溫度升高,H2S的轉化率增大,說明正反應為吸熱反應,升溫平衡正向進行,平衡常數增大,K(T1)<K(T2);(3)①反應混合物各物質的物質的量不變化,說明反應處于平衡狀態,由圖可知在15-20min和25-30min出現平臺,各組分的物質的量不變,反應處于平衡狀態;②由圖可知,反應進行至20min時,平衡向正反應移動,瞬間只有氧氣的濃度增大,應是增大了氧氣的濃度.由圖可知,反應向正反應進行,10min到15min反應混合物單位時間內的變化量增大,說明反應速率增大,10min改變瞬間,各物質的物質的量不變.a.加了催化劑,增大反應速率,a正確;b.縮小容器體積,增大壓強,增大反應速率,b正確;c.降低溫度反應速率降低,c錯誤;d.10min改變瞬間,各物質的物質的量不變,不是增加SO2的物質的量,d錯誤;故答案為:增大氧氣的濃度;ab;
(4)煙氣中的SO2可用某濃度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,依據溶液中電荷守恒分析,c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-),c(H+)=c(OH-),得到(Na+)=2c(SO32-)+c(HSO3-)。


科目:高中化學 來源: 題型:
【題目】【化學——選修3物質結構與性質】
原子序數依次增大的四種元素A、B、C、D依次處于第一至第四周期,自然界中存在多種A的化合物,B原子核外電子有6種不同的運動狀態,B與C可形成正四面體形分子,D的基態原子的最外能層只有一個電子,其他能層均已充滿電子。
請回答下列問題:
(1)這四種元素中電負性最大的元素,其基態原子的價電子排布圖為 。
(2)C所在主族的四種元素分別與A形成的化合物,沸點由高到低的順序是 (填化學式),呈現如此遞變規律的原因是 。
(3)B元素可形成多種單質,一種晶體結構如圖一所示,其原子的雜化類型為 ,另一種的晶胞如圖二所示,用最簡式表示該晶胞的空間利用率 。
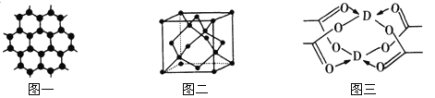
(4)D元素形成的單質,其晶胞內D原子的配位數為 ,D的醋酸鹽晶體局部結構如圖三,該晶體中含有的化學鍵是 (填選項序號)。
①極性鍵 ②非極性鍵 ③配位鍵 ④金屬鍵
(5)D元素形成的單質,既不溶于氨水也不溶于雙氧水,但溶于兩者的混合溶液。寫出該反應的離子方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫能是一種極具發展潛力的清潔能源,硫碘循環制氫主要的熱化學方程式為:
Ⅰ.SO2(g)+2H2O(l)+I2(g)=H2SO4 (l)+2HI(g) △H=35.9 kJ/mol
Ⅱ.2H2SO4(l)=2SO2(g)+O2(g)+2H2O(l) △H=470kJ/mol
Ⅲ.2HI(g)=H2(g)+I2(g) △H=14.9kJ/mol
(1)反應2H2(g)+ O2(g)=2H2O(l)的△H= mol·L-1。
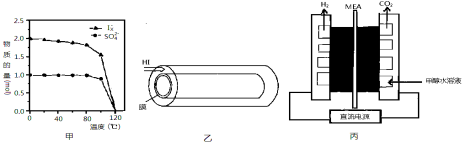
(2)反應Ⅰ在液相中發生稱為bensun反應,向水中加入1mol SO2和3mol I2,在不同溫度下恰好完全反應生成的n(SO42-)和n(Ix-)的變化見圖甲。
①Ix-中x= 。②溫度達到120℃時,該反應不發生的原因是 。
(3)反應Ⅲ是在圖乙中進行,其中的高分子膜只允許產物通過,高分子膜能使反應程度 ___ (填“增大”、“減小”或“不變”),在該裝置中為了進一步增大達平衡時HI的分解率;不考慮溫度的影響,還可以采取的措施為 。
(4)圖丙是一種制備H2的方法,裝置中的MEA為允許質子通過的電解質膜。
①寫出陽極電極的反應式: 。
②電解產生的氫氣可以用鎂鋁合金(Mg17Al12)來儲存,合金吸氫后得到僅含一種金屬的氫化物(其中氫的質量分數為0.077)和一種金屬單質,該反應的化學方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】TiO2和TiCl4都是鈦的重要化合物,某化學興趣小組在實驗室對兩者的制備及性質進行探究。
Ⅰ.制備TiCl4
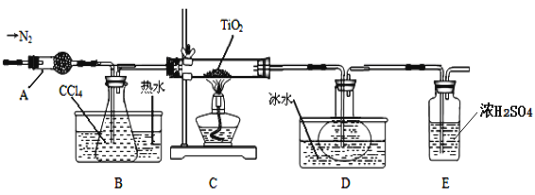
實驗室利用反應TiO2 (s)+CCl4(g)![]() TiCl4(g)+CO2(g),在無水無氧條件下制備TiCl4,裝置圖和有關信息如下:
TiCl4(g)+CO2(g),在無水無氧條件下制備TiCl4,裝置圖和有關信息如下:
物質 | 熔點/℃ | 沸點/℃ | 其他 |
CCl4 | —23 | 76 | 與TiCl4互溶 |
TiCl4 | —25 | 136 | 遇潮濕空氣產生白霧 |
請回答下列問題:
(1)儀器A的名稱是 。
(2)實驗開始前后的操作包括:①檢查裝置氣密性,②組裝儀器,③通N2一段時間,④加裝藥品,⑤點燃
酒精燈⑥停止通N2⑦停止加熱。正確的操作順序是__________________________。實驗結束后欲分離D中的液態混合物,所采用操作的名稱是 。
(3)裝置E能否 (填“能”或“不能”)換成裝置A,理由是 。
(4)TiCl4是制取航天航空工業材料——鈦合金的重要原料。某鈦合金的元素還有Al和Si等,已知在常溫下,鈦是一種耐強酸強堿的金屬,請設計實驗檢驗其中的Si元素。 。
Ⅱ.制備TiO2及測定TiO2的質量分數:
在TiCl4中加水、加熱,水解得到沉淀TiO2·xH2O,經過濾、水洗,再烘干、焙燒除去水分得到粉體TiO2。
(5)寫出生成TiO2·xH2O的化學方程式 。
(6)檢驗沉淀是否洗滌干凈的方法是___________________________________________。
(7) 一定條件下,將TiO2溶解并還原為Ti3+,用NH4Fe(SO4)2標準溶液滴定Ti3+至全部生成Ti4+。滴定分析時,稱取上述TiO2試樣0.2g,消耗0.1 mol·L-1 NH4Fe(SO4)2標準溶液20mL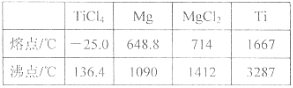 。
。
①配制NH4Fe(SO4)2標準溶液時,加入一定量H2SO4的目的是: 。
②該滴定操作所用到的指示劑是 。
③則TiO2質量分數為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組以CoCl2·6H2O、NH4Cl、H2O2、液氨、氯化銨為原料,在活性炭催化下合成了橙黃色晶體X。為測定其組成,進行如下實驗。
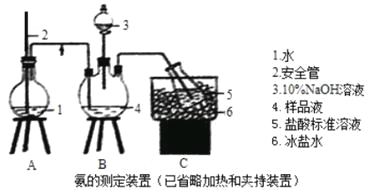
①氨的測定:精確稱取wgX,加適量水溶解,注入如圖所示的三頸瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸氣,將樣品溶液中的氨全部蒸出,用V1mLc1mol·L—1的鹽酸溶液吸收。蒸氨結束后取下接收瓶,用c2mol·L—1NaOH標準溶液滴定過剩的HCl,到終點時消耗V2mLNaOH溶液。
②氯的測定:準確稱取樣品X,配成溶液后用AgNO3標準溶液滴定,K2CrO4溶液為指示劑,至出現磚紅色沉淀不再消失為終點(Ag2CrO4為磚紅色)。
回答下列問題:
(1)裝置中安全管的作用原理是 。
(2)用NaOH標準溶液滴定過剩的HCl時,應使用 式滴定管,可使用的指示劑為 。
(3)樣品中氨的質量分數表達式為 。
(4)測定氨前應該對裝置進行氣密性檢驗,若氣密性不好測定結果將 (填“偏高”或“偏低”)。
(5)測定氯的過程中,使用棕色滴定管的原因是 ;滴定終點時,若溶液中c(Ag+)=2.0×10—5mol·L—1,c(CrO42—)為 mol·L—1。(已知:Ksp(Ag2CrO4)=1.12×10—12)
(6)經測定,樣品X中鈷、氨、氯的物質的量之比為1:6:3,鈷的化合價為 ,制備X的化學方程式為 ;X的制備過程中溫度不能過高的原因是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)CaC2中C22-與O22+互為等電子體,O22+的電子式可表示為 ;1 mol O22+中含有的π鍵數目為____________________。
(2)Fe2(SO4)3晶體中鐵離子的核外電子排布式為 。
(3)乙醇與乙醛的相對分子質量相差不大,但乙醇的沸點(78.5℃)卻比乙醛的沸點(20.8℃)高出許多,其原因是 。
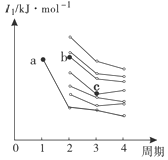
(4)右圖是部分主族元素第一電離能梯度圖,圖中a點對應的元素為氫,b、c兩點對應的元素分別為 、 (填元素符號)。
(5)亞硝酸的酸性強于次氯酸的原因為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分。表中所列的字母分別代表某一種化學元素。
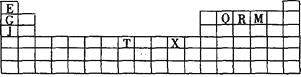

(1)寫出基態T3+的核外電子排布式: ;T在周期表中所在分區為 。
(2)Q、R、M的第一電離能由大到小的順序是 (用元素符號表示),原因 。
(3)下列有關上述元素的說法正確的是 。
A.J比X活潑,所以J可以在溶液中置換出X |
B.將J2M2溶于水,要破壞離子鍵和共價鍵 |
C.RE3沸點高于QE4,主要是因為前者相對分子質量較大 |
D.一個Q2E4分子中含有五個δ鍵和一個π鍵 |
(4)G2O的熔點比J2O的 (填“高”或“低”) ,其原因是 。
(5) G與R單質直接化合生成一種離子化合物G3R。該晶體具有類似石墨的層狀結構。每層中,G原子構成平面六邊形,每個六邊形的中心有一個R原子。層與層之間還夾雜一定數量的原子。請問這些夾雜的原子應該是 (填G或R的元素符號)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將適量AgBr固體溶在水中,溶液中存在AgBr(s)![]() Ag+(aq)+Br-(aq)。則下列說法正確的是( )
Ag+(aq)+Br-(aq)。則下列說法正確的是( )
A.向此體系中滴加足量濃NaCl溶液,發現沉淀轉化為白色,說明Ksp(AgCl)<Ksp(AgBr)
B.某溶液中c(Ag+)·c(Br-)=Ksp(AgBr),說明此時c(Ag+)=c(Br-)
C.向此體系中加入少量AgBr固體,平衡正向移動,當再次平衡時c(Ag+)、c(Br-)增大
D.此體系中一定存在c(Ag+)=c(Br-)=[Ksp(AgBr)]1/2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表給出五種短周期元素的相關信息。
元素 | 相關信息 |
A | 常溫、常壓下,其單質是最輕的氣體,它將成為備受青睞的清潔燃料 |
B | 工業上通過分離液態空氣獲得其單質,其某種同素異形體是保護地球地表環境的重要屏障 |
C | 植物生長三要素之一,它能形成多種氧化物,某些氧化物會造成光化學污染 |
D | 室溫下其單質為淡黃色粉末狀固體,加熱易熔化。該單質在氧氣中燃燒,發出明亮的藍紫色火焰 |
E | 常溫下其單質為黃綠色氣體,其單質水溶液有漂白、殺菌作用 |
請按要求回答下列問題:
(1)D元素核外電子排布 ;
(2)A、B兩元素形成的含有非極性鍵的化合物的結構式 ;A、B兩元素形成的具有相同電子數的離子有(填化學式):______________、_____________。
(3)C與A形成的某一化合物能和C與B形成的另一無色化合物(這兩種化合物分子中原子個數比皆為1∶2)一起用作火箭助推劑,兩者發生反應生成無毒物質,寫出上述化學反應方程式: 。
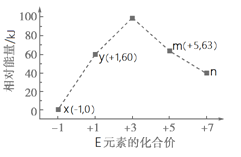
(4)一定條件下,在水溶液中1 mol E-、EO(x=1,2,3,4)的能量(kJ)相對大小如右圖所示。n是 (填離子符號)。離子反應y→x+m的熱化學方程式為 。
(5)Na2DB3水溶液中各離子濃度的大小順序是 (填離子符號)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com