
【題目】氫能是一種極具發展潛力的清潔能源,硫碘循環制氫主要的熱化學方程式為:
Ⅰ.SO2(g)+2H2O(l)+I2(g)=H2SO4 (l)+2HI(g) △H=35.9 kJ/mol
Ⅱ.2H2SO4(l)=2SO2(g)+O2(g)+2H2O(l) △H=470kJ/mol
Ⅲ.2HI(g)=H2(g)+I2(g) △H=14.9kJ/mol
(1)反應2H2(g)+ O2(g)=2H2O(l)的△H= mol·L-1。
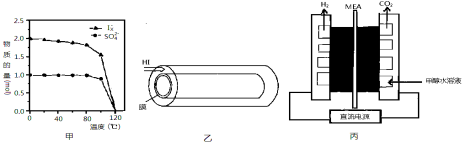
(2)反應Ⅰ在液相中發生稱為bensun反應,向水中加入1mol SO2和3mol I2,在不同溫度下恰好完全反應生成的n(SO42-)和n(Ix-)的變化見圖甲。
①Ix-中x= 。②溫度達到120℃時,該反應不發生的原因是 。
(3)反應Ⅲ是在圖乙中進行,其中的高分子膜只允許產物通過,高分子膜能使反應程度 ___ (填“增大”、“減小”或“不變”),在該裝置中為了進一步增大達平衡時HI的分解率;不考慮溫度的影響,還可以采取的措施為 。
(4)圖丙是一種制備H2的方法,裝置中的MEA為允許質子通過的電解質膜。
①寫出陽極電極的反應式: 。
②電解產生的氫氣可以用鎂鋁合金(Mg17Al12)來儲存,合金吸氫后得到僅含一種金屬的氫化物(其中氫的質量分數為0.077)和一種金屬單質,該反應的化學方程式為 。
【答案】(1)-571.6
(2)①3 ②此溫度下碘單質、水、二氧化硫均為氣態,氣相中不發生反應
(3)增大 向裝置中通入氮氣(或其它“惰性”氣體)吹出產物
(4)①CH3OH + H2O-6e-=CO2↑+6H+。② Mg17Al12+17H2=17MgH2+12Al
【解析】
試題分析:(1)根據蓋斯定律,-(Ⅲ+Ⅱ+I)×2可得到反應2H2(g)+ O2(g)=2H2O(l),則△H=-(14.9+470+35.9)×2mol·L-1= -571.6mol·L-1;
(2)①向水中加入1mol SO2和3mol I2,產物由圖甲可知n(SO42-):n(Ix-)=1:2,結合原子守恒可得x=3; ②溫度達到120℃時,該反應不發生的原因是在此溫度下,碘單質、水、二氧化硫均為氣態,氣相中不發生反應;
(3)反應Ⅲ是在圖乙中進行,其中的高分子膜只允許產物通過,結合平衡移動原理,減小生成物可促進平衡正向移動,故此高分子膜能使反應程度增大,在該裝置中為了進一步增大達平衡時HI的分解率;除升高溫度外,還可以采取的措施為向裝置中通入氮氣(或其它“惰性”氣體)吹出產物;
(4) ①電解時陽極發生氧化反應,產物為CO2,電極的反應式為CH3OH + H2O-6e-=CO2↑+6H+;
②Mg和Al形成的氫化物可能分別為MgH2、AlH3,其中MgH2中氫元素的質量分數為0.077,AlH3中氫元素的質量分數為0.1,故產物為MgH2,該反應的化學方程式為Mg17Al12+17H2=17MgH2+12Al。


科目:高中化學 來源: 題型:
【題目】【化學—選修5:有機化學基礎】鹽酸普魯卡因(![]() )是一種局部麻醉劑,麻醉作用較快、較強,毒性較低,其合成路線如下:
)是一種局部麻醉劑,麻醉作用較快、較強,毒性較低,其合成路線如下:
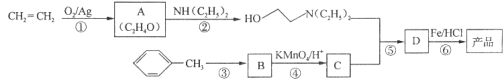
已知:①![]()
②![]()
③
請回答以下問題:
(1)A的核磁共振氫譜只有一個峰,則A的結構簡式為____________________。
(2)C的結構簡式為__________,C中含有的含氧官能團的名稱為__________。
(3)合成路線中屬于氧化反應的有_________(填序號),反應③的反應類型為_______________。
(4)反應⑤的化學反應方程式為______________________________________________。
(5)B的某種同系物E,相對分子質量比B大28,其中—NO2與苯環直接相連,則E的結構簡式為____________________(任寫一種)。
(6)符合下列條件的E的同分異構體的數目有__________種。
①結構中含有一個“—NH2”與一個“—COOH” ②苯環上有三個各不相同的取代基
(7)苯丙氨酸(![]() )是人體必需的氨基酸之一,寫出其發生縮聚反應的化學方程式____________________________________________________________。
)是人體必需的氨基酸之一,寫出其發生縮聚反應的化學方程式____________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[化學——選修3:物質結構與性質]太陽能電池板材料除單晶硅外,還有銅、銦、鎵、硒等化學物質。
(1)基態硅原子的價電子排布圖: 。
(2)硒和硫同為VIA族元素,與其相鄰的元素有砷和溴,則三種元素的第二電離能由小到大的順序為 。(用I2X表示)
(3)氣態SeO3分子的雜化類型為 ,與SeO3互為等電子體的一種陰離子為 (填化學式)。
(4)膽礬CuSO4·5H2O可寫成[Cu(H2O) 4]SO4 ·H2O,其結構示意圖如下:
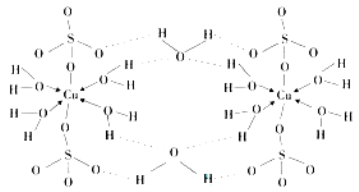
膽礬中含有的粒子間作用力是 (填序號)。
A.離子鍵 B.極性鍵 C.金屬鍵 D.配位鍵 E.氫鍵 F.非極性鍵
(5)在硫酸銅溶液中加入過量KCN,生成配合物K 2[Cu(CN)4],該配合物屬于 晶體,已知CN-與N2為等電子體,指出1molCN-中![]() 鍵的數目為 。
鍵的數目為 。
(6)一種銅金合金晶體具有面心立方最密堆積結構,在晶胞中金原子位于頂點,銅原子位于面心,則該合金中銅原子(Cu)與金原子(Au)個數比為 ;若該晶體的晶胞棱長為a nm,則該合金密度為 g/cm3。(列出計算式,不要求計算結果,阿伏加德羅常數的值為NA)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近年來,科學家合成了一系列具有獨特化學特性的氫鋁化合物(AlH3)n,常用作還原劑。已知最簡單的氫鋁化合物的化學式為Al2H6,它的熔點為150℃且熔融狀態不能導電,燃燒時放出大量的熱量。Al2H6的球棍模型如圖所示。下列說法錯誤的是
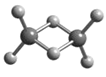
A. Al2H6中Al為-3價,H為+1價
B. Al2H6中含有離子鍵和極性共價鍵
C. Al2H6在固態時所形成的晶體是分子晶體
D. Al2H6在空氣中完全燃燒,產物為氧化鋁和水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】異苯丙醛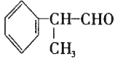 在工業上有重要用途,其合成流程如下:
在工業上有重要用途,其合成流程如下:

(1)異苯丙醛被酸性高錳酸鉀氧化后所得有機物的結構簡式是____________。
(2)在合成流程上②的反應類型是____________,反應④發生的條件是____________,
(3)反應⑤的化學方程式為____________。
(4)異苯丙醛發生銀鏡反應的化學方程式為__________。
(5)D物質與有機物X在一定條件下可生成一種相對分子質量為178的酯類物質,則X的名稱是____________。D物質有多種同分異構體,其中滿足苯環上有兩個取代基,且能使FeCl3溶液顯紫色的同分異構體有____________種。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度時,在2L容器中X.、Y、Z三種物質的物質的量隨時間變化曲線如右圖所示,由圖中數據分析,
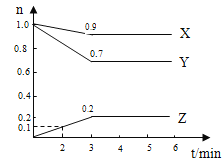
(1)該反應的化學方程式為
(2)反應開始至2min、Z的平均反應速率為 。
(3)平衡時X的體積分數為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)在汽車上安裝三效催化轉化器,可使汽車尾氣中的主要污染物(CO、NOx、碳氫化合物)進行相互反應,生成無毒物質,減少汽車尾氣污染。某研究性學習小組探究某種催化劑在不同空燃比(空氣與燃油氣的質量比)條件下對汽車尾氣的催化效果。在一定條件下,測得尾氣中的主要污染物的轉化率與空燃比的關系如右圖所示。空燃比約為 時,催化劑對汽車尾氣的催化效果最好。(填a、b、c、d)

(2)工業上也常用NaOH溶液吸收法處理NOx ,已知:NO + NO2 + 2NaOH= 2NaNO2 + H2O(I)
2NO2 + 2NaOH =NaNO2 + NaNO3 + H2O(II)
現有2 240 mL(標準狀況)NO 和NO2的混合氣體溶于200 mL NaOH溶液中,恰好完全反應,并無氣體放出,則NaOH溶液物質的量濃度是 。
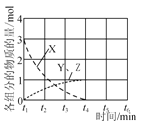
(3)NO直接催化分解(生成N2與O2)也是一種脫硝途徑。在不同條件下,NO的分解產物不同。在高壓下,NO在40 ℃下分解生成兩種化合物,體系中各組分物質的量隨時間變化曲線如圖所示。寫出Y和Z的化學式:__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫單質及其化合物在工農業生產中有著重要的應用。請回答下列問題:
(1)一種煤炭脫硫技術可以把硫元素以CaSO4的形成固定下來,但產生的CO又會與CaSO4發生化學反應,相關的熱化學方程式如下:
①CaSO4(s)+CO(g)![]() CaO(s)+SO2(g)+CO2(g)△H = +210.5kJmol-1
CaO(s)+SO2(g)+CO2(g)△H = +210.5kJmol-1
②1/4CaSO4(s)+CO(g)![]() 1/4CaS(s)+CO2(g) △H = - 47.3kJmol-1
1/4CaS(s)+CO2(g) △H = - 47.3kJmol-1
反應CaO(s)+3CO(g)+SO2(g) ![]() CaS(s)+3CO2(g) △H= kJmol-1;
CaS(s)+3CO2(g) △H= kJmol-1;
平衡常數K的表達式為 。
(2)圖1為在密閉容器中H2S氣體分解生成H2和S2(g)的平衡轉化率與溫度、壓強的關系。
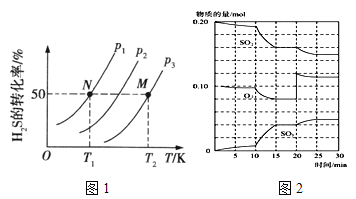
圖1中壓強p1、p2、p3的大小順序為 ,理由是 ;該反應平衡常數的大小關系為K(T1) K(T2) (填“>”、“<”或“=”),理由是 。
(3)在一定條件下,二氧化硫和氧氣發生如下反應:2SO2(g)+O2(g) ![]() 2SO3(g) △H<0
2SO3(g) △H<0
①600℃時,在一密閉容器中,將二氧化硫和氧氣混合,反應過程中SO2、O2、SO3物質的量變化如圖2,反應處于平衡狀態的時間段是 。
②據圖2判斷,反應進行至20min時,曲線發生變化的原因是 (用文字表達);10min到15min的曲線變化的原因可能是 (填寫編號)。
A.加了催化劑 B.縮小容器體積
C.降低溫度 D.增加SO3的物質的量
(4)煙氣中的SO2可用某濃度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,該溶液中c(Na+)= (用含硫微粒濃度的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】50ml0.50mol·L-1鹽酸與50mL0.55mol·L-1NaOH溶液在如下圖所示的裝置中進行中和反應。通過測定反應過程中放出的熱量可計算中和熱。回答下列問題:
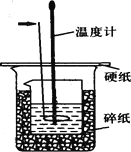
(1)箭頭所指儀器的名稱是 。作用是 。
(2)實驗所用的NaOH溶液體積與鹽酸相同,但濃度卻比鹽酸大的原因是 。
(3)用相同濃度和體積的醋酸代替HCl溶液進行上述實驗,放出的熱量會 。(填“偏大”“偏小”或“無影響”)。測得的△H會 (填“偏大”“偏小”或“無影響”)。
(4)上圖所示實驗裝置存在著一處錯誤,這處錯誤是 。
(5)實驗測得中和熱△H =" -" 57.3 kJ·mol–1若忽略能量的損失,請你計算出實驗前后溫度的差值△t (保留一位小數,水的比熱容c=4.18J/(g·℃)兩種溶液的密度近似取1g/ml )
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com