
| A. | 鎂片不用特殊方法保存 | |
| B. | 鍍鋅的鐵比鍍錫的鐵耐用 | |
| C. | 輪船水線以下的船殼上裝一定數量的鋅塊以保護船體 | |
| D. | 純鋅與稀硫酸反應時,滴入少量硫酸銅溶液后速率加快 |
分析 電化學往往專門指“電池的科學”,因此事實中只要是形成了原電池則能用電化學理論解釋.
A、Mg表面易形成致密的氧化物薄膜而阻止進一步的反應;
B、活潑性不同的兩種金屬遇到合適的電解質溶液能構成原電池,較活潑的金屬作負極,負極易失電子被腐蝕;
C、活潑性不同的兩種金屬遇到合適的電解質溶液能構成原電池,較活潑的金屬作負極,負極易失電子被腐蝕;
D、原電池原理可使反應速率加快;
解答 解:A、Mg表面易形成一層致密的氧化物薄膜而保護內層的鎂不再被氧化,所以鎂不用特殊方法保護,此現象與電化學知識無關,故A選;
B、鍍鋅鐵發生金屬被腐蝕現象時,因Zn比Fe活潑,Zn被腐蝕,鍍錫鐵破損后發生電化腐蝕,因Fe比Sn活潑,因而是鐵被腐蝕.所以,鍍鋅鐵比鍍錫鐵耐用.發生原電池反應而可用電化學知識解釋,故B不選;
C、輪船水線下的船殼裝上鋅塊后,可保護船殼在海水中不被腐蝕,因為Zn比Fe活潑,Zn與Fe構成原電池,在海水中鋅被腐蝕,從而保護船殼,發生原電池反應可用電化學知識解釋,故C不選;
D、滴入少量硫酸銅溶液后,鋅把銅置換出來形成原電池反應,故加快反應速率,可用原電池原理解釋,故D不選.
故選A.
點評 本題是對電化學知識的考查題,解題的關鍵是對相關的事實進行分析,只要是存在原電池的反應,便可用電化學理論解釋.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 能使溴水褪色,也能使高錳酸鉀酸性溶液褪色 | |
| B. | 在一定條件下與H2充分反應,生成1-丙醇 | |
| C. | 能發生銀鏡反應表現出氧化性 | |
| D. | 在一定條件下能被空氣氧化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化學反應既能實現物質的轉化、又能實現能量的轉化 | |
| B. | 分子是保持物質化學性質的一種粒子 | |
| C. | 儲存在物質中的化學能在化學反應前后是不變的 | |
| D. | 構成宏觀物質的微觀粒子之間的相互作用有多種形式,如離子鍵、共價鍵等 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 西南地區有較豐富的食鹽礦和電力資源,適合建設大型的氯堿工業.下圖是用惰性電極電解飽和食鹽水的原理示意圖,請回答下列問題:
西南地區有較豐富的食鹽礦和電力資源,適合建設大型的氯堿工業.下圖是用惰性電極電解飽和食鹽水的原理示意圖,請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯、乙烯都能被酸性KMnO4溶液氧化 | |
| B. | 煤的干餾和石油的分餾原理相同,都是化學變化 | |
| C. | 從苯的凱庫勒式看,分子中含有雙鍵,所以苯屬于烯烴 | |
| D. | 乙醇分子中的化學鍵如圖,在Cu等催化作用下和O2反應,①③處斷裂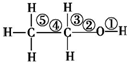 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳酸氫鈉溶液中加入過量的石灰水:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| B. | 氯化鋁溶液中加入過量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 用碳酸鈉溶液吸收足量二氧化硫:2CO32-+2SO2+H2O═2HCO3-+SO32- | |
| D. | 在FeBr2溶液中通入足量的Cl2氣體:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2+2H Br=2HCl+Br2 | B. | Cl2+FeI2=FeCl2+I2 | ||
| C. | 3Cl2+6FeI2=2FeCl3+4FeI3 | D. | 2Fe3++2I-=2Fe2++I2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com