
| A. | 將高溫水蒸氣通過熾熱的鐵粉,鐵粉變紅色 | |
| B. | 向Fe(OH)3膠體中滴加稀H2SO4,先出現沉淀,后沉淀溶解 | |
| C. | 向FeCl2溶液中加入幾滴KSCN溶液,溶液變為血紅色,則FeCl2溶液完全變質 | |
| D. | 鋁在空氣中耐腐蝕,所以鋁是不活潑金屬 |
分析 A.Fe與水蒸氣反應生成四氧化三鐵和氫氣;
B.膠體中滴加稀H2SO4,先發生膠體聚沉,后發生復分解反應;
C.如果FeCl2溶液變質,變質后的物質是FeCl3,Fe3+能和SCN-生成絡合物,使溶液呈現血紅色現象,但不能說明無FeCl2存在;
D.鋁是活潑金屬,空氣中耐腐蝕是表面形成了穩定的氧化物.
解答 解:A.Fe與水蒸氣反應生成四氧化三鐵和氫氣,則將高溫水蒸氣通過熾熱的鐵粉,鐵粉變黑色,故A錯誤;
B.膠體中滴加稀H2SO4,發生膠體聚沉,則向Fe(OH)3膠體中滴加稀H2SO4,先出現沉淀,后沉淀溶解(發生復分解反應),故B正確;
C.Fe3+能和SCN-生成絡合物,使溶液呈現血紅色現象明顯,這一反應是Fe3+的特征反應,所以用KSCN溶液檢驗FeCl2溶液是否變質,但不能說明無FeCl2存在,故C錯誤;
D.鋁是活潑金屬,在空氣中耐腐蝕是因為表面形成了一層氧化鋁保護膜,阻止反應進行,在空氣中耐腐蝕,故D錯誤;
故選B.
點評 本題考查物質的性質及元素化合物知識,為高頻考點,把握化學性質與反應為解答的關鍵,側重鐵、鋁知識的考查,注意物質的性質及檢驗,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 配制一定物質的量濃度的溶液時,容量瓶必須潔凈、干燥,不漏水 | |
| B. | 實驗室里需要480 mL 2.0 mol/L的氫氧化鈉溶液,配制該溶液時先稱量氫氧化鈉固體38.4 g,然后再按照溶解、冷卻、移液、定容、搖勻的步驟進行操作 | |
| C. | 用容量瓶配制溶液,定容時俯視刻度線,所配溶液的濃度偏大 | |
| D. | 實驗室配制500 mL 0.2 mol/L的硫酸亞鐵溶液,其操作是用天平稱量27.8 g綠礬,將其放入500 mL容量瓶,加水溶解、稀釋、定容、搖勻 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| A | B | C | D | |
| A | -- | 白色沉淀 | 無現象 | 無色氣體 |
| B | 白色沉淀 | -- | 白色沉淀 | 白色沉淀 |
| C | 無現象 | 白色沉淀 | -- | 無現象 |
| D | 無色氣體 | 白色沉淀 | 無現象 | -- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇在濃硫酸存在的情況下與乙酸發生酯化反應 | |
| B. | 乙醇與金屬鈉反應 | |
| C. | 乙醇在濃硫酸作用下的消去反應 | |
| D. | 乙醇與O2的催化氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蛋白質、淀粉、硝化纖維、油脂都屬于高分子化合物 | |
| B. | 聚丙烯能使溴水褪色 | |
| C. | 氯丁橡膠在空氣中燃燒只生成CO2和H2O | |
| D. | 利用木材作原料制得的纖維是人造纖維 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
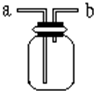 如圖所示是中學化學實驗中常見的裝置,它有多種用途.
如圖所示是中學化學實驗中常見的裝置,它有多種用途.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com