
【題目】設NA為阿伏加德羅常數,下列敘述中正確的是( )
A. 標準狀況下,3.36LCCl4中含有,7.5NA個原子
B. 常溫常壓下,32gO2和O3的混合物中含有的氧原子數約為1.204×1024
C. CO2和標準狀況下11.2LHCl具有相同的原子數
D. 1L0.1mol/L的CH3COOH溶液中,H+的數目為0.1NA
 黃岡小狀元解決問題天天練系列答案
黃岡小狀元解決問題天天練系列答案 三點一測快樂周計劃系列答案
三點一測快樂周計劃系列答案科目:高中化學 來源: 題型:
【題目】鎮痛藥物J的合成方法如下:

已知:

(1)B的名稱為_________________;F的結構簡式為_______________。
(2)C中含氧官能團名稱為_______________;②的反應類型為____________反應。
(3)③的化學方程式為_______________________________ 。
(4)有機物K分子組成比F少兩個氫原子,符合下列要求的K的同分異構體有________種。
A.遇FeCl3顯紫色 B.苯環上有三個取代基
(5)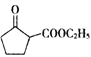 是一種重要的化工中間體。以環已醇(
是一種重要的化工中間體。以環已醇(![]() )和乙醇為起始原料,結合己知信息選擇必要的無機試劑,寫出
)和乙醇為起始原料,結合己知信息選擇必要的無機試劑,寫出 的合成路線____________________。(已知:RCH=CHR’
的合成路線____________________。(已知:RCH=CHR’![]() RCOOH+R’COOH,R、R'為烴基。用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)
RCOOH+R’COOH,R、R'為烴基。用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各實驗中需用濃鹽酸而不宜用稀鹽酸,請寫出反應的化學方程式并闡明理由。
(1)配制SnCl2溶液時,將SnCl2(s)溶于濃鹽酸后再加水稀釋______。
(2)加熱MnO2與濃鹽酸的混合物制取氯氣______。
(3)需用濃鹽酸與濃硝酸混合配制王水才能溶解金(生成HAuCl4)______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應原理在科研和生產中有廣泛應用,根據題意回答下列問題:
I工業上制備Na2S的反應原理如下
①Na2SO4(s)===Na2S(s)+2O2(g) △H1=+1011.0kJ·mol-1
②C(s)+O2(g)===CO2(g) △H2=-393.5kJ·mol-1
③2C(s)+O2(g)===2CO(g) △H3=-221.0kJ·mol-1
④Na2SO4(s)+4C(s)===Na2S(s)+4CO(g) △H4
(1)△H4=___________ kJ·mol-1。
(2)反應④能自發進行的條件是___________。
(3)工業上制備Na2S不用反應①,而用反應④的理由是_____________________________。
Ⅱ.在一定溫度下,向某恒容密閉容器中充入等物質的量的NO和CO發生反應:2NO(g)+2C0(g) ![]() 2CO2(g)+N2(B) △H=-748kJ/mo1。用氣體傳感器測得不同時間NO的濃度如下:
2CO2(g)+N2(B) △H=-748kJ/mo1。用氣體傳感器測得不同時間NO的濃度如下:
時間(s) | 0 | 10 | 20 | 30 | 40 | …… |
C(NO)/mol/L | 0.100 | 0.050 | 0.025 | 0.010 | 0.010 | …… |
(1)計算此溫度下該反應的K=______________________。
(2)達到平衡時,下列措施能提高NO轉化率的是___________(填序號)。
A.選用更有效的催化劑
B.降低反應體系的溫度
C.充入氬氣使容器內壓強增大
D.充入CO使容器內壓強增大
Ⅲ.工業上常用臭氧處理含NO2-的廢水。
(1)O3氧化NO2-可產生NO3-和O2,反應中每生成1mol的O2轉移___________mol電子。
(2)O3可由電解稀硝酸制得,原理如圖。圖中陰極為___________(填“A”或“B”),陽極(惰性電極)的電極反應式為____________________________________________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從廢鉛蓄電池鉛膏(含PbSO4、PbO2和Pb等)中回收鉛的一種工藝流程如下:

已知:濃硫酸不與PbO2反應,Ksp(PbCl2)=2.0×10-5,Ksp(PbSO4)=1.5×10-8,PbCl2(s)+2Cl-(aq)=PbCl42-(aq)。下列說法錯誤的是
A. 合理處理廢鉛蓄電池有利于資源再利用和防止重金屬污染
B. 步驟①中可用濃硫酸代替濃鹽酸
C. 步驟①、②、③中均涉及過濾操作
D. PbSO4(s)+2Cl-(aq)![]() PbCl2(s)+SO42-(aq)的平衡常數為7.5×10-4
PbCl2(s)+SO42-(aq)的平衡常數為7.5×10-4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某氯化鉀樣品中含有少量K2CO3、K2SO4和不溶于水的雜質。為了提純KCl,先 將樣品溶于適量水中,充分攪拌后過濾,再將濾液按如圖所示步驟進行操作。下列說法中正確的是( )

A. 試劑Ⅰ是Ba(NO3)2溶液,試劑Ⅲ是HCl溶液
B. ①②③的操作均為過濾
C. 步驟②中加入試劑Ⅱ的目的是除去Ba2+
D. Y和Z中都含有BaSO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生用0.200 0 mol·L-1的標準NaOH溶液滴定未知濃度的鹽酸,其操作如下:
①用蒸餾水洗滌堿式滴定管,并立即注入NaOH溶液至“0”刻度線以上;
②固定好滴定管并使滴定管尖嘴處充滿液體;
③調節液面至“0”或“0”刻度線以下,并記下讀數;
④移取20.00 mL待測液注入潔凈的還存有少量蒸餾水的錐形瓶中,并加入3滴酚酞溶液;
⑤用標準液滴定至終點,記下滴定管液面讀數。
請回答下列問題:
(1)以上步驟有錯誤的是______(填編號)。若測定結果偏高,其原因可能是________(填字母)。
A.配制標準溶液的固體NaOH中混有KOH雜質
B.滴定終點讀數時,仰視滴定管的刻度,其他操作正確
C.盛裝未知液的錐形瓶用蒸餾水洗過后再用未知液潤洗
D.所配的標準NaOH溶液物質的量濃度偏大
(2)判斷滴定終點的現象是_____________________________________。
(3)如圖是某次滴定時的滴定管中的液面,其讀數為________mL。

(4)根據下列數據,請計算待測鹽酸的濃度:________mol·L-1。
滴定次數 | 待測體積(mL) | 標準燒堿溶液體積(mL) | |
滴定前讀數 | 滴定后讀數 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 2.00 | 24.10 |
第三次 | 20.00 | 4.00 | 24.00 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com