
【題目】下列各項正確的是
A. 鈉與水反應的離子方程式:Na+H2O = Na++OH-+H2↑
B. 氯氣與水反應的離子方程式:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
C. AlCl3溶液中滴入過量的氨水:Al3++3NH3·H2O = Al(OH)3↓+3NH4+
D. 鈉和硫酸銅溶液反應的離子方程式:2Na+Cu2+ = 2Na++Cu
【答案】C
【解析】
A. 原子不守恒;
B. 次氯酸為弱酸,寫化學式,不能拆;
C. 氯水為弱堿,可以與鋁鹽制備氫氧化鋁沉淀;
D. 鈉投入到鹽溶液,首先與水反應生成氫氧化鈉與氫氣。
A. 鈉與水反應的離子方程式:2Na+2H2O = 2Na++2OH-+H2↑,故A項錯誤;
B. HClO為弱電解質,在離子方程式書寫時,應寫成化學式,則氯氣與水反應的離子方程式:Cl2+H2O![]() H++Cl-+HClO,故B項錯誤;
H++Cl-+HClO,故B項錯誤;
C. Al(OH)3不溶于弱堿,則AlCl3溶液中滴入過量的氨水的離子方程式為:Al3++3NH3·H2O = Al(OH)3↓+3NH4+,故C項正確;
D. 鈉化學性質很活潑,與硫酸銅溶液反應時,先與水反應生成氫氧化鈉與氫氣,生成的氫氧化鈉再繼續與溶質硫酸銅反應生成氫氧化銅沉淀,其離子方程式:2Na+Cu2++2H2O= 2Na++Cu(OH)2↓+H2↑,故D項錯誤;
答案選C。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】向NaOH和Na2CO3的混合溶液中滴加0.1mol/L稀鹽酸,CO2的生成量與加入鹽酸的體積(V)的關系如下圖所示。下列判斷正確的是

A. 在0-a范圍內,只發生中和反應
B. ab段發生反應的離子方程式為CO32- +2H+ = CO2 ↑+H2O
C. a = 0.3
D. 原混合溶液中NaOH和Na2CO3的物質的量之比為1:2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電解原理在化學工業中有廣泛應用。右圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連。請回答以下問題:

(1)若X、Y都是惰性電極,a是飽和NaCl溶液,實驗開始時,同時在兩邊各滴入幾滴酚酞試液,則
①電解池中X極上的電極反應式為 。在X極附近觀察到的現象是 。
②Y電極上的電極反應式為 ,檢驗該電極反應產物的方法是 。
(2)如要用電解方法精煉粗銅,電解液a選用CuSO4溶液,則
①X電極的材料是 ,電極反應式是 。
②Y電極的材料是 ,電極反應式是 。
(說明:雜質發生的電極反應不必寫出)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過氧化氫H2O2(氧的化合價為﹣1價),俗名雙氧水,醫療上利用它有殺菌消毒作用來清洗傷口。對于下列A~D涉及H2O2的反應,填寫空白:
A.Na2O2+2HCl===2NaCl+H2O2
B.Ag2O+H2O2===2Ag+O2+H2O
C.2H2O2===2H2O+O2
D.3H2O2+Cr2(SO4)3+10KOH===2K2CrO4+3K2SO4+8H2O
(1)H2O2僅體現氧化性的反應是_________(填代號)。
(2)H2O2既體現氧化性又體現還原性的反應是_________(填代號)。
(3)在稀硫酸中,KMnO4和H2O2能發生氧化還原反應。
氧化反應:H2O2﹣2e﹣===2H++O2↑
還原反應:MnO![]() +5e﹣+8H+===Mn2++4H2O
+5e﹣+8H+===Mn2++4H2O
寫出該氧化還原反應的離子方程式:___________________。
(4)在K2Cr2O7+14HCl===2KCl+3Cl2↑+7H2O+2CrCl3的反應中,有0.3 mol電子轉移時生成Cl2的體積為______(標準狀況),被氧化的HCl的物質的量為____。
(5)除去鎂粉中混入的鋁粉雜質用溶解、_______方法,化學反應方程式為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室需要0.80 mol·L-1 NaOH溶液475 mL 和0.40 mol·L-1硫酸500 mL。根據這兩種溶液的配制情況回答下列問題:
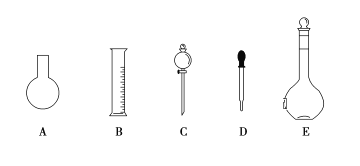
(1)如圖所示的儀器中配制溶液肯定不需要的是____________(填序號),配制上述溶液還需用到的玻璃儀器是____________________(填儀器名稱)。
(2)容量瓶所不具備的功能有________(填序號)。
A.配制一定體積準確濃度的標準溶液
B.量取一定體積的液體
C.測量容量瓶規格以下的任意體積的液體
D.貯存溶液
E.用來加熱溶解固體溶質
(3)根據計算用托盤天平稱取NaOH的質量為___________g。
(4)在實驗中其他操作均正確,若容量瓶用蒸餾水洗滌后未干燥,則所得溶液濃度________0.80 mol·L-1(填“大于”“等于”或“小于”,下同)。若還未等溶液冷卻就定容了,則所得溶液濃度________0.80 mol·L-1。
(5)根據計算得知,所需質量分數為98%、密度為1.84 g·cm-3的濃硫酸的體積為________mL(計算結果保留一位小數)。如果實驗室有10 mL、15 mL、20 mL、50 mL的量筒,最好選用________mL的量筒。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組同學為探究 H2O2、 H2SO3、 Br2 氧化性強弱,設計如下實驗(夾持儀器已略去,裝置的氣密性已檢驗)。
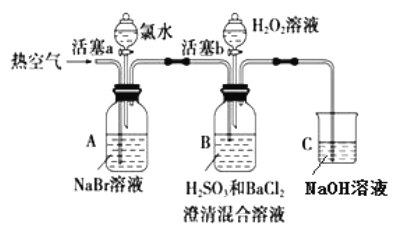
實驗記錄如下:
實驗操作 | 實驗現象 | |
① | 打開活塞 a,滴加氯水,關閉活塞 a | _____________________________________________ |
② | 吹入熱空氣一段時間后停止 | A中溶液顏色明顯變淺;B中有氣泡,產生大量白色沉淀,沉降后上層清液為無色 |
③ | 打開活塞b,逐滴加入H2O2溶液 | 開始時溶液顏色無明顯變化;繼續滴加H2O2溶液,一段時間后,混合液逐漸變成橙紅色。 |
完成下列填空:
(1)在進行操作①時,A中的實驗現象是___________,有關反應的離子方程式是___________。
(2)操作②吹入熱空氣的目的是____________。B 中產生白色沉淀的化學式是___________。
(3)裝置C的作用是____________________。
(4)由上述實驗可知,在此實驗條件下,H2O2、H2SO3、Br2氧化性強弱順序為________________。
(5)操作③開始時顏色無明顯變化可能原因是(寫出一條即可):___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某無色溶液中可能含有Mg2+、Ba2+、Cl-、HCO3-中的一種或幾種離子。為確定其成分,進行以下實驗:
實驗1:取l0mL無色溶液,滴加適量稀鹽酸無明顯現象。
實驗2:另取l0mL無色溶液,加入足量的Na2SO4溶液,有白色沉淀生成。
實驗3:將實驗l后的溶液于錐形瓶中,向錐形瓶中逐滴加入NaOH溶液,滴加過程中產生沉淀的質量與加入NaOH溶液的體積的關系如圖所示。

回答下列問題:
(1)原溶液中不存在的離子有________,存在的離子有___________________。
(2)實驗3中,圖像中OA段反應的離子方程式為___________________。
(3)根據圖像計算原溶液中Mg2+的物質的量濃度______________。(寫出計算過程)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知20℃時,飽和NaCl溶液的密度為ρg/cm3,物質的量濃度為c mol/L,則下列說法中不正確的是
A. 溫度低于20℃時,飽和NaCl溶液的濃度小于c mol/L
B. 此溶液中NaCl的質量分數為![]()
C. 20℃時,密度小于ρg/cm3的NaCl溶液是不飽和溶液
D. 20℃時,飽和NaCl溶液的溶解度![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將4molA氣體和2molB氣體在2L的容器中混合并在一定條件下發生如下反應:2A(g)+B(g) 2C(g)。若經2s后測得C的濃度為0.6mol/L,現有幾種說法:
①用物質A表示的反應的平均速率為0.3 mol/Ls
②用物質B表示的反應的平均速率為0.6 mol/Ls
③2s時物質A的轉化率為70%
④2s時B物質的濃度為0.7 mol/L
其中正確的是( )
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com