
以下關于膠體的說法不正確的是
A.膠體粒子能透過濾紙,但不能透過半透膜
B.Fe(OH)3膠體粒子具有較大的表面積,具有吸附性,能吸附陽離子,故在電場作用下會產生電泳現象
C.向Fe(OH)3膠體中逐滴滴入稀硫酸,會先出現紅褐色沉淀然后沉淀消失的現象
D.只有膠體粒子能作布朗運動
科目:高中化學 來源:2015-2016學年遼寧東北育才學校高二下第二段考化學試卷(解析版) 題型:填空題
(1)基態鈦原子的價電子排布圖為
(2)已知TiCl4在通常情況下是無色液體,熔點為﹣37℃ ,沸點為136℃ ,可知TiCl4為 晶體.
(3)硫酸氧鈦晶體中陽離子為鏈狀聚合形式的離子,結構如圖所示。該陽離子Ti與O的原子數之比為 。
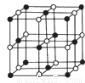
(4)Co的一種氧化物的晶胞如圖所示,在該晶體中與一個鈷原子等距離且最近的鈷原子有 個;筑波材料科學國家實驗室一個科研小組發現了在5K下呈現超導性的晶體,該晶體具有CoO2的層狀結構(如圖所示,小球表示Co原子,大球表示O原子)。下列用粗線畫出的重復結構單元示意圖不能描述CoO2的化學組成是 。

(5)由C、Mg、Ni三種元素組成的一種簡單立方結構的化合物具有超導性,其晶胞中C位于體心位置,Mg位于頂角,Ni占據面心位置,該化合物的化學式為 ,晶體中Mg原子周圍距離最近的Ni原子有 個,該新型超導材料晶胞參數a=0.38nm,計算該晶體的密度 (g•cm﹣3)(保留三位有效數字)
(6)金屬鈦晶胞結構如圖所示,設鈦原子的半徑為r,則該晶胞體積的表達式為

查看答案和解析>>
科目:高中化學 來源:2016屆海南中學高三考前高考模擬十化學試卷(解析版) 題型:填空題
焦炭與CO、CO2、H2均是重要的化工原料,由CO2制備甲醇過程可能涉及的反應如下:
反應Ⅰ:CO2 (g)+3H2 (g)  CH3OH(g)+H2O(g) △H1 =-49.58kJ·mol -1
CH3OH(g)+H2O(g) △H1 =-49.58kJ·mol -1
反應Ⅱ:CO2 (g)+H2 (g)  CO(g)+H2O(g) △H2 =+41.19kJ·mol -1
CO(g)+H2O(g) △H2 =+41.19kJ·mol -1
反應Ⅲ:CO(g)+2H2(g)  CH3OH(g) △H3
CH3OH(g) △H3
回答下列問題:
(1)反應Ⅲ的△H3 = ,反應Ⅲ自發進行的條件是 (填“較低溫”、“較高溫”或“任何溫度”)。
(2)將焦炭與水蒸氣置于容積為2L的密閉容器中發生反應:C(s) +H2O(g)  CO(g)+H2(g),其中H2O、
CO(g)+H2(g),其中H2O、
CO的物質的量隨時間的變化曲線如圖所示。

①0~1min 內用H2表示該反應的速率為 ,第一個平衡時段的平衡常數是 。
②若反應進行到2min時,改變了溫度,使曲線發生如圖所示的變化,則溫度變化為 (填“升溫”或“降溫”)。
③反應至5min時,若也只改變了某—個條件,使曲線發生如圖所示的變化,該條件可能是下述中的 。
a.加入了C(s) b.加入了水蒸氣
c.降低了溫度 d.增大了壓強
(3)某研究小組將一定量的H2和CO2充入恒容密閉容器中并加入合適的催化劑(發生反應Ⅰ、Ⅱ、Ⅲ),測得了不同溫度下體系達到平衡時CO2的轉化率(曲線a)及CH3OH 的產率(曲線b),如圖所示,請回答問題:
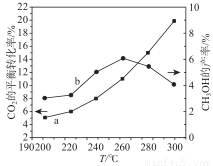
據圖可知當溫度高于260℃后,CO的濃度隨著溫度的升高而 (填“增大”、“減小”、“不變”或“無法判斷”),其原因是 。
(4)若以CO、O2、K2CO3等構成的熔融鹽電池為電源,用惰性電極電解200mL 飽和食鹽水,則負極上的電極反應式為 ,當有2.8g燃料被消耗時,電解池中溶液的pH= (常溫下,忽略溶液的體積變化,不考慮能量的其他損耗)。
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三臨考模擬化學試卷(解析版) 題型:實驗題
現有一份含有FeCl3和FeCl2固體的混合物,為測定FeCl2的含量,進行如下實驗:
①稱取混合物樣品的質量7.06g,將樣品溶解
②向溶解后的溶液中,加入足量的雙氧水
③再向②所得溶液中加入足量的NaOH溶液,得到紅褐色沉淀
④將沉淀過濾、洗滌后,加熱灼燒,到質量不再減少,得到固體物質4.00g
根據實驗回答下列問題:
(1)樣品溶解過程中需加入___________,以防止__________________;
(2)寫出溶解后的溶液與雙氧水反應的離子方程式____________;
(3)過濾操作中除用漏斗外,還需要的玻璃儀器有____________;
(4)簡述檢驗實驗步驟④中沉淀已經洗滌干凈的方法____________;
(5)通過實驗所得數據,計算固體樣品中FeCl2的質量分數:____________;
(6)實驗室采用下列裝置制取少量無水FeCl3固體。(已知FeCl3固體易潮解,部分夾持儀器已略去。)
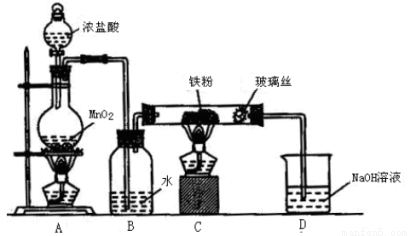
該裝置存在明顯缺陷,得不到無水FeCl3固體,請你對該裝置進行合理的改進:____________。
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三臨考模擬化學試卷(解析版) 題型:選擇題
往碘化亞鐵溶液中緩慢通入1.5mol氯氣,反應完成后溶液中有1/2的Fe2+被氧化成Fe3+。則原碘化亞鐵溶液的物質的量為
A.1.1mol B.1.5mol C.1.2mol D.1.0mol
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三考前預測化學試卷(解析版) 題型:填空題
某大學實驗室對煤矸石(主要含Al2O3、SiO2及Fe2O3)制備聚合氯化鋁{[Al2(OH)nCl6-n]m(1≤n≤5,m≤10),簡稱PAC,是一種新型、高效的絮凝劑和凈水劑}。其工藝流程如下:
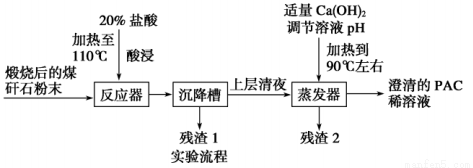
請回答下列問題:
(1)用濃鹽酸配制20%的鹽酸所需的玻璃儀器有______________________________。
(2)加20%的鹽酸酸浸,有關反應的離子方程式為_____________________________。
(3)殘渣2的主要成分是,設計實驗證明你的結論(填操作、現象):_____________________。
(4)由澄清的PAC稀溶液獲得聚合氯化鋁固體,該實驗操作是_________________,得到的PAC粗產品中可能含有的雜質離子是____________。
(5)從不引入雜質的角度來考慮,調節溶液pH的試劑可改為________(填字母)。
A.NaOH B.Al C.氨水 D.Al2O3
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三考前預測化學試卷(解析版) 題型:填空題
BPA的結構簡式如右下圖所示,常用來生產防碎塑料聚碳酸酯。
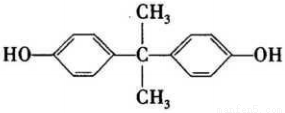
(1)該物質的分子式為___________,含氧官能團的名稱是_________,屬于____類。
(2)該物質最多_____個碳原子共面。
(3)充分燃燒0.1mol該有機物,消耗的O2在標準狀況下的體積為_________。
(4)下列關于BPA的敘述中,不正確的是_______。
A.可以發生還原反應
B.遇FeCl3溶液紫色
C.1mol該有機物最多可與2molH2反應
D.可與NaOH溶液反應
查看答案和解析>>
科目:高中化學 來源:2016屆貴州省高三第八次月考理綜化學試卷(解析版) 題型:實驗題
姜黃素的合成路線如圖所示:

已知:①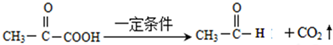
②
請回答下列問題:
(1)D中含有的官能團名稱是__________,D→E的反應類型是__________。
(2)姜黃素的結構簡式為__________。
(3)反應A→B的化學方程式為__________。
(4)D的催化氧化產物與B可以反應生成一種高分子化合物,其結構簡式為__________。
(5)下列有關E的敘述不正確的是__________(填序號).
a.能發生氧化、加成、取代和縮聚反應
b.1molE與濃溴水反應最多消耗3mol的Br2
c.E能與FeCl3溶液發生顯色反應
d.1molE最多能與3molNaOH發生反應
(6)G香蘭醛(C8H8O3)的同分異構體中,符合下列條件的共有__________種,其中核磁共振氫譜中有4組吸收峰的同分異構體的結構簡式為__________
①屬于酯類;②能發生銀鏡反應;③苯環上的一取代物只有2種;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com