

 HCO3-+OH-,溶液顯堿性,促進油脂的水解(結合相關離子方程式解釋).
HCO3-+OH-,溶液顯堿性,促進油脂的水解(結合相關離子方程式解釋).分析 (1)合成氨的原料氣是N2、H2;反應物為甲烷和水,條件是高溫、催化劑,產物之一是氫氣,甲烷完全燃燒產物是二氧化碳,不完全燃燒產物為一氧化碳,據此寫出即可;
(2)依據反應原理推斷設備A中的化學反應方程式,并得出副產物;
(3)依據尿素的化學式和題目所給的額信息結合化學反應原理寫出化學反應方程式;
(4)純堿是Na2CO3,是強堿弱酸鹽,在溶液中水解顯堿性,而油脂能在堿性條件下水解;
(5)根據流程圖來分析;
(6)依據質量分數的計算方法,計算即可.
解答 解:(1)合成氨的原料氣是N2、H2;依據題給的信息,甲烷與水在高溫催化劑作用下生成二氧化碳(或一氧化碳)和氫氣,故化學反應方程式為CH4+2H2O $\frac{\underline{\;\;催化劑\;\;}}{高溫高壓}$CO2+4H2或CH4+H2O$\frac{\underline{\;\;催化劑\;\;}}{高溫高壓}$CO+3H2,故答案為:CH4+2H2O $\frac{\underline{\;\;催化劑\;\;}}{高溫高壓}$CO2+4H2或CH4+H2O$\frac{\underline{\;\;催化劑\;\;}}{高溫高壓}$CO+3H2;
(2)在生產中,設備A中應生成目標產物純堿,故發生的反應為:NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,由于NaHCO3是想得到的產品,故NH4Cl是副產品,故答案為:NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓;NH4Cl;
(3)尿素的水解生成兩種氣體,結合尿素的元素組成,故生成的是氨氣和二氧化碳,故反應為:CO(NH2)2+H2O=2NH3↑+CO2↑,故答案為:NaCl;CO(NH2)2+H2O=2NH3↑+CO2↑;
(4)純堿是Na2CO3,是強堿弱酸鹽,在溶液中水解顯堿性:CO32-+H2O HCO3-+OH-,而油脂能在堿性條件下水解,故答案為:CO32-+H2O
HCO3-+OH-,而油脂能在堿性條件下水解,故答案為:CO32-+H2O HCO3-+OH-,溶液顯堿性,促進油脂的水解;
HCO3-+OH-,溶液顯堿性,促進油脂的水解;
(5)根據流程圖可知,由于合成氨的反應是可逆反應,不能進行徹底,故N2、H2可以循環利用,NaHCO3及分解產生的CO2也可以循環利用,故答案為:N2、H2、CO2、NaHCO3;
(6)生成mg固體為BaCO3,其物質的量為:$\frac{mg}{197g/mol}$,則碳酸鈉的質量為:$\frac{mg}{197g/mol}$×106g/mol=$\frac{106m}{197}$g,
故氯化鈉的質量為(w-$\frac{106m}{197}$)g,則氯化鈉的質量分數為:$\frac{w-\frac{106m}{197}}{w}$×100%=(1-$\frac{106m}{197w}$)×100%,
故答案為:(1-$\frac{106m}{197w}$)×100%.
點評 本題考查了純堿的工業制法,題目難度較大,試題知識點較多、綜合性較強,充分考查了學生的分析、理解能力及靈活應用基礎知識的能力,明確合成原理為解答關鍵.


 字詞句篇與同步作文達標系列答案
字詞句篇與同步作文達標系列答案科目:高中化學 來源: 題型:選擇題
| A. | 金屬元素與非金屬元素能形成共價化合物 | |
| B. | 只有在原子中,質子數與核外電子數相等 | |
| C. | 目前使用的元素周期表中,最長的周期含有36種元素 | |
| D. | 氧和臭氧互為同位素 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題


查看答案和解析>>
科目:高中化學 來源: 題型:解答題
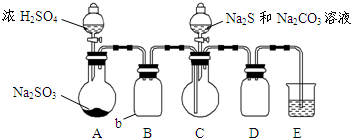 硫代硫酸鈉是一種重要的化工產品.某興趣小組擬制備硫代硫酸鈉晶體(Na2S2O3•5H2O).
硫代硫酸鈉是一種重要的化工產品.某興趣小組擬制備硫代硫酸鈉晶體(Na2S2O3•5H2O).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 把電能轉變為化學能的裝置 | |
| B. | 活潑金屬做正極,不活潑金屬或非金屬做負極 | |
| C. | 外電路中電子從負極流向正極 | |
| D. | 正極發生氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ⅦA族元素形成的單質的熔點隨元素原子序數增大而升高 | |
| B. | ⅦA族元素易形成-1價離子 | |
| C. | 最高價氧化物的水化物顯酸性 | |
| D. | 從上到下氣態氫化物的穩定性依次增強 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com