
如圖所示,將充滿NO2氣體的三個燒瓶關閉彈簧夾后,分別置于盛有下列物質的燒杯(燒杯內有水)中,下列敘述正確的是
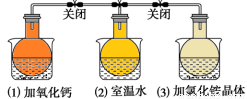
A.燒瓶(3)中氣體顏色最深
B.NH4Cl溶于水時放出熱量
C.2NO2 N2O4是放熱反應
N2O4是放熱反應
D.燒瓶(2)中氣體的壓強比(1)大
科目:高中化學 來源:2016-2017學年河北省高二上開學測化學試卷(解析版) 題型:推斷題
已知A、B、C、D、E、F、G、H、I均為有機物,根據下列框圖和已知條件回答問題:
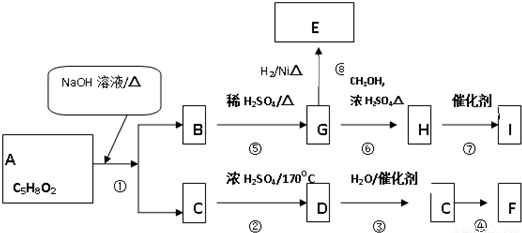
已知:A中有一個甲基,D都能使溴水褪色,F能發生銀鏡反應,I的結構簡式為: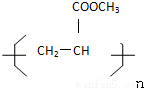
請回答下列問題:
(1)A中含有的官能團: (文字敘述)
(2)屬于取代反應的有:
(3)寫出反應④的化學方程式
(4)寫出A的結構簡式
(5)E有多種同分異構體,其中一種既能發生銀鏡反應又能和NaOH溶液反應,請寫出它的結構簡式
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省高一上開學測化學試卷(解析版) 題型:選擇題
已知反應A2(g)+B2(g)= 2AB(g),斷開1molA2中的化學鍵消耗的能量為Q1 kJ,斷開1mol B2中的化學鍵消耗的能量為Q2 kJ,生成1molAB中的化學鍵釋放的能量為Q3 kJ(Q1、Q2、Q3均大于零),則下列說法正確的是( )
A.若A2和B2的總能量之和大于生成的2AB的總能量,則反應放熱
B.若A2和B2的總能量之和小于生成的2AB的總能量,則反應放熱
C.若該反應為放熱反應,則Q1+Q2<Q3
D.若該反應為吸熱反應,則Q1+Q2<Q3
查看答案和解析>>
科目:高中化學 來源:2017屆重慶一中高三上學期開學測理綜化學試卷(解析版) 題型:選擇題
向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量與生成沉淀和氣體的量(縱坐標)的關系如圖所示,則溶液中三種離子的物質的量之比為
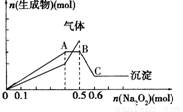
A.2:1:2 B.1:2:2 C.2:2:1 D.9:2:4
查看答案和解析>>
科目:高中化學 來源:2017屆山西省等五校高三上學期第一次聯考化學試卷(解析版) 題型:實驗題
某工廠的廢金屬屑的主要成分為鋁、鐵和銅,某化學興趣小組在學習了元素及其化合物的相關知識后,設計了如圖1實驗流程,用該工廠的金屬廢料制取氯化鋁、綠礬晶體(FeSO4·7H2O)和膽礬晶體(CuSO4·5H2O)。
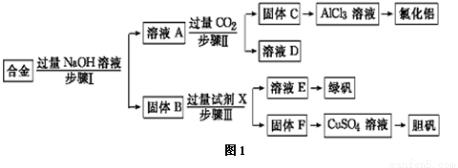
請回答:
(1)寫出步驟Ⅱ反應的離子方程式: 。
(2)步驟Ⅰ、Ⅱ、Ⅲ進行的實驗操作中均需用到的玻璃儀器有 。
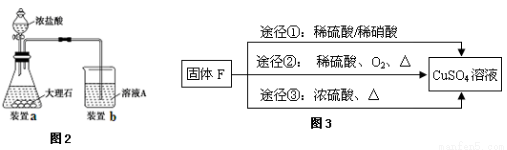
(3)進行步驟Ⅱ時,該小組用如圖2所示裝置及試劑制取CO2并將制得的氣體通入溶液A中一段時間后,觀察到燒杯中產生的白色沉淀會逐漸減少,原因是 。
(4)從溶液E得到綠礬晶體的實驗操作是 。
(5)用固體F制備CuSO4溶液,可設計如圖3三種途徑:
寫出途徑③中反應的化學方程式: ,用途徑①制備CuSO4溶液時,混酸中硫酸和硝酸的最佳物質的量之比為 。
(6)用惰性電極電解硫酸銅溶液一段時間后,陰極增重3.2g。請寫出陽極電極反應式 ,陽極產生 L氣體(標準狀況)。
查看答案和解析>>
科目:高中化學 來源:2017屆山西省等五校高三上學期第一次聯考化學試卷(解析版) 題型:選擇題
以硫鐵礦為原料生產硫酸所得的酸性廢水中砷元素含量極高,為控制砷的排放,采用化學沉降法處理含砷廢水,相關數據如下表,若混合溶液中Ca2+、Al3+、Fe3+的濃度均為1.0×10-3 mol·L-1,c(AsO43-)最大是
難溶物 | Ksp |
Ca3(AsO4)2 | 6.8×10-19 |
AlAsO4 | 1.6×10-16 |
FeAsO4 | 5.7×10-21 |
A.5.7×10-18 mol·L-1 B.2.6×10-5 mol·L-1
C.1.6×10-13 mol·L-1 D.5.7×10-24 mol·L-1
查看答案和解析>>
科目:高中化學 來源:2017屆山西省等五校高三上學期第一次聯考化學試卷(解析版) 題型:選擇題
下列有關化學用語表示正確的是
A.原子結構示意圖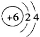 只能表示12C,不能表示14C
只能表示12C,不能表示14C
B.次氯酸的結構式:H-Cl-O
C.NH4Cl的電子式:
D.間硝基甲苯的結構簡式: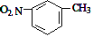
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二上9月調研化學試卷(解析版) 題型:選擇題
根據碘與氫氣反應的熱化學方程式 (i)I2(g)+H2(g) 2HI(g) △H= - 9.48kJ/mol ,(ii) I2(s)+H2(g)
2HI(g) △H= - 9.48kJ/mol ,(ii) I2(s)+H2(g) 2HI(g) △H= + 26.48kJ/mol,下列判斷正確的是
2HI(g) △H= + 26.48kJ/mol,下列判斷正確的是
A.254g I2(g)中通入2g H2(g),反應放熱9.48 kJ
B.1 mol固態碘與1mol氣態碘所含的能量相差l7.00 kJ
C.反應(i)的產物比反應(ii)的產物穩定
D.反應(i) 拆開1mol I-I鍵與1mol H-H鍵需要的總能量小于拆開2mol H-I鍵需要的總能量
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省高二上開學測化學試卷(解析版) 題型:選擇題
微型鈕扣電池在現代生活中有廣泛應用.有一種銀鋅電池,其電極分別是Ag2O和Zn,電解質溶液為KOH,電極反應為:
Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-
根據上述反應式,判斷下列敘述中正確的是( )
A.在使用過程中,電池負極區溶液的pH增大
B.使用過程中,電子由Ag2O極經外電路流向Zn極
C.Zn是正極,Ag2O是負極
D.Zn電極發生還原反應,Ag2O電極發生氧化反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com