
 周期表前四周期的元素a、b、c、d、e,原子序數依次增大.a是宇宙中最豐富的元素,b的價電子層中的未成對電子有3個,c的最外層電子數為其內層電子數的3倍,d與c同族,e的最外層只有1個電子,但次外層有18個電子.回答下列問題:
周期表前四周期的元素a、b、c、d、e,原子序數依次增大.a是宇宙中最豐富的元素,b的價電子層中的未成對電子有3個,c的最外層電子數為其內層電子數的3倍,d與c同族,e的最外層只有1個電子,但次外層有18個電子.回答下列問題: .
.分析 周期表前四周期的元素a、b、c、d、e,原子序數依次增大.a是宇宙中最豐富的元素,則a為H元素;c的最外層電子數為其內層電子數的3倍,原子只能有2個電子層,最外層電子數為6,故c為O元素;b的價電子層中的未成對電子有3個,原子序數小于氧,核外電子排布為1s22s22p3,故b為N元素;e的最外層只有1個電子,但次外層有18個電子,處于第四周期,故核外電子數為2+8+18+1=29,則e為Cu;d與c(氧)同族,d的原子序數小于Cu,故d為S元素,據此解答.
解答 解:周期表前四周期的元素a、b、c、d、e,原子序數依次增大.a是宇宙中最豐富的元素,則a為H元素;c的最外層電子數為其內層電子數的3倍,原子只能有2個電子層,最外層電子數為6,故c為O元素;b的價電子層中的未成對電子有3個,原子序數小于氧,核外電子排布為1s22s22p3,故b為N元素;e的最外層只有1個電子,但次外層有18個電子,處于第四周期,故核外電子數為2+8+18+1=29,則e為Cu;d與c(氧)同族,d的原子序數小于Cu,故d為S元素.
(1)N元素原子2p能級是半滿穩定狀態,能量較低,第一電離能高于同周期相鄰元素,同主族自上而下第一電離能減小,故第一電離能:N>O>S,
e為Cu元素,基態E原子的價電子排布為3d104s1,價電子軌道示意圖為 ,
,
故答案為:N>O>S; ;
;
(2)c的氫化物為H2O、d的氫化物為H2S,由于水分子之間能形成氫鍵,故沸點:H2O>H2S,
故答案為:H2O>H2S;水分子之間能形成氫鍵;
(3)a是H元素,a和其他元素形成的二元共價化合物中,分子呈三角錐形,該分子為氨氣,氨氣分子中氮原子含有3個共價鍵和一個孤電子對,所以該分子的中心原子的雜化方式為sp3;分子中既含有極性共價鍵、又含有非極性共價鍵的化合物是H2O2、N2H4等,
故答案為:sp3;H2O2、N2H4;
(4)這些元素形成的含氧酸中,分子的中心原子的價層電子對數為3的酸是HNO2、HNO3;酸根呈三角錐結構的酸是H2SO3,
故答案為:HNO2、HNO3;H2SO3;
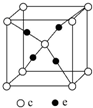
(5)根據晶胞的結構圖可知,晶胞中含有氧原子數為1+8×$\frac{1}{8}$=2,銅原子數為4,所以該化合物的化學式為Cu2O,銅離子化合價為+1,氧離子周圍有4個+1價銅離子,配位數為4;
晶胞質量為(4×$\frac{64}{{N}_{A}}$+2×$\frac{16}{{N}_{A}}$)g,晶胞的邊長為a pm,則晶胞體積為(a×10-10cm)3,則晶胞密度為:(4×$\frac{64}{{N}_{A}}$+2×$\frac{16}{{N}_{A}}$)g÷(a×10-10cm)3=$\frac{288×1{0}^{30}}{{a}^{3}{N}_{A}}$g/cm3,
故答案為:+1;4;$\frac{288×1{0}^{30}}{{a}^{3}{N}_{A}}$.
點評 本題是對物質結構的考查,涉及核外電子排布、電離能、雜化軌道、空間構型、晶胞的計算等,中等難度,需要學生具備扎實的基礎,(4)為易錯點,采取逆向思維方式考查構型判斷,增大題目難度.


科目:高中化學 來源: 題型:選擇題
| A. | 在0.1 mol•L-1BA溶液中,c(A-)+c(H+)=c(OH-)+c(B+) | |
| B. | 若將0.1 mol•L-1 BOH溶液稀釋至0.001 mol•L-1則溶液的pH=9 | |
| C. | 若將一定量的上述兩溶液混合后pH=7,則混合液中:c(A-)>c(B+) | |
| D. | 若將上述兩溶液按體積比1:1混合,則混合液中:c(A-)>c(B+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 逆反應速率增大,平衡逆向移動 | |
| B. | 正反應速率增大,平衡正向移動 | |
| C. | 正、逆反應速率都減小,平衡逆向移動 | |
| D. | 正、逆反應速率都增大,平衡正向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 實驗現象 | 原因 |
| 溶液最初從紫色逐漸變為紅 色 | 氯氣與水反應生成的H+使石蕊變色 |
| 隨后溶液逐漸變為無色 | |
| 然后溶液從無色逐漸變為黃綠 色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ③①④②⑤ | B. | ①③⑤④② | C. | ③②①⑤④ | D. | ⑤②④①③ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | △H3=(△H1+△H2)/2 | B. | △H3=△H1+△H2 | C. | △H2=△H1+△H3 | D. | △H2=(△H1+△H3)/2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有② | B. | 只有②③ | C. | 只有①② | D. | 全部 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com