
 CH3COOC2H5+H2O
CH3COOC2H5+H2O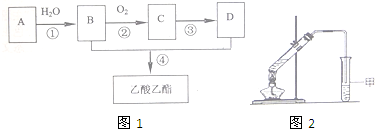
分析 有機物A的產量可以用來衡量一個國家的石油化工發展水平,則A是乙烯;乙烯和水反應生成乙醇,則B是乙醇;乙醇被氧氣氧化生成C、C反應生成D,D和乙醇反應生成乙酸乙酯,則D是乙酸、C是乙醛,據此進行解答.
解答 解:有機物A的產量可以用來衡量一個國家的石油化工發展水平,則A是乙烯,乙烯和水反應生成乙醇,則B是乙醇,乙醇被氧氣氧化生成C,C反應生成D,D和乙醇反應生成乙酸乙酯,則D是乙酸,C是乙醛,
(1)A乙烯,則A中的官能團是碳碳雙鍵,乙烯和水發生加成反應生成乙醇,所以反應類型是加成,
故答案為:碳碳雙鍵;加成;
(2)反應②為:在銅作催化劑、加熱條件下,乙醇被氧氣氧化生成乙醛和水,反應方程式為:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
反應④為:在濃硫酸作催化劑、加熱條件下,乙酸和乙醇發生酯化反應生成乙酸乙酯,反應方程式為:CH3COOH+C2H5OH CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
故答案為:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;CH3COOH+C2H5OH CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(3)G是乙酸乙酯的同分異構體,且G能與NaHCO3反應,則G中含有羧基,為丁酸,可能的結構簡式為:CH3CH2CH2COOH、(CH3)2CHCOOH,
故答案為:CH3CH2CH2COOH、(CH3)2CHCOOH;
(4)①生成物含有乙醇和乙酸,二者都易溶于水,不能用插入到液面以下,否則產生倒吸現象,故答案為:防止倒吸;
②生成的乙酸乙酯不溶于飽和碳酸鈉溶液,應用分液的方法分離,故答案為:b;
③由于乙酸的沸點較低,則乙酸易揮發,揮發出來的乙酸可與碳酸鈉發生反應:2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑,所以產生氣泡,
故答案為:乙酸的沸點低,加熱時,少量乙酸進入試管甲,振蕩時,乙酸與碳酸鈉接觸,發生反應2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑,產生氣泡.
點評 本題考查有機物的推斷,題目難度中等,明確常見有機物結構與性質為解答關鍵,注意掌握乙酸乙酯的制取原理及操作方法,試題側重于學生分析能力、實驗能力的考查,


科目:高中化學 來源: 題型:選擇題
| A. | 實驗室用KClO3制取氧氣所剩余的KCl和MnO2的混合物 | |
| B. | 實驗室用稀鹽酸和大理石反應制取CO2時,得到的CaCl2和大理石的混合物 | |
| C. | 某同學用氫氣還原氧化銅來制取純凈的銅,由于最后操作不當而使還原生成的銅部分被氧化后剩余的混合物 | |
| D. | 用過量的Zn粉和稀H2SO4溶液來制取H2最后剩余的混合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等溫濃度均為0.1 mol•L-1的HA、HB溶液中,其溶液的pH大小為:pH(HA)>pH(HB) | |
| B. | 在0.1mol•L-1的NaA溶液中各離子濃度關系為:c(Na+)>c(A-)>c(OH-)>c(H+) | |
| C. | 等體積pH相同的HA、HB溶液,分別加入等濃度的NaOH溶液,恰好完全反應消耗的NaOH溶液體積HA比HB多 | |
| D. | 等溫濃度均為0.1 mol•L-1的NaA、NaB溶液中,其溶液的pH大小為:pH(NaA)>pH(NaB) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入適量的6 mol•L-1的鹽酸 | B. | 加入適量蒸餾水 | ||
| C. | 加熱 | D. | 用鋅粉替代鋅片 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
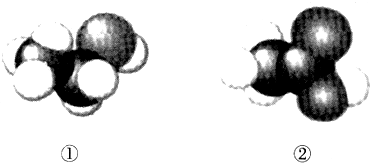
| A. | 二者互為同系物 | B. | 均易溶于水 | ||
| C. | 均能與金屬鈉反應生成氫氣 | D. | 可用紫色石蕊溶液鑒別 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 在體積均為1.0L的兩恒容密閉容器中加入足量的相同的碳粉,再分別加入0.1molCO2和0.2molCO2,在不同溫度下反應CO2(g)+C(s)?2CO(g)達到平衡,平衡時c(CO2)隨溫度的變化如圖所示(圖中Ⅰ、Ⅱ、Ⅲ點均處于曲線上).下列說法正確的是( )
在體積均為1.0L的兩恒容密閉容器中加入足量的相同的碳粉,再分別加入0.1molCO2和0.2molCO2,在不同溫度下反應CO2(g)+C(s)?2CO(g)達到平衡,平衡時c(CO2)隨溫度的變化如圖所示(圖中Ⅰ、Ⅱ、Ⅲ點均處于曲線上).下列說法正確的是( )| A. | 狀態Ⅱ和狀態ⅢCO2的轉化率相同 | |
| B. | 體系的總壓強PⅢ:P總(狀態Ⅱ)>2PⅠ (狀態Ⅰ) | |
| C. | 反應的平衡常數:KⅠ>KⅡ=KⅢ | |
| D. | 逆反應速率v逆:v逆(狀態Ⅰ)>v逆(狀態Ⅲ) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
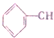 =CH2 D.
=CH2 D.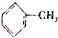
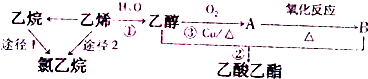
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 酸性強弱:H2SiO3<H2CO3<H2SO4 | B. | 熱穩定性:HCl>HBr>HI | ||
| C. | 原子半徑:Na<Mg<Al | D. | 熔點:SiO2>NaCl>CO2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com