
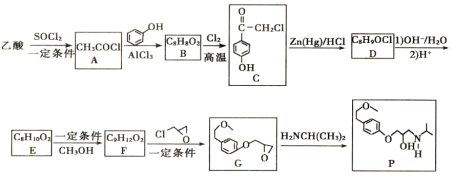
【題目】有機物P可用于治療各種類型高血壓及心絞痛,其合成路線如圖所示:
已知:![]()
![]()
(1)P中含氧官能同的名稱為______________。
(2)A→B的化學方程式為_______________。
(3)C→D的反應類型為_________________。
(4)F的結構簡式為____________,E→F所需的試劑和條件為______________________。
(5)芳香族化合物Q是C的同分異構體,同時滿足下列條件的Q有__________種。
①苯環上有三個取代基 ②分子中含有“![]() ”原子團
”原子團
(6)J(![]() )是一種藥物中間體,參照上述合成路線和相關信息,設計以苯甲酸、苯酚和
)是一種藥物中間體,參照上述合成路線和相關信息,設計以苯甲酸、苯酚和![]() 為原料制備J的合成路線________________(其他無機試劑任選)。
為原料制備J的合成路線________________(其他無機試劑任選)。
【答案】羥基、醚鍵  +HCl 還原反應
+HCl 還原反應 ![]() 濃硫酸、加熱 20
濃硫酸、加熱 20 ![]()
【解析】
乙酸與SOCl2發生取代反應,生成CH3COCl,在氯化鋁環境下與苯酚發生取代反應生成HO-C6H4-COCH3,與氯氣發生取代反應生成![]() ,然后與Zn(Hg)發生還原反應,生成HO-C6H4-CH2CH2Cl,在堿性溶液中發生水解反應后酸化生成HO-C6H4-CH2CH2OH,再與甲醇發生取代反應,生成
,然后與Zn(Hg)發生還原反應,生成HO-C6H4-CH2CH2Cl,在堿性溶液中發生水解反應后酸化生成HO-C6H4-CH2CH2OH,再與甲醇發生取代反應,生成![]() ,最后再經過兩次取代反應生成目標產物。
,最后再經過兩次取代反應生成目標產物。
(1)根據官能團結構可知,P中含氧官能同的名稱為羥基、醚鍵。
(2)根據分子式變化可知,反應為取代反應,A→B的化學方程式為 +HCl。
+HCl。
(3)碳氧雙鍵轉化為碳氫鍵,C→D的反應類型為還原反應。
(4)根據逆推法,F的結構簡式為![]() ,E和F的羥基反應,生成醚鍵,所需的試劑和條件為濃硫酸、加熱。
,E和F的羥基反應,生成醚鍵,所需的試劑和條件為濃硫酸、加熱。
(5)芳香族化合物Q是C的同分異構體,分子式為C8H7O2Cl,①苯環上有三個取代基 ②分子中含有“![]() ”原子團,根據排列組合方法,同時滿足條件的同分異構體有20種。
”原子團,根據排列組合方法,同時滿足條件的同分異構體有20種。
(6)參照上述合成路線和相關信息,根據逆推法,制備![]() 的合成路線為
的合成路線為![]() 。
。


 優生樂園系列答案
優生樂園系列答案科目:高中化學 來源: 題型:
【題目】普通水泥在固化過程中自由水分子減少并產生Ca(OH)2,溶液呈堿性。根據這一物理化學特點,科學家發明了電動勢法測水泥初凝時間。此方法的原理如圖所示,反應的總方程式為:2Cu+Ag2O=Cu2O+2Ag,下列有關說法正確的

A.Cu為正極,Ag2O為負極
B.電池工作時,OH—向正極移動
C.正極的電極反應為:2Cu+2OH——2e—=Cu2O+H2O
D.外電路中每通過2mol電子,正極質量減少16g
查看答案和解析>>
科目:高中化學 來源: 題型:
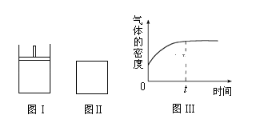
【題目】如圖所示,圖Ⅰ是恒壓密閉容器,圖Ⅱ是恒容密閉容器.當其它條件相同時,在Ⅰ、Ⅱ中分別加入2molX和2molY,開始時容器的體積均為VL,發生如下反應并達到平衡狀態(提示:物質X、Y的狀態均未知,物質Z的狀態為氣態):2X(?)+Y(?)aZ(g)此時Ⅰ中X、Y、Z的物質的量之比為1:3:2。下列判斷正確的是( )
A.物質Z的化學計量數a=2
B.若Ⅱ中氣體的密度如圖Ⅲ所示,則X、Y中只有一種為氣態
C.若X、Y均為氣態,則在平衡時X的轉化率:Ⅰ<Ⅱ
D.若X為固態、Y為氣態,則Ⅰ、Ⅱ中從開始到平衡所需的時間:Ⅰ>Ⅱ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學工作者結合實驗與計算機模擬結果,研究了在Pt/SiO2催化劑表面上CO2與H2的反應歷程,前三步歷程如圖所示,其中吸附在Pt/SiO2催化劑表面上的物種用“· ”標注,Ts表示過渡態。
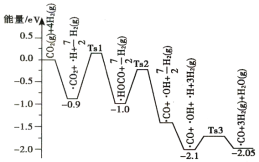
下列有關敘述正確的是
A.前三步總反應的△H<0
B.·HOCO轉化為·CO和·OH為吸熱過程
C.催化劑通過參與化學反應,能降低反應的活化能,提高反應物的轉化率
D.歷程中活化能(能壘)最小的反應方程式為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示測定溶液導電性實驗的裝置,甲與乙中盛有濃度相同的不同液體。接通電源后將甲中液體逐滴滴入乙中,發現燈泡由亮→暗滅→亮。下表中甲、乙所盛液體符合要求的是( )

選項 | 甲 | 乙 |
A | 氯化鈉溶液 | 硝酸銀溶液 |
B | 氨水 | 醋酸 |
C | 稀鹽酸 | 碳酸鈣懸濁液 |
D | 硫酸銅溶液 | 氫氧化鋇溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈷鉬系催化劑主要用于石油煉制等工藝,從廢鈷鉬催化劑(主要含有MoS2、CoS和Al2O3)中回收鈷和鉬的工藝流程如圖:

已知:浸取液中的金屬離子主要為MoO![]() 、Co2+、Al3+。
、Co2+、Al3+。
(1)鉬酸銨[(NH4)2MoO4]中Mo的化合價為___,MoS2在空氣中高溫焙燒產生兩種氧化物:SO2和___(填化學式)。
(2)酸浸時,生成MoO![]() 的離子方程式為___。
的離子方程式為___。
(3)若選擇兩種不同萃取劑按一定比例(協萃比)協同萃取MoO![]() 和Co2+,萃取情況如圖所示,當協萃比=___更有利于MoO
和Co2+,萃取情況如圖所示,當協萃比=___更有利于MoO![]() 的萃取。
的萃取。

(4)向有機相1中滴加氨水,發生反應的離子方程式為___。
(5)Co2+萃取的反應原理為Co2++2HR![]() CoR2+2H+,向有機相2中加入H2SO4能進行反萃取的原因是___(結合平衡移動原理解釋)。
CoR2+2H+,向有機相2中加入H2SO4能進行反萃取的原因是___(結合平衡移動原理解釋)。
(6)水相2中的主要溶質除了H2SO4,還有___(填化學式)。
(7)Co3O4可用作電極,若選用KOH電解質溶液,通電時可轉化為CoOOH,則陽極電極反應式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中正確的是( )
A.22.4L CO2與足量Na2O2反應轉移的電子數為NA
B.1mol·L-1的NaOH溶液中含Na+數目為NA
C.78gNa2O2晶體中含有的陰離子數目為2NA
D.a g CO和H2的混合氣體充分燃燒的產物與足量的Na2O2充分反應后,固體質量增加ag
查看答案和解析>>
科目:高中化學 來源: 題型:
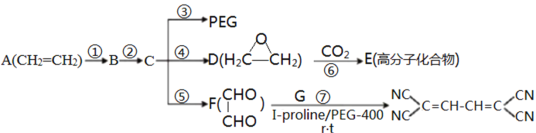
【題目】聚乙二醇(PEG)是一種非離子性惰性溶劑和綠色有機合成的重要催化劑,如圖是合成PEG等的簡單流程,其中E是一種聚碳酸酯高分子化合物。
已知①RCH2Cl![]() RCH2CN
RCH2CN
②R’CHO+RCH2CN![]() +H2O
+H2O
請根據以上信息回答下列問題:
(1)反應②所需的試劑和反應條件___;反應⑥的反應類型是___。
(2)物質F的名稱為___。
(3)物質E的結構簡式為___;反應⑦的另一種產物為水,則G的結構簡式為___。
(4)反應③的化學方程式為___。
(5)M與D的組成元素相同,且M中各原子數目為D中各原子數目的2倍,寫出符合下列條件的M的結構簡式___ (只寫一種)。
a.能與新制的氫氧化銅懸濁液反應生成磚紅色沉淀
b.能在稀硫酸中發生水解反應
(6)寫出以乙烯為原料合成![]() 的路線圖,其它無機試劑任選___。
的路線圖,其它無機試劑任選___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有氯化鈉和碘化鈉的混合物共26.7 g,溶于水,通入足量氯氣后,蒸干、灼燒,固體質量變為 17.55 g。
(1)原混合物中碘化鈉的質量是________。
(2)原混合物中氯化鈉的質量分數是________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com