

分析 Ⅰ.根據容量瓶的使用方法、配制一定物質的量濃度的溶液使用的儀器、中和熱測定使用儀器、中和滴定存在使用的儀器進行分析;
Ⅱ.含有鋁、鐵、銅的合金加入氫氧化鈉溶解,只有鋁與氫氧化鈉反應生成偏鋁酸鈉和氫氣,所以濾渣B為鐵和銅,再經稀硫酸反應過濾的濾液為氯化亞鐵,進一步轉化成綠礬,濾渣F為銅單質,進一步轉化成膽礬;濾液A則為偏鋁酸鈉溶液,加過量鹽酸經途徑Ⅰ生成氯化鋁溶液,而濾液A通足量氣體C經途徑Ⅱ生成沉淀D,根據氫氧化鋁只溶于強酸強堿,所以氣體C為二氧化碳,沉淀D為氫氧化鋁,與鹽酸反應生成氯化鋁溶液,
(1)根據反應所得產物的組成來選擇合適的制取方案;根據所發生的反應來確定溶液的組成情況;
(2)綠礬晶體中有結晶水,溫度過高會使結晶水失去,根據溶液來得到晶體來分析實驗操作;
(3)從“綠色化學”角度考慮,反應中不產生有污染的物質,同時反應的原子利用率要高;
(4)根據銅元素質量守恒進行計算;
(5)根據實驗中的酸和堿的量的情況來對比回答.
解答 解:Ⅰ.①使用容量瓶的第一步操作是檢查容量瓶是否漏水,
故答案為:查漏;
②若用上述儀器配制500mL 2mol•L-1的NaCl溶液,需要的玻璃儀器有:燒杯、玻璃棒、500mL容量瓶、膠頭滴管等,還缺少的玻璃儀器是:燒杯、玻璃棒、膠頭滴管,
故答案為:玻璃棒;膠頭滴管;
③若用上述儀器測定中和熱,則缺少的玻璃儀器為:燒杯、環形玻璃攪拌棒,
故答案為:環形玻璃攪拌棒;
④用上述儀器進行中和滴定,則缺少的儀器是:錐形瓶,
故答案為:錐形瓶;
Ⅱ.含有鋁、鐵、銅的合金加入氫氧化鈉溶解,只有鋁與氫氧化鈉反應生成偏鋁酸鈉和氫氣,所以濾渣B為鐵和銅,再經稀硫酸反應過濾的濾液為氯化亞鐵,進一步轉化成綠礬,濾渣F為銅單質,進一步轉化成膽礬;濾液A則為偏鋁酸鈉溶液,加過量鹽酸經途徑Ⅰ生成氯化鋁溶液,而濾液A通足量氣體C經途徑Ⅱ生成沉淀D,根據氫氧化鋁只溶于強酸強堿,所以氣體C為二氧化碳,沉淀D為氫氧化鋁,與鹽酸反應生成氯化鋁溶液,
(1)途徑Ⅰ偏鋁酸鈉和過量的鹽酸反應生成氯化鋁和氯化鈉的混合物,而途徑Ⅱ向偏鋁酸鈉中通入足量的二氧化碳,會得到純凈的氫氧化鋁沉淀,再用鹽酸溶解,所得溶液的成分只有氯化鋁,所以途徑Ⅱ更合理;鋁、鐵、銅的合金中只有金屬鋁可以和強堿反應生成偏鋁酸鈉和氫氣,所以濾液A的成分是偏鋁酸鈉,可以和過量的二氧化碳反應生成氫氧化鋁和碳酸氫鈉,實質為:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案為:Ⅱ;因為濾液A是偏鋁酸鈉和氫氧化鈉溶液,按途徑I直接向A中加入鹽酸得到的AlCl3溶液中含有大量的氯化鈉雜質;按途徑II通入二氧化碳氣體,得Al(OH)3沉淀,將Al(OH)3溶解于鹽酸中得到的是純凈的AlCl3溶液;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(2)綠礬晶體中有結晶水,溫度過高會使結晶水失去,所以將混合液來制備綠礬時應先將溶液加熱濃縮、然后冷卻結晶,即可得到綠礬,
故答案為:蒸發濃縮、冷卻結晶、過濾;
(3)F為銅單質,從“綠色化學”角度考慮,反應中不產生有污染的物質,同時反應的原子利用率要高,所以F制備膽礬晶體最佳方案為先將銅與空氣中的氧氣反應生成氧化銅,再用硫酸與氧化銅反應生成硫酸銅,反應方程式為2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO、CuO+H2SO4=CuSO4+H2O,
故答案為:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO、CuO+H2SO4=CuSO4+H2O;
(4)20g含Cu 16%的合金中含有銅的物質的量為$\frac{20×16%}{64}$mol=0.05mol,根據銅元素守恒可知,制得膽礬晶體的質量為250g/mol×0.05mol=12.5g,
故答案為:12.5;
(5)在實驗方案一中,酸的量的控制上沒有過高的要求,只需過量即可,但是方案二中,需要的是適量的酸,這很難控,
故答案為:后者的方案不合理;因為該方案不符合實驗方案設計的簡約性原則,即操作步驟多、試劑消耗量大、作用時間長.
點評 本題考查了常見儀器的使用方法、物質的分離和提純等知識,題目難度中等,試題涉及的題量稍大,知識點較多,充分考查了學生分析、理解能力及靈活應用所學知識的能力.


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:解答題
 FeSO4是一種精細化工產品,可用于治療缺鐵性貧血、制革、木材防腐等.制備步驟:①將3mol•L-1硫酸加入鐵粉里,微熱,攪拌使其充分反應;②趁熱過濾;③在50℃左右蒸發、結晶,得到晶體--綠礬(FeSO4•7H2O).回答下列問題:
FeSO4是一種精細化工產品,可用于治療缺鐵性貧血、制革、木材防腐等.制備步驟:①將3mol•L-1硫酸加入鐵粉里,微熱,攪拌使其充分反應;②趁熱過濾;③在50℃左右蒸發、結晶,得到晶體--綠礬(FeSO4•7H2O).回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 Zn-MnO2干電池應用廣泛,其電解質溶液是ZnCl2-NH4Cl混合溶液.
Zn-MnO2干電池應用廣泛,其電解質溶液是ZnCl2-NH4Cl混合溶液.查看答案和解析>>
科目:高中化學 來源: 題型:填空題

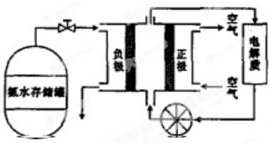
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 實驗室中按照一定順序混合2mL濃硫酸、3mL乙醇、2mL乙酸后加熱制備乙酸乙酯,將產生的蒸汽經導管通到飽和碳酸鈉溶液的液面上(如圖所示).
實驗室中按照一定順序混合2mL濃硫酸、3mL乙醇、2mL乙酸后加熱制備乙酸乙酯,將產生的蒸汽經導管通到飽和碳酸鈉溶液的液面上(如圖所示).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2O的結構式:H-O-H | B. | 乙烯的結構簡式為CH2CH2 | ||
| C. | CO2的比例模型: | D. | 丙烯的電子式: |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | PH4I可由PH3和HI化合而得 | |
| B. | PH4I在物質分類中屬于正鹽 | |
| C. | PH4I對熱不穩定,受熱時產生有色氣體 | |
| D. | PH4I屬于共價化合物 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com