
分析 (1)依據熱化學方程式和蓋斯定律計算(1)×3-(3)×2+(2)×2得到NH3(g)燃燒生成NO2 (g)和H2O(g) 熱化學方程式;
(2)向Ba(OH)2溶液中逐滴加入明礬溶液至鋇離子剛好沉淀完全時氫氧化鋇和硫酸鋁鉀按照2:1反應生成硫酸鋇沉淀、偏鋁酸鉀,據此分析書寫離子方程式;
(3)Mn的原子序數為25,根據能量最低原理可寫出Mn的基態原子的電子排布式,進而可確定Mn2+基態的電子排布式;根據N2與CO為等電子體,結合等電子體結構相似判斷;
解答 解:(1)依據熱化學方程式和蓋斯定律計算得到所需熱化學方程式;
(1)2H2 (g)+O2 (g)=2H2O(g)△H=-483.6kJ/mol
(2)N2 (g)+2O2 (g)=2NO2 (g)△H=67.8kJ/mol
(3)N2 (g)+3H2 (g)=2NH3(g)△H=-92.0kJ/mol
依據熱化學方程式和蓋斯定律計算(1)×3-(3)×2+(2)×2得到NH3(g)燃燒生成NO2 (g)和H2O(g) 熱化學方程式:4NH3(g)+7O2(g)?4NO2(g)+6H2O(g)△H=-1131.2kJ/mol;
故答案為:4NH3(g)+7O2(g)?4NO2(g)+6H2O(g)△H=-1131.2kJ/mol;
(2)向Ba(OH)2溶液中逐滴加入明礬溶液至鋇離子剛好沉淀完全時氫氧化鋇和硫酸鋁鉀按照2:1反應生成硫酸鋇沉淀、偏鋁酸鉀,偏鋁酸鉀是強堿弱酸鹽,偏鋁酸跟離子水解溶液顯堿性,PH>7,依據電荷守恒、原子守恒書寫反應的離子方程式為:2Ba2++4OH-+2SO42-+Al3+=AlO2-+2BaSO4↓+2H2O,
故答案為:>,2Ba2++4OH-+2SO42-+Al3+=AlO2-+2BaSO4↓+2H2O;
(3)Mn的原子序數為25,基態原子的電子排布式為,1s22s22p63s23p63d54s2,則Mn2+基態的電子排布式可表示為1s22s22p63s23p63d5(或[Ar]3d5),N2與CO為等電子體,二者結構相似,N2的結構為N≡N,則CO的結構為C≡O,
故答案為:1s22s22p63s23p63d5;C≡O;
點評 本題考查了熱化學方程式書寫方法和注意問題,物質的結構與性質知識,側重于電子排布式、等電子體判斷等知識,主要是熱化學方程式和蓋斯定律的計算應用,掌握基礎是關鍵,題目難度中等.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
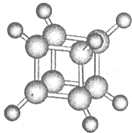
| A. | 其一氯代物只有一種 | B. | 其二氯代物有三種同分異構體 | ||
| C. | 常溫下為氣體 | D. | 它與苯乙烯(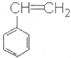 )互為同分異構體 )互為同分異構體 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 氯水的顏色呈淺黃綠色,說明氯水中含有HClO | |
| B. | 向氯水中滴加硝酸酸化的AgNO3溶液,產生白色沉淀,說明氯水中含有Cl- | |
| C. | 向氯水中加入NaHCO3粉末,有氣泡產生,說明氯水中含有H+ | |
| D. | 向品紅溶液中滴加氯水,溶液褪色,說明氯水中含有HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗器材(省略夾持裝置) | 相應實驗 |
| A | 燒杯、玻璃棒、石棉網、酒精燈 | 濃縮結晶硫酸銅溶液制膽礬 |
| B | 燒杯、玻璃棒、膠頭滴管、漏斗、濾紙 | 用鹽酸除去硫酸鋇中的少量碳酸鋇 |
| C | 燒杯、玻璃棒、膠頭滴管、容量瓶 | 用固體氯化鈉配制100 mL 0.5 mol•L-1的溶液 |
| D | 燒杯、玻璃棒、膠頭滴管、分液漏斗 | 用溴水和CCl4除去NaBr溶液中的少量NaI |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 12% | B. | 32% | C. | 44% | D. | 88% |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com