
分析 (1)氨氧化法制取硝酸流程為:氨氣催化氧化生成NO,然后NO與氧氣反應生成NO2,最后NO2與水反應生成HNO3;
根據關系式N2~2HNO3計算生產濃度40%的硝酸的質量;
(2)在所得溶液中加入1L NaOH溶液,反應后溶液呈中性,金屬離子已完全沉淀,溶液中溶質為NaNO3,n(NaNO3)=n(NaOH)=1.0mol/L×1.0L=1mol,沉淀為Cu(OH)2,質量為39.2g,氫氧化鐵物質的量為:$\frac{39.2g}{98g/mol}$=0.4mol,根據銅元素守恒有n(Cu)+2n(Cu2O)=n[Cu(OH)2],反應后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.4mol;
①設Cu和Cu2O的物質的量分別為xmol、ymol,根據二者質量及Cu元素物質的量列方程計算二者的物質的量之比;
②利用電子轉移守恒計算n(NO),根據N元素守恒可知原硝酸溶液n(HNO3)=n(NO)+n(NaNO3),根據Na元素可知n(NaNO3)=n(NaOH),進而計算硝酸濃度;
(3)氫氧化鈉溶液過量,反應后溶液中只含兩種溶質,則反應生成NaNO3,發生的反應為:4NO+3O2+4NaOH=4NaNO3+2H2O,剩余的氣體可能為氧氣,也可能為NO,根據反應方程式進行討論計算出混合氣體中NO與O2的體積.
解答 解:(1)氨氧化法制取硝酸的反應式:4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO;
設能生產出濃度為40%的硝酸x千克,則:
N2~~~~~~~~2HNO3
28 126
200千克×85% 40%×x千克
則28:126=200千克×85%:40%×x千克
解得x=1912.5
故答案為:4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O,2NO+O2=2NO2,3NO2+H2O=2HNO3+NO;1912.5;
(2)①在所得溶液中加入NaOH溶液后,此時溶液呈中性,金屬離子已完全沉淀,溶液中溶質為NaNO3,n(NaNO3)=n(NaOH)=1.0mol/L×1.0L=1mol,沉淀為Cu(OH)2,質量為39.2g,Cu(OH)2的物質的量為:$\frac{39.2g}{98g/mol}$=0.4mol,
根據銅元素守恒有:n(Cu)+2n(Cu2O)=n[Cu(OH)2],所以反應后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.4mol,
設Cu和Cu2O的物質的量分別為xmol、ymol,根據二者質量可得:64x+144y=27.2,
根據銅元素守恒有:x+2y=0.4,
聯立方程解得:x=0.2,y=0.1,
所以原固體混合物中Cu和Cu2O的物質的量之比為2:1,
答:混合物中Cu和Cu2O的物質的量之比為2:1;
②根據電子轉移守恒可知:3n(NO)=2n(Cu)+2n(Cu2O),
即3n(NO)=2×0.2mol+2×0.1mol,
則n(NO)=0.2mol,
根據N元素守恒可知n(HNO3)=n(NO)+n(NaNO3)=0.2mol+1.0mol/L×1.0L=1.2mol,所以原硝酸溶液的濃度為$\frac{1.2mol}{0.5L}$=2.4mol/L,
答:硝酸的物質的量濃度是2.4mol/L.
(3)氫氧化鈉溶液過量,反應后溶液中只含兩種溶質,則反應生成NaNO3,發生的反應為:4NO+3O2+4NaOH=4NaNO3+2H2O,發生反應的NO和O2的總體積為:30mL-2mL=28mL,
若剩余的2mL為NO時,氧氣體積為28mL×$\frac{3}{7}$=12mL,NO體積為:30mL-12mL=18mL,原混合氣體中NO和O2體積比18mL:12mL=3:2;
若剩余的2mL為氧氣時,NO體積為28mL×$\frac{4}{7}$=16mL,氧氣體積為:30mL-16mL=14mL,原混合氣體中NO和O2體積比16mL:14mL=8:7;
答:原混合氣體中NO和O2體積比為3:2或8:7.
點評 本題考查化學方程式計算、混合物計算,屬于拼合型題目,注意守恒法、討論法在化學計算中的應用.


 口算題卡加應用題集訓系列答案
口算題卡加應用題集訓系列答案 綜合自測系列答案
綜合自測系列答案科目:高中化學 來源: 題型:解答題
| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| CO | H2 | CH3OH |
| 0.5mol•L-1 | 2mol•L-1 | 6mol•L-1 |

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
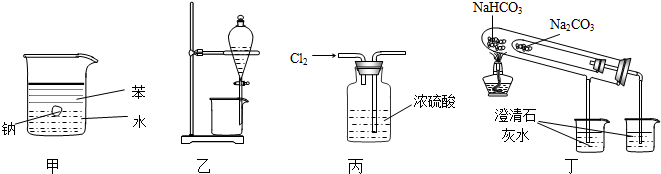
| A. | 用甲圖裝置證明密度ρ(苯)<ρ(鈉)<ρ(水) | |
| B. | 用乙圖裝置分離酒精和四氯化碳 | |
| C. | 用丙圖裝置干燥Cl2 | |
| D. | 用丁圖裝置比較NaHCO3和Na2CO3的熱穩定性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1120mL | B. | 2240mL | C. | 3360mL | D. | 4480mL |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋼鐵發生吸氧或析氫腐蝕時,鐵均作負極反應被氧化:Fe-3e-═Fe3+ | |
| B. | 用銅做電極電解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;通電\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | 草木灰與銨態氮肥不能混用的原因:2NH4++CO32-═2NH3↑+CO2↑+H2O | |
| D. | 不能用濃H2SO4干燥H2S氣體的原因:H2SO4(濃)+H2S═SO2↑+S↓+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 明礬做凈水劑:Al3++3H2O═Al (OH)3↓+3H+ | |
| B. | 小蘇打治療胃酸過多:CO32-+2H+═CO2↑+H2O | |
| C. | 漂白液加白醋,提高漂白效率:CH3COOH+ClO-═HClO+CH3COO- | |
| D. | 酸化的淀粉碘化鉀溶液在空氣中放置一段時間變藍:4I-+O2+2H2O═2I2+4OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com