
| W | 單質是淡黃色固體 |
| X | 在地殼中的含量居第二位 |
| Y | 原子最外層電子數是電子總數的$\frac{2}{3}$ |
| Z | 第3周期原子半徑最小的金屬 |
| A. | 氣態氫化物的熱穩定性:X>W | |
| B. | 非金屬性:Y<W;離子半徑:Z>W | |
| C. | W在空氣中燃燒所得產物,可用于殺菌消毒 | |
| D. | 金屬Z與少量NaOH溶液反應,生成兩性氫氧化物 |
分析 W、X、Y、Z是短周期元素,W單質是淡黃色固體,則W為S元素;X在地殼中的含量居第二位,則X為Si;Y原子最外層電子數是電子總數的$\frac{2}{3}$,只能處于第二周期,令最外層電子數為x,則$\frac{2}{3}$(2+x)=x,解得x=4,則Y為C元素;Z是第3周期原子半徑最小的金屬,則Z為Al,結合元素周期律與元素化合物性質解答.
解答 解:W、X、Y、Z是短周期元素,W單質是淡黃色固體,則W為S元素;X在地殼中的含量居第二位,則X為Si;Y原子最外層電子數是電子總數的$\frac{2}{3}$,只能處于第二周期,令最外層電子數為x,則$\frac{2}{3}$(2+x)=x,解得x=4,則Y為C元素;Z是第3周期原子半徑最小的金屬,則Z為Al.
A.非金屬性W(S)>X(Si),故硫化氫更穩定性,故A錯誤;
B.非金屬性:Y(C)<W(S),Al3+離子比S2-離子少一個電子層,則離子半徑Al3+<S2-,故B錯誤;
C.W在空氣中燃燒所得產物為二氧化硫,可用于殺菌消毒,故C正確;
D.鋁與氫氧化鈉溶液反應生成偏鋁酸鈉,故D錯誤,
故選:C.
點評 本題考查結構性質位置關系應用,推斷元素是解題關鍵,難度不大,注意對基礎知識的理解掌握.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 摩爾是國際單位制的7個基本物理量之一 | |
| B. | 物質的量可以理解為物質的質量 | |
| C. | 物質的量的單位是“摩爾” | |
| D. | 物質的量是表示物質的數量的單位 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 一定溫度下,向2.0L恒容密閉容器中充入1.0mol PCl5,反應PCl5(g)?PCl3(g)+Cl2(g)△H,經過一段時間后達到平衡,反應過程中測定的部分數據如圖.下列說法正確的是( )
一定溫度下,向2.0L恒容密閉容器中充入1.0mol PCl5,反應PCl5(g)?PCl3(g)+Cl2(g)△H,經過一段時間后達到平衡,反應過程中測定的部分數據如圖.下列說法正確的是( )| A. | 反應在50s~250s內的平均速率v(PCl3)=4.0×10-4mol•L-1•s-1 | |
| B. | 保持其他條件不變,升高溫度,平衡時c(PCl5)=0.38 mol•L-1,則反應的△H<0 | |
| C. | 保持其他條件不變,將容器的容積縮小一半,平衡逆向移動,化學平衡常數減小 | |
| D. | 相同溫度下,起始時向容器中充入0.5 mol PCl5,重新達到平衡時,0.1 mol<n(PCl3)<0.2 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
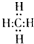 ,結構式是
,結構式是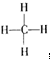 ,能說明它是正四面體而非正方形平面結構的理由是②.(填寫編號)
,能說明它是正四面體而非正方形平面結構的理由是②.(填寫編號)查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁與氧氣在常溫下不反應 | |
| B. | 鋁的化學性質不活潑 | |
| C. | 常溫下與氧氣反應,鋁的表面形成了一層致密的氧化膜 | |
| D. | 鋁制容器既耐酸又耐堿 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{H}_{4}^{+})}$ | B. | $\frac{c(N{H}_{4}^{+})•c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ | ||
| C. | $\frac{c{H}^{+}}{cO{H}^{-}}$ | D. | c(H+)•c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一氧化碳的摩爾質量為28g | |
| B. | 0.5 mol OH-的質量為8.5g | |
| C. | 鎂原子的摩爾質量等于它的相對原子質量 | |
| D. | 一個鈉原子的質量等于$\frac{23}{6.02×1{0}^{23}}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯水要現用現制,并保存在蓋有橡膠塞的棕色瓶子中,置于冷暗處 | |
| B. | 向沸水中逐滴加入少量飽和FeCl3溶液,可制得Fe(OH)3膠體 | |
| C. | HCl溶液和NaCl溶液均通過離子導電,所以HCl和NaCl均是離子化合物 | |
| D. | 電解NaCl溶液得到22.4 L H2(標準狀況),理論上需要轉移NA個電子(NA表示阿伏加德羅常數) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com