
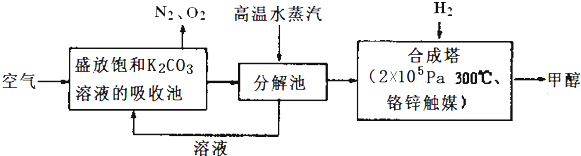
分析 把空氣吹入碳酸鉀溶液,碳酸鉀會吸收空氣中二氧化碳氣體,得到碳酸氫鉀溶液,在高溫水蒸汽中碳酸氫鉀分解生成碳酸鉀,二氧化碳和水,目的是富集二氧化碳,進入合成塔,通入氫氣在一定溫度壓強下反應生成甲醇;
(1)碳酸鉀吸收空氣中二氧化碳反應生成碳酸氫鉀;
(2)分解池中是碳酸氫鉀分解生成碳酸鉀、二氧化碳和水;
(3)依據合成甲醇的反應產物分析判斷原子利用率,原子利用率是指反應物中的所有原子進入期望產物中的百分比,反應達到完全轉化,即100%轉化為目標產物;
(4)空氣中的氧氣和氫氣混合加熱或點燃可能發生爆炸;
(5)依據影響反應速率的因素分析,此溫度會提高反應速率,催化劑活性最大;
(6)Fe3++3H2O?Fe(OH)3+3H+,25℃時Ksp[Fe(OH)3]=2.8×10-39,Ksp=c(Fe3+)×c3(OH-),Kw=c(H+)×c(OH-),則K=$\frac{{c}^{3}({H}^{+})}{c(F{e}^{3+})}$=$\frac{(\frac{Kw}{c(O{H}^{-})})^{3}}{c(F{e}^{3+})}$=$\frac{K{w}^{3}}{Ksp}$.
解答 解:(1)碳酸鉀能和二氧化碳反應生成碳酸氫鈉,所以碳酸鉀的作用是:吸收空氣中二氧化碳,富集空氣中的CO2,反應的化學方程式為:K2CO3+CO2+H2O=2KHCO3,
故答案為:富集空氣中的CO2;
(2)在加熱條件下,碳酸氫鉀能分解生成碳酸鉀、二氧化碳和水,化學方程式為:2KHCO3$\frac{\underline{\;\;△\;\;}}{\;}$K2CO3+CO2↑+H2O;
故答案為:2KHCO3$\frac{\underline{\;\;△\;\;}}{\;}$K2CO3+CO2↑+H2O;
(3)CO2與H2在300℃、2KPa的條件下生成水和甲醇,化學方程式為:CO2+3H2$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CH3OH,產物有甲醇、還有H2O,不符合轉化率100%,若合成塔中有2.2kgCO2與足量H2恰好完全反應,可放出2473.5kJ的熱量,1mol二氧化碳反應放熱49.47KJ,寫出合成塔中發生反應的熱化學方程式為:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.47KJ/mol;
故答案為:否;CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.47KJ/mol;
(4)如果空氣不經過吸收池和分解池,而是直接通入合成塔,空氣中的氧氣和氫氣混合加熱或點燃可能發生爆炸,引發危險,
故答案為:不可以;空氣中的氧氣和氫氣混合加熱或點燃可能發生爆炸,
(5)依據影響反應速率的因素分析,此溫度會提高反應速率,催化劑活性最大,
故答案為:提高催化劑的催化活性,加快反應速率;
(6)Fe3++3H2O?Fe(OH)3+3H+,25℃時Ksp[Fe(OH)3]=2.8×10-39,Ksp=c(Fe3+)×c3(OH-),Kw=c(H+)×c(OH-),則K=$\frac{{c}^{3}({H}^{+})}{c(F{e}^{3+})}$=$\frac{(\frac{Kw}{c(O{H}^{-})})^{3}}{c(F{e}^{3+})}$=$\frac{K{w}^{3}}{Ksp}$=$\frac{(1{0}^{-14})^{3}}{2.8×1{0}^{-39}}$=3.6×10-4,
故答案為:3.6×10-4 .
點評 本題考查了甲醇的工業生產,主要考查物質的相互轉化和制備的方法及注意事項,在解答時,首先分析題中的轉化流程,然后結合學過的知識進行解答,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 0.5 mol•L-1鹽酸 | B. | 0.5 mol•L-1 KOH溶液 | ||
| C. | 0.5 mol•L-1醋酸 | D. | 0.5 mol•L-1Na2SO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 物質 | 沸點/℃ | 熔點/℃ | 密度(20℃)/g•cm-3 | 溶解性 |
| 甲醇 | 64.7 | / | 0.7915 | 易溶于水 |
| 乙醚 | 34.5 | / | 0.7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 | / | 33~36 | / | 易溶于甲醇、乙醚,微溶于水 |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 名稱 | 分子量 | 性狀 | 密度g/cm3 | 熔點℃ | 沸點℃ | 溶解度:克/100mL溶劑 | ||
| 水 | 醇 | 醚 | ||||||
| 苯甲醛 | 106 | 無色液體 | 1.06 | -26 | 178 | 0.3 | 互溶 | 互溶 |
| 乙酸酐 | 102 | 無色液體 | 1.082 | -73 | 138 | 12 | 溶 | 不溶 |
| 肉桂酸 | 148 | 無色固體 | 1.248 | 133 | 300 | 0.04 | 24 | 溶 |

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 步驟①和②中的氣體屬于可循環使用的氣體 | |
| B. | 步驟②中發生的反應為:Ca2++CO2+2NH3•H2O═CaCO3↓+2NH4++H2O | |
| C. | 往甲中通CO2有利于(NH4)2SO4生成 | |
| D. | 以上涉及的化學反應中有氧化還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:多選題

| A. | 點a處的正反應速率比點b處的大 | |
| B. | 點c處的正反應速率與逆反應速率相等 | |
| C. | 點d(t1時刻)的n(N2)比點e(t2時刻)處的n(N2)大 | |
| D. | 其他條件不變,773K下反應至t1時刻,此時畫出的兩根平行線間的距離將要變小 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 開始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com