
【題目】下列反應的化學方程式(或離子方程式)錯誤的是
A. 乙醛與銀氨溶液反應 CH3CHO+2[Ag(NH3)2]OH![]() CH3COONH4+2Ag↓+3NH3+H2O
CH3COONH4+2Ag↓+3NH3+H2O
B. 向Na2CO3溶液中加入過量醋酸溶液:CO32-+2H+=CO2↑+H2O
C. 苯酚與氫氧化鈉溶液反應 C6H5OH+OH—→ C6H5O—+H2O
D. 用鐵棒作陽極、碳棒作陰極電解飽和氯化鈉溶液:2C1-+2H2O![]() H2↑+Cl2↑+2OH—
H2↑+Cl2↑+2OH—
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】前四周期元素A、B、C、D、E、F,原子序數依次遞增。已知:A、B、D、C的價電子數依次增多,其中C元素的原子半徑最小;A有兩個單電子,E的未成對電子數是前四周期中最多的,且其外圍電子數與D相同,F的最外層電子數為2,內層全部排滿。請用對應的元素符號回答下面的問題:
(1)寫出E的價電子排布式:__________________________________________。
(2)在A形成的化合物中,A采取sp2雜化,且分子量最小的化合物為(寫化學式)_____________________, 鍵角約為_____________________________________。
(3)下列物質的性質與氫鍵有關的是__________________________________________
A. 可燃冰的形成 B. A的氫化物的沸點 C. B的氫化物的熱穩定性
(4)E3+可以與AB-形成配離子,其中E3+以d2sp3方式雜化,雜化軌道全部用來與AB-形成配位鍵,則E3+的配位數為________,1mol該配離子中含有_____________molσ 鍵。
(5)在C和D形成的化合物中,中心原子沒有孤電子對的分子的空間構型為__________。
(6)根據下列圖片說明為什么同周期過渡金屬第一電離能變化沒有主族元素變化明顯__________________________________________。

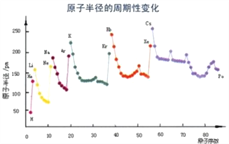
(7)F與D形成的化合物晶胞如圖,F的配位數為_____________,晶體密度為a g/cm3,NA為阿伏加德羅常數,則晶胞邊長為__________________pm。(1pm=10-10cm)

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3 , 在一定條件下可實現如圖所示的物質之間的變化: 
據此回答下列問題:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中對于溶液和沉淀的分離采取的方法是 .
(2)根據上述框圖反應關系,寫出下列B、E所含物質的化學式 B;E .
(3)寫出②、③兩個反應方程式 ②;③ .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有V L 0.5mol/L的鹽酸,欲將其濃度擴大一倍,以下方法中最宜采用的是( )
A.加熱濃縮到原來體積的一半
B.加入0.05mol/L的鹽酸0.125V L
C.加入10mol/L的鹽酸0.1V L,再稀釋至1.5 V L
D.標況下通入11.2L氯化氫氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖為A、B、C、D、E之間的相互轉換關系A為一種氣態單質,D是一種紅棕色氣體。下列說法正確的是
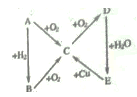
A. C 物質和O2必須在催化劑表面才能反應生成D
B. Cu 和E 溶液反應體現了E 的強氧化性和酸性
C. 可用NaOH 溶液除去混在D物質中的少量B 物質
D. B 生成C 的反應中,氧化劑與還原劑之比為4: 5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應的產物中,有的有同分異構體,有的沒有同分異構體,其中一定不存在同分異構體的反應是
A. 異戊二烯(![]() )與等物質的量的Br2發生加成反應
)與等物質的量的Br2發生加成反應
B. 2—氯丁烷(![]() )與NaOH乙醇溶液共熱發生消去HCl分子的反應
)與NaOH乙醇溶液共熱發生消去HCl分子的反應
C. 甲苯在一定條件下發生硝化生成一硝基甲苯的反應
D. 2—丙醇一定條件下發生消去反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖表示某種有機物的結構,關于它的性質敘述中正確的是

A. 1mol該有機物在一定條件下,能與7molH2發生加成反應
B. 不能與FeCl3溶液作用發生顯色反應
C. 能與NaHCO3反應放出氣體
D. 1mol該有機物在一定條件下,能與8molNaOH反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫代硫酸鈉(Na2S2O3)可由亞硫酸鈉和硫粉通過化合反應制得。
已知:①Na2S2O3在酸性溶液中不能穩定存在;
②硫代硫酸鈉與碘反應的離子方程式為:2S2O32-+I2 = S4O62- + 2I- 。
(Ⅰ)制備Na2S2O3·5H2O

①打開K1,關閉K2,向放有銅片的圓底燒瓶中加入足量濃硫酸,加熱。圓底燒瓶中發生反應的化學方程式為___________________________________________。
②C中混合液被氣流攪動,反應一段時間后,硫粉的量逐漸減少。C中碳酸鈉的作用是_____。“停止C中的反應”的操作是____________________。
③過濾C中的混合液。將濾液加熱濃縮、冷卻結晶、過濾、洗滌、烘干,得到產品。
④裝置B中盛放的試劑是(填化學式)_____________溶液,其作用是__________________。
(Ⅱ)用I2的標準溶液測定產品的純度
取5.5g產品,配制成100mL溶液。取10.00mL溶液,以淀粉溶液為指示劑,用濃度為0.050mol/L I2的標準溶液進行滴定,相關數據記錄如下表所示:
編號 | 1 | 2 | 3 |
溶液的體積/mL | 10.00 | 10.00 | 10.00 |
消耗I2標準溶液的體積/mL | 19.95 | 17.10 | 20.05 |
①滴定時,達到滴定終點的現象是______________________________。
②Na2S2O3·5H2O在產品中的質量分數是___________(用百分數表示,且保留1位小數)。
③下列操作中可能使測定結果偏低的是________(填字母)。
A.酸式滴定管未用標準液潤洗就直接注入I2的標準液
B.滴定前盛放Na2S2O3溶液的錐形瓶用蒸餾水洗凈后沒有干燥
C.酸式滴定管尖嘴部分在滴定前沒有氣泡,滴定后有氣泡
D.讀取I2標準液時,開始仰視讀數,滴定結束時俯視讀數
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com