
| A. | ②④⑥⑦ | B. | ③⑤⑥⑦ | C. | ④⑤⑥ | D. | ①②③ |
分析 ①濃鹽酸隨反應的進行濃度減小,當減小到一定濃度不再和二氧化錳反應.
②18.4mol/L的硫酸為濃硫酸,常溫下遇到鐵、鋁金屬發生的鈍化,不再繼續反應.
③向100mL3mol/L的硝酸中加入5.6g鐵根據反應的量,鐵全部反應生成二價鐵離子和三價鐵離子;
④合成氨的反應是可逆反應,不可能完全轉化;
⑤將足量鋅粉投入到50mL 18mol•L-1的硫酸中,首先生成二氧化硫,當濃硫酸轉化為稀硫酸時與反應生成氫氣,所以硫酸完全轉化;
⑥將足量Ca(ClO)2投入到20mL 10mol•L-1鹽酸中,發生歸中反應生成氯氣;
⑦將足量銅投入到50mL 12mol•L-1的硝酸中,首先生成二氧化氮,后來生成一氧化氮氣體,硝酸完全轉化.
解答 解:①濃鹽酸濃度變稀到一定濃度不會和二氧化錳發生氧化還原反應,故錯誤;
②標準狀況下,鋁片遇濃硫酸發生鈍化,阻止反應進行,故錯誤;
③根據反應Fe+4HNO3=Fe(NO3)3+NO+2H2O,0.3mol硝酸氧化0.075mol鐵為三價鐵離子,剩余0.025mol鐵會繼續和生成的0.1mol三價鐵離子反應,依據反應2Fe3++Fe=3Fe2+ 可知剩余0.025mol鐵全部溶解需要三價鐵離子0.05mol,故正確;
④合成氨的反應是可逆反應,不可能完全轉化,故錯誤;
⑤將足量鋅粉投入到50mL 18mol•L-1的硫酸中,首先生成二氧化硫,當濃硫酸轉化為稀硫酸時與反應生成氫氣,所以硫酸完全轉化,故正確;
⑥將足量Ca(ClO)2投入到20mL 10mol•L-1鹽酸中,發生歸中反應生成氯氣,鹽酸完全轉化,故正確;
⑦將足量銅投入到50mL 12mol•L-1的硝酸中,首先生成二氧化氮,后來生成一氧化氮氣體,硝酸完全轉化,故正確;
故選B.
點評 本題考查氯氣實驗室制備中試劑的過程反應,常溫下鋁、鐵在濃硫酸中鈍化,變價金屬鐵與硝酸反應量不同產物不同及其有關過量計算方法,化學反應的可逆性,一定條件下達到平衡.注意審清題意,物質反應時條件不同產物不同,量不同產物不同.


科目:高中化學 來源: 題型:選擇題
 將1molH2(g)和2mol I2(g)置于某2L密閉容器中,在一 定溫度下發生反應:H2(g)+I2(g)?2HI(g)△H<0,并達到平衡,HI的體積分數ω(HI)隨時間變化如曲線如圖(Ⅱ)所示.若改變反應條件,ω(HI)的變化曲線如圖(Ⅰ)所示,則改變的條件可能是( )
將1molH2(g)和2mol I2(g)置于某2L密閉容器中,在一 定溫度下發生反應:H2(g)+I2(g)?2HI(g)△H<0,并達到平衡,HI的體積分數ω(HI)隨時間變化如曲線如圖(Ⅱ)所示.若改變反應條件,ω(HI)的變化曲線如圖(Ⅰ)所示,則改變的條件可能是( )| A. | 恒溫恒容加入適當催化劑 | B. | 恒溫條件縮小體積 | ||
| C. | 恒容條件下升高溫度 | D. | 恒溫條件擴大反應容器 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 干冰用于人工降雨 | |
| B. | 蔗糖中加入濃硫酸,蔗糖變黑,體積膨脹 | |
| C. | 溶洞中鐘乳石的形成 | |
| D. | 豆科作物的根瘤菌對空氣中氮的固定 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
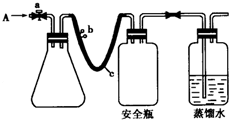 實驗室用如圖方法測定某水樣中O2的含量.
實驗室用如圖方法測定某水樣中O2的含量.查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
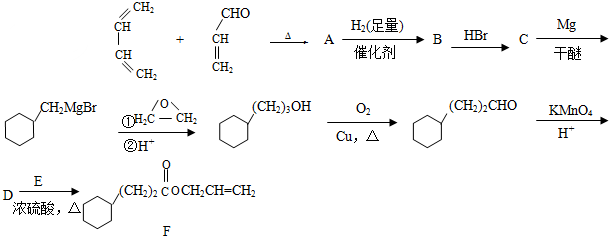
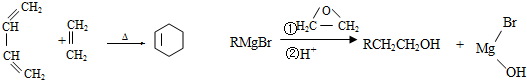
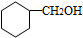 .
. .
. .
.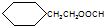
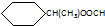 .
.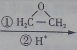 CH3CH2CH2CH2OH(其他試劑任選).
CH3CH2CH2CH2OH(其他試劑任選).查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | |||||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑧ | ⑩ | ||
| 4 | ② | ④ | ⑨ |
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com