
| A. | 原子半徑:D>E>C>B>A | |
| B. | 熱穩定性:EA4>A2C | |
| C. | 單質D可用海水作原料獲得 | |
| D. | 化合物DC與化合物EC2中化學鍵類型相同 |
分析 A、B、C、D、E是短周期中原子序數依次增大的5種元素.A、B形成的氣態化合物的水溶液呈堿性,應為NH3,則A為H元素,B為N元素;D原子最外層電子數與最內層電子數相等,原子序數比N元素大,則D為Mg元素;B、C同周期,則C為第二周期元素,D與C形成的化合物是一種耐高溫材料,應為MgO,則C為O元素;A、B、C、D的原子序數之和是1+7+8+12=28,是E的兩倍,則E的原子序數為14,E為Si元素,根據元素對應的單質、化合物的性質結合元素周期律知識解答該題.
解答 解:A、B、C、D、E是短周期中原子序數依次增大的5種元素.A、B形成的氣態化合物的水溶液呈堿性,應為NH3,則A為H元素,B為N元素;D原子最外層電子數與最內層電子數相等,原子序數比N元素大,則D為Mg元素;B、C同周期,則C為第二周期元素,D與C形成的化合物是一種耐高溫材料,應為MgO,則C為O元素;A、B、C、D的原子序數之和是1+7+8+12=28,是E的兩倍,則E的原子序數為14,E為Si元素.
A.A為H元素,原子序數最小,B、C為N、O元素,位于第二周期,D、E為Mg、Si元素,位于第三周期,原子核外電子層數越多,半徑越大,同周期元素原子序數越大,半徑越小,則有原子半徑:D>E>B>C>A,故A錯誤;
B.由于非金屬性:Si<O,非金屬性越大,對應的氫化物越穩定,則熱穩定性:SiH4<H2O,故B錯誤;
C.從海水中提取鎂,通常將熟石灰加入海水中,沉淀出氫氧化鎂,氫氧化鎂與鹽酸反應生成氯化鎂,電解熔融狀態的氯化鎂制得金屬鎂,故C正確;
D.化合物MgO含有離子鍵,化合物SiO2中共價鍵,化學鍵類型不一樣,故D錯誤.
故選C.
點評 本題考查元素的推斷、元素周期律以及對應元素化合物的性質,題目難度不大,注意常見元素化合物的性質.


 陽光課堂課時優化作業系列答案
陽光課堂課時優化作業系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
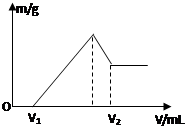 將0.1molMg、Al混合物溶于100mL4mol/L的鹽酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的過程中,沉淀質量m與NaOH溶液的體積V的變化如圖所示.
將0.1molMg、Al混合物溶于100mL4mol/L的鹽酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的過程中,沉淀質量m與NaOH溶液的體積V的變化如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在含Ba(OH)2、KOH的混合溶液中緩慢通入CO2:Ba(OH)2、KOH、K2CO3、BaCO3 | |
| B. | 在含NH4+、Al3+、H+的溶液中逐滴加入KOH溶液:H+、Al3+、NH4+、Al(OH)3 | |
| C. | 在含AlO2-、OH-、CO32-的溶液中逐滴加入鹽酸:AlO2-、Al(OH)3、OH-、CO32- | |
| D. | 在含等物質的量的Fe2+、Ag+、Cu2+、H+的溶液中加入鋅粉:Ag+、Cu2+、H+、Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 可逆反應X2(g)+3Y2(g)═2Z2(g)在一密閉容器中進行,如圖是該過程中的反應速率(v)與時間(t)的關系曲線,下列敘述正確的是( )
可逆反應X2(g)+3Y2(g)═2Z2(g)在一密閉容器中進行,如圖是該過程中的反應速率(v)與時間(t)的關系曲線,下列敘述正確的是( )| A. | t2-t3,各物質的濃度不再發生變化 | |
| B. | t3時刻改變溫度,該反應限度不會改變 | |
| C. | t2-t3,反應不再發生 | |
| D. | t1時,反應只向正方向進行 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com