
【題目】煤化工中常需研究不同溫度下的平衡常數、投料比及產率等問題。已知:CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常數隨溫度的變化如下,試回答下列問題:
CO2(g)+H2(g)的平衡常數隨溫度的變化如下,試回答下列問題:
溫度/℃ | 400 | 500 | 830 | 1000 |
平衡常數K | 10 | 9 | 1 | 0.6 |
(1)該反應的平衡常數表達式K=__________。該反應的正反應是______反應(填“放熱”或“吸熱”)。
(2)某溫度下,上述反應達到平衡后,恒容、升高溫度,原化學平衡向______反應方向移動(填“正”或“逆”),容器內混合氣體的壓強________(填“增大”、“減小”或“不變”)。
(3)能判斷該反應是否達到化學平衡狀態的依據是(_____)
a.容器中壓強不變b.混合氣體中c(CO)不變
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)830℃,在恒容反應器中發生如表中的反應,按表中的物質的量投入反應混合物,其中向正反應方向進行的有__________(選填A、B、C、D)
n(CO) | n(H2O) | n(H2) | n(CO2) | |
A | 1 | 5 | 2 | 3 |
B | 2 | 2 | 1 | 1 |
C | 3 | 3 | 0 | 0 |
D | 0. | 2 | 1 | 1 |
【答案】 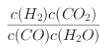 放熱 逆 增大 bc BC
放熱 逆 增大 bc BC
【解析】(1)![]()
![]() ,反應的平衡常數
,反應的平衡常數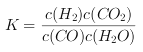 ;根據表中數據可以知道,溫度升高平衡常數減小,說明平衡向逆反應方向移動,正反應為放熱反應,正確答案:
;根據表中數據可以知道,溫度升高平衡常數減小,說明平衡向逆反應方向移動,正反應為放熱反應,正確答案: 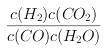 ;放熱。
;放熱。
(2) 反應是放熱反應,溫度升高,反應速率增大,平衡向逆反應方向移動,反應前后氣體體積不變,等容容器中壓強之比等于溫度之比,所以壓強增大,正確答案:逆;增大;增大。
(3) 反應前后氣體體積不變,壓強始終不會變化,所以壓強不變,無法判斷是否達到平衡狀態,a錯誤 ;濃度不變,反應達到了化學平衡狀態,b正確;正、逆反應速率相等,各組分濃度不變,達到了化學平衡狀態,c正確;濃度相等時,不能判斷各組分濃度是否不變,無法判斷是否達到平衡狀態,故d錯誤;正確選項bc。
(4)根據![]() 時,平衡常數
時,平衡常數![]() 計算:
計算:
根據濃度商![]() ,反應向逆反應方向移動,A錯誤;根據濃度商
,反應向逆反應方向移動,A錯誤;根據濃度商![]() ,反應向正反應方向移動,B正確;只有反應物,反應向正反應方向移動,C正確; 根據濃度商
,反應向正反應方向移動,B正確;只有反應物,反應向正反應方向移動,C正確; 根據濃度商![]() .達到平衡狀態,平衡不移動,D錯誤;正確答案:BC。
.達到平衡狀態,平衡不移動,D錯誤;正確答案:BC。


科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列說法正確的是
A. 常溫常壓下,28g由C2H4和C3H6組成的混合氣體所含原子數為6NA
B. 由0.1mol雙氧水參加反應生成氧氣,轉移的電子總數一定為0.2NA
C. 0.lmol/L(NH4)2SO4溶液與0.2mol/LNH4Cl溶液中的NH4+數目相同
D. 2.4gT218O所含中子數為1.2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是某學校購買的硫酸試劑標簽上的部分內容.據此下列說法正確的是( )

A. 該硫酸的物質的量濃度為1.84mol/L
B. 1mol Zn與足量的該硫酸反應產生2gH2
C. 配制200mL 4.6mol/L的稀硫酸需取該硫酸50mL
D. 該硫酸與等體積的水混合所得溶液的物質的量濃度等于9.2mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了探究HCl、H2CO3和H2SiO3的酸性強弱,某學生設計了如圖所示的實驗裝置,一次實驗即可達到實驗目的(不必選用其他酸性物質)請回答下列問題:
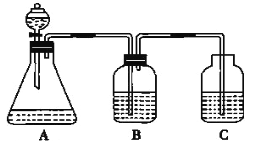
(1)錐形瓶中裝有某種可溶性正鹽溶液,則分液漏斗中所盛試劑應為_______。
(2)裝置B中所盛的試劑是_______,其作用是_______。
(3)裝置C中所盛的試劑是_______,C中所發生反應的離子方程式為_______。
(4)由此得出HCl、H2CO3、H2SiO3的酸性強弱順序是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了檢驗某溶液中是否含有常見的四種無機離子,某化學小組的同學進行了如下所示的實驗操作。其中檢驗過程中產生的氣體能使濕潤的紅色石蕊試紙變藍。由該實驗能得出的正確結論是( )

A.原溶液中一定含有SO42- B.原溶液中一定含有NH4+
C.原溶液中一定含有Cl- D.原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在FeCl3和CuCl2的混合液中逐漸加入鐵粉,溶液中Fe2+的物質的量濃度和加入鐵粉的物質的量之間關系如圖所示。則該溶液中FeCl3與CuCl2的物質的量濃度之比為

A. 3∶1 B. 1∶2 C. 2∶1 D. 1∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硅是無機非金屬材料的主角,硅的氧化物和硅酸鹽約占地殼質量的90%以上。
(1)計算機芯片和太陽能電池的主要成分是________,光導纖維的主要成分是___________。
(2)工藝師常用氫氟酸來雕刻玻璃,該反應的化學方程式為__________。
(3)工業上可利用水玻璃和鹽酸反應制備硅酸凝膠后,進一步脫水處理可得到硅膠,寫出水玻璃和鹽酸反應的離子方程式_______。
(4)玉石的主要成分基本都屬于硅酸鹽,翡翠的主要成分為NaAlSi2O6,將其表示為氧化物形式為___。
(5)高純度單晶硅可以按下列方法制備:
SiO2 ![]() Si(粗)
Si(粗) ![]() SiHCl3
SiHCl3 ![]() Si(純)
Si(純)
寫出步驟①的化學方程式_______________________________________。
步驟②的產物經過冷凝后得到的SiHCl3(沸點33.0℃)中含有少量的SiCl4(沸點57.6℃),提純SiHCl3主要操作的名稱是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是( )
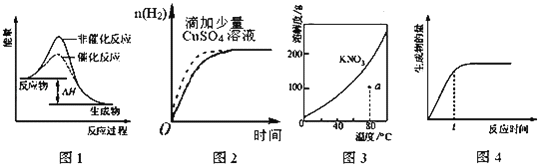
A. 圖1表示某吸熱反應分別在有、無催化劑的情況下反應過程中的能量變化
B. 圖2表示常溫下,等量鋅粉與足量的等濃度的鹽酸反應(滴加CuSO4溶液的為虛線)
C. 圖3表示KNO3的溶解度曲線,a點所示的溶液是80℃時KNO3的不飽和溶液
D. 圖4表示某可逆反應生成物的量隨反應時間變化的曲線,t時反應物轉化率最大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是以鉛蓄電池為電源,模擬氯堿工業電解飽和食鹽水的裝置圖(C、D均為石墨電極)。
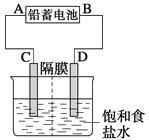
已知:鉛蓄電池在放電時發生下列電極反應:
負極Pb+SO![]() -2e-===PbSO4
-2e-===PbSO4
正極PbO2+4H++SO![]() +2e-===PbSO4+2H2O
+2e-===PbSO4+2H2O
(1)請寫出電解飽和食鹽水的化學方程式_______________________________________。
(2)若在電解池中C極一側滴酚酞試液,電解一段時間后未呈紅色,說明鉛蓄電池的A極為________極。
(3)用鉛蓄電池電解1 L飽和食鹽水(食鹽水足量)時,
①若收集到11.2 L(標準狀況下)氯氣,溶液pH=_________________。
②若鉛蓄電池消耗H2SO4 2 mol,則可收集到H2的體積(標準狀況下)為___________L。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com