
| A. | 體積 | B. | 原子個數 | C. | 質量 | D. | 電子數 |
分析 同溫同壓下,氣體摩爾體積相等,根據N=nNA、m=nM進行有關計算,注意水分子與氨氣分子的結構特點:水分子為3原子分子,含有10個電子;氨氣分子為4原子分子,含有10個電子.
解答 解:A.如果水是液體時,氣體摩爾體積對其不適用,雖然二者物質的量相等,但其體積不等,故A錯誤;
B.水分子為3原子分子,氨氣分子為4原子分子,含相同分子數的H2O和NH3,原子個數之比為:3:4,故B錯誤;
C.依據N=nNA、m=nM,含相同分子數的H2O和NH3物質的量相等,質量之比為18:17,故C錯誤;
D.1個氨氣分子和1個水分子都含有10個電子,則含相同分子數的H2O和NH3一定具有相同的電子數,故D正確;
故選:D.
點評 本題考查了物質的量的有關計算,靈活運用物質的量有關公式解答即可,注意氣體摩爾體積的適用范圍及適用條件,易錯選項是A.


科目:高中化學 來源: 題型:選擇題
| A. | 鈉與氧氣直接反應不能得到Na2O2 | |
| B. | Na2O2遇水劇烈反應放出O2,且每生成1 mol O2轉移2 mol電子 | |
| C. | Na2O2與CO2可以反應放出O2,因此可以用作潛水艇的供氧劑 | |
| D. | Na2O2在空氣中長時間暴露最后會生成Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4HCO3溶液與過量KOH濃溶液:NH4++OH-═NH3↑+H2O | |
| B. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好為中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 稀硝酸和過量的鐵屑反應:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | Fe(OH)3溶于氫碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ①②③ | C. | ①②③④ | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子中含有兩個氫原子的酸一定是二元酸 | |
| B. | “血液透析”利用了膠體的性質 | |
| C. | Na2O、Na2O2組成元素相同,與CO2反應產物相同 | |
| D. | 鋼鐵發生電化學腐蝕時,負極的電極反應式為Fe-3e-═Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,100 mL 1 mol•L-1 Na2CO3溶液中含有的陰離子數大于0.1NA | |
| B. | 常溫常壓下,28g14CO和N2的混合物所含的質子數為14NA | |
| C. | 將NA個NH3分子溶于1L水中得到1 mol•L-1的氨水 | |
| D. | 1molCl2分別與足量的鐵或氫氧化鈉溶液反應,轉移電子數均為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
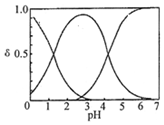 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三種形態的粒子的分布分數δ隨溶液pH變化的關系如圖所示[已知Ksp(CaC2O4)=2.3×10-9].下列說法正確的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三種形態的粒子的分布分數δ隨溶液pH變化的關系如圖所示[已知Ksp(CaC2O4)=2.3×10-9].下列說法正確的是( )| A. | 0.1mol•L-1H2C2O4溶液使KMnO4溶液褪色的離子方程式:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| B. | 0.1 mol•L-1 NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| C. | pH=5時,溶液中主要含碳微粒濃度大小關系為:c(C2O42-)>c(H2C2O4)>c(HC2O4-) | |
| D. | 一定溫度下,往CaC2O4飽和溶液中加入少量CaCl2固體,c(C2O42-)將減小,c(Ca2+)不變 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com